Белки — это высокомолекулярные органические соединения, биополимеры, построенные из 20 видов L-?-аминокислотных остатков, соединенных в определенной последовательности в длинные цепи. Молекулярная масса белков варьируется от 5 тысяч до 1 миллиона. Название «белки» впервые было дано веществу птичьих яиц, свертывающемуся при нагревании в белую нерастворимую массу. Позднее этот термин был распространен на другие вещества с подобными свойствами, выделенные из животных и растений.
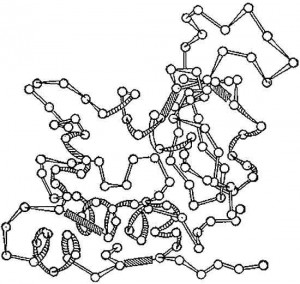
Рис. 1. Наиболее сложными биополимерами являются белки. Их макромолекулы состоят из мономеров, которыми являются аминокислоты. Каждая аминокислота имеет две функциональные группы: карбоксильную и аминогруппу. Все разнообразие белков создается в результате различных сочетаний 20 аминокислот.
Белки преобладают над всеми другими присутствующими в живых организмах соединениями, составляя, как правило, более половины их сухого веса. Предполагается, что в природе существует несколько миллиардов индивидуальных белков (например, только в бактерии кишечной палочки присутствует более 3 тысяч различных белков).
Белки играют ключевую роль в процессах жизнедеятельности любого организма. К числу белков относятся ферменты, при участии которых протекают все химические превращения в клетке (обмен веществ); они управляют действием генов; при их участии реализуется действие гормонов, осуществляется трансмембранный транспорт, в том числе генерация нервных импульсов. Они являются неотъемлемой частью иммунной системы (иммуноглобулины) и системы свертывания крови, составляют основу костной и соединительной ткани, участвуют в преобразовании и утилизации энергии.
Первые попытки выделить белки были предприняты еще в 18 веке. К началу 19 века появляются первые работы по химическому изучению белков. Французские ученые Жозеф Луи Гей-Люссак и Луи Жак Тенар попытались установить элементный состав белков из разных источников, что положило начало систематическим аналитическим исследованиям, благодаря которым был сделан вывод о том, что все белки сходны по набору элементов, входящих в их состав. В 1836 голландский химик Г. Я. Мульдер предложил первую теорию строения белковых веществ, согласно которой все белки имеют некий гипотетический радикал (С40H62N10O12), связанный в различных пропорциях с атомами серы и фосфора. Он назвал этот радикал «протеином» (от греческого protein — первый, главный). Теория Мульдера способствовала увеличению интереса к изучению белков и совершенствованию методов белковой химии. Были разработаны приемы выделения белков путем экстракции растворами нейтральных солей, впервые были получены белки в кристаллической форме (гемоглобин, некоторые белки растений). Для анализа белков стали использовать их предварительное расщепление с помощью кислот и щелочей.
Одновременно все большее внимание стало уделяться изучению функции белков. Йенс Якоб Берцелиус в 1835 первым высказал предположение о том, что они играют роль биокатализаторов. Вскоре были открыты протеолитические ферменты — пепсин (Т. Шванн, 1836) и трипсин (Л. Корвизар, 1856), что привлекло внимание к физиологии пищеварения и анализу продуктов, образующихся в ходе расщепления пищевых веществ. Дальнейшие исследования структуры белка, работы по химическому синтезу пептидов завершились появлением пептидной гипотезы, согласно которой все белки построены из аминокислот. К концу 19 века было изучено большинство аминокислот, входящих в состав белков.
В начале 20 века немецкий химик Эмиль Герман Фишер впервые применил методы органической химии для изучения белков и доказал, что белки состоят из ?-аминокислот, связанных между собой амидной (пептидной) связью. Позже, благодаря использованию физико-химических методов анализа, была определена молекулярная масса многих белков, установлена сферическая форма глобулярных белков, проведен рентгеноструктурный анализ аминокислот и пептидов, разработаны методы хроматографического анализа (см. хроматография).
Был выделен первый белковый гормон — инсулин (Фредерик Грант Бантинг, Джон Джеймс Рикард Маклеод, 1922), доказано присутствие гамма -глобулинов в антителах, описана ферментативная функция мышечного белка миозина (Владимир Александрович Энгельгардт, М. Н. Любимова, 1939). Впервые в кристаллическом виде были получены ферменты — уреаза (Дж. Б. Салинер, 1926), пепсин (Дж. Х. Нортрон, 1929), лизоцим (Э. П. Абрахам, Роберт Робинсон, 1937).
Рис. 2. Схема трёхмерной структуры фермента лизоцима. Кружки — аминокислоты; тяжи — пептидные связи; заштрихованные прямоугольники — дисульфидные связи. Видны спирализованные и вытянутые участки полипептидной цепи.
В 1950-х годах была доказана трехуровневая организация белковых молекул — наличие у них первичной, вторичной и третичной структуры; создали автоматический анализатор аминокислот (Станфорд Мур, Уильям Хауард Стайн, 1950). В 60-х годы были предприняты попытки химического синтеза белков (инсулин, рибонуклеаза). Существенно усовершенствовались методы рентгеноструктурного анализа; был создан прибор — секвенатор (П. Эдман, Г. Бэгг, 1967), позволявший определять последовательность аминокислот в полипептидной цепи. Следствием этого явилось установление структуры нескольких сотен белков из самых разных источников. Среди них протеолитические ферменты (пепсин, трипсин, химотрипсин, субтилизин, карбоксипептидазы), миоглобины, гемоглобины, цитохромы, лизоцимы, иммуноглобулины, гистоны, нейротоксины, белки вирусных оболочек, белково-пептидные гормоны. В результате появились предпосылки для решения актуальных проблем энзимологии, иммунологии, эндокринологии и других областей биологической химии.
В конце 20 века значительные успехи были достигнуты в изучении роли белков в ходе матричного синтеза биополимеров, понимания механизмов их действия в различных процессах жизнедеятельности организмов, установления связи между их структурой и функцией. Огромное значение при этом имело совершенствование методов исследования, появление новых способов для разделения белков и пептидов.
Разработка эффективного метода анализа последовательности расположения нуклеотидов в нуклеиновых кислотах позволила значительно облегчить и ускорить определение аминокислотной последовательности в белках. Это оказалось возможным потому, что порядок расположения аминокислот в белке определяется последовательностью нуклеотидов в кодирующем этот белок гене (фрагменте ДНК). Следовательно, зная расстановку нуклеотидов в этом гене и генетический код, можно безошибочно предсказать, в каком порядке располагаются аминокислоты в полипептидной цепи белка. Наряду с успехами в структурном анализе белков значительные результаты были достигнуты в изучении их пространственной организации, механизмов образования и действия надмолекулярных комплексов, в том числе рибосом и других клеточных органелл, хроматина, вирусов и т. д.
Практически все белки построены из 20 ?-аминокислот, принадлежащих к L-ряду, и одинаковых практически у всех организмов. Аминокислоты в белках соединены между собой пептидной связью —СО—NH—, которая образуется карбоксильной и ?-аминогруппой соседних аминокислотных остатков: две аминокислоты образуют дипептид, в котором остаются свободными концевые карбоксильная (—СООН) и аминогруппа (H2N—), к которым могут присоединяться новые аминокислоты, образуя полипептидную цепь.
Участок цепи, на котором находится концевая Н2N-группа, называют N-концевым, а противоположный ему — С-концевым. Огромное разнообразие белков определяется последовательностью расположения и количеством входящих в них аминокислотных остатков. Хотя четкого разграничения не существует, короткие цепи принято называть пептидами или олигопептидами (от олиго…), а под полипептидами (белками) понимают обычно цепи, состоящие из 50 и более аминокислот. Наиболее часто встречаются белки, включающие 100-400 аминокислотных остатков, но известны и такие, молекула которых образована 1000 и более остатками. Белки могут состоять из нескольких полипептидных цепей. В таких белках каждая полипептидная цепь носит название субъединицы.
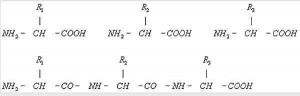
Рис. 3. Белок всех организмов состоит из 20 видов аминокислот. Каждый белок характеризуется определённым ассортиментом и количественным соотношением аминокислот. В молекулах белков аминокислоты соединены между собой пептидными связями (— СО — NH —) в линейной последовательности, составляющей так называемую первичную структуру белка. Верхняя строка — свободные аминокислоты с боковыми группами R1, R2, R3; нижняя строка — аминокислоты соединены пептидными связями.
Полипептидная цепь способна самопроизвольно формировать и удерживать особую пространственную структуру. Исходя из формы белковых молекул белки делят на фибриллярные и глобулярные. В глобулярных белках одна или несколько полипептидных цепей свернуты в компактную структуру сферической формы, или глобулу. Обычно эти белки хорошо растворимы в воде. К их числу относятся почти все ферменты, транспортные белки крови и многие запасные белки. Фибриллярные белки представляют собой нитевидные молекулы, скрепленные друг с другом поперечными связями и образующие длинные волокна или слоистые структуры. Они обладают высокой механической прочностью, нерастворимы в воде и выполняют главным образом структурные и защитные функции. Типичными представителями таких белков являются кератины волос и шерсти, фиброин шелка, коллаген сухожилий.
Порядок расположения ковалентно связанных аминокислот в полипептидной цепи называют аминокислотной последовательностью, или первичной структурой белков. Первичная структура каждого белка, кодируемая соответствующим геном, постоянна и несет в себе всю информацию, необходимую для формирования структур более высокого уровня. Потенциально возможное число белков, которые могут образоваться из 20 аминокислот, практически не ограничено.
В результате взаимодействия боковых групп аминокислотных остатков отдельные относительно небольшие участки полипептидной цепи принимают ту или иную конформацию (тип укладки), известную как вторичная структура белков. Наиболее характерными элементами ее являются периодически повторяющиеся ?-спираль и ?-структура. Вторичная структура весьма стабильна. Так как она в значительной мере определяется аминокислотной последовательностью соответствующего участка белка, становится возможным ее предсказание с определенной степенью вероятности. Термин «?-спираль» был введен американским биохимиком, физиком и химиком Лайнусом Карлом Полингом, описавшим укладку полипептидной цепи в белке ?-кератине в виде правосторонней спирали (?-спираль можно сравнить со шнуром от телефонной трубки). На каждый виток такой спирали в белке приходится 3,6 аминокислотных остатков. Это означает, что группа —С= О одной пептидной связи образует водородную связь с группой —NH другой пептидной связи, отстоящей от первой на четыре аминокислотных остатка. В среднем каждый ?-спиральный участок включает до 15 аминокислот, что соответствует 3-4 оборотам спирали. Но в каждом отдельном белке длина спирали может сильно отличаться от этой величины. В поперечном сечении ?-спираль имеет вид диска, от которого наружу направлены боковые цепи аминокислот.
?-структура, или ? -складчатый слой, может быть образована несколькими участками полипептидной цепи. Эти участки растянуты и уложены параллельно друг другу, связываясь между собой водородными связями, которые возникают между пептидными связями. Они могут быть ориентированы в одном и том же или в противоположных направлениях (направление движения вдоль полипептидной цепи принято считать от N-конца к С-концу). В первом случае складчатый слой называют параллельным, во втором — антипараллельным. Последний образуется, когда пептидная цепь делает резкий поворот вспять, образуя изгиб (? -изгиб). Боковые цепи аминокислот ориентированы перпендикулярно плоскости ? -слоя.
Относительное содержание ? -спиральных участков и ? -структур может широко варьироваться в разных белках. Существуют белки с преобладанием ?-спиралей (около 75% аминокислот в миоглобине и гемоглобине), а основным типом укладки цепи во многих фибриллярных белках (в том числе фиброин шелка, ?-кератин) является ? -структура. Участки полипептидной цепи, которые нельзя отнести ни к одной из вышеописанных конформаций, называют соединительными петлями. Их структура определяется главным образом взаимодействиями между боковыми цепями аминокислот, и в молекуле любого белка она укладывается строго определенным образом.
Третичной структурой называют пространственное строение глобулярных белков. Но часто это понятие относят к характерному для каждого конкретного белка способу сворачивания полипептидной цепи в пространстве. Третичная структура формируется полипептидной цепью белка самопроизвольно, по-видимому, по определенному пути (путям) свертывания с предварительным образованием элементов вторичной структуры. Если стабильность вторичной структуры обусловлена водородными связями, то третичная структура фиксируется разнообразной системой нековалентных взаимодействий: водородными, ионными, межмолекулярными взаимодействиями, а также гидрофобными контактами между боковыми цепями неполярных аминокислотных остатков.
В некоторых белках третичная структура дополнительно стабилизируется за счет образования дисульфидных связей (—S—S—-связей) между остатками цистеина. Как правило, внутри белковой глобулы расположены боковые цепи гидрофобных аминокислот, собранные в ядро (их перенос внутрь глобулы белка выгоден термодинамически), а на периферии находятся гидрофильные остатки и часть гидрофобных. Белковую глобулу окружает несколько сотен молекул гидратной воды, необходимой для стабильности молекулы белка и нередко участвующей в его функционировании. Третичная структура подвижна, отдельные ее участки могут смещаться, что приводит к конформационным переходам, которые играют значительную роль во взаимодействии белка с другими молекулами.
Третичная структура является основой функциональных свойств белка. Она определяет образование в белке ансамблей функциональных групп — активных центров и зон связывания, придает им необходимую геометрию, позволяет создать внутреннюю среду, являющуюся предпосылкой протекания многих реакций, обеспечивает взаимодействие с другими белками.
Третичная структура белков однозначно соответствует его первичной структуре; вероятно, существует еще нерасшифрованный стереохимический код, определяющий характер свертывания белка. Однако один и тот же способ укладки в пространстве обычно соответствует не единственной первичной структуре, а целому семейству структур, в которых совпадать может лишь небольшая доля (до 20-30%) аминокислотных остатков, но при этом в определенных местах цепи сходство аминокислотных остатков сохраняется. Результатом является образование обширных семейств белков, характеризующихся близкой третичной и более или менее сходной первичной структурой и, как правило, общностью функции. Таковы, например, белки организмов разных видов, несущие одинаковую функцию и эволюционно родственные: миоглобины и гемоглобины, трипсин, химотрипсин, эластаза и другие протеиназы животных.
Рис. 4. В результате соединения нескольких белковых макромолекул, обладающих третичной структурой, в сложный комплекс формируется четвертичная структура белка. Примером таких сложных белков является гемоглобин, состоящий из четырех макромолекул.
Нередко, особенно в крупных белках, сворачивание полипептидной цепи проходит через формирование отдельными участками цепи более или менее автономных элементов пространственной структуры — доменов, которые могут обладать функциональной автономией, будучи ответственными за ту или иную биологическую активность белка. Так, N-концевые домены белков системы свертывания крови обеспечивают их присоединение к клеточной мембране.
Существует много белков, молекулы которых представляют собой ансамбль из глобул (субъединиц), удерживаемых вместе за счет гидрофобных взаимодействий, водородных или ионных связей. Такие комплексы называют олигомерными, мультимерными или субъединичными белками. Укладку субъединиц в функционально активном белковом комплексе называют четвертичной структурой белка. Некоторые белки способны образовывать структуры более высоких порядков, например, полиферментные комплексы, протяженные структуры (белки оболочек бактериофагов), надмолекулярные комплексы, функционирующие как единое целое (например, рибосомы или компоненты дыхательной цепи митохондрий).
Четвертичная структура позволяет создать молекулы необычной геометрии. Так, у ферритина, образованного 24 субъединицами, имеется внутренняя полость, благодаря которой белку удается связать до 3000 ионов железа. Кроме того, четвертичная структура позволяет в одной молекуле выполнять несколько различных функций. В триптофансинтетазе совмещены ферменты, ответственные за несколько последовательных стадий синтеза аминокислоты триптофана.
Первичная структура белков определяет все остальные уровни организации белковой молекулы. Поэтому при изучении биологической функции различных белков важно знание этой структуры. Первым белком, для которого была установлена аминокислотная последовательность, был гормон поджелудочной железы — инсулин. Эта работа, потребовавшая 11 лет, была выполнена английским биохимиком Фредериком Сенгером (1954). Он определил расположение 51 аминокислоты в молекуле гормона и показал, что она состоит из 2-х цепей, соединенных дисульфидными связями. Позже большая часть работ по установлению первичной структуры белков была автоматизирована.
С развитием методов генетической инженерии появилась возможность еще более ускорить этот процесс, определяя первичную структуру белков в соответствии с результатами анализа нуклеотидной последовательности в генах, кодирующих эти белки. Вторичную и третичную структуру белков исследуют с помощью достаточно сложных физических методов, например, кругового дихроизма или рентгеноструктурного анализа белковых кристаллов. Третичная структура была впервые установлена английским биохимиком Джоном Коудери Кендрю (1957) для белка мышц — миоглобина.
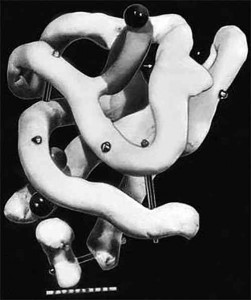
Рис. 5. Модель молекулы миоглобина (пространственная конфигурация молекулы)
Сравнительно слабые связи, ответственные за стабилизацию вторичной, третичной и четвертичной структур белка, легко разрушаются, что сопровождается потерей его биологической активности. Разрушение исходной (нативной) структуры белка, называемое денатурацией, происходит в присутствии кислот и оснований, при нагревании, изменении ионной силы и других воздействиях. Как правило, денатурированные белки плохо или совсем не растворяются в воде. При непродолжительном действии и быстром устранении денатурирующих факторов возможна ренатурация белка с полным или частичным восстановлением исходной структуры и биологических свойств.
Сложность строения белковых молекул, чрезвычайное разнообразие выполняемых ими функций затрудняют создание единой и четкой их классификации, хотя попытки сделать это предпринимались неоднократно, начиная с конца 19 века. Исходя из химического состава белки делят на простые и сложные (иногда их называют протеидами). Молекулы первых состоят только из аминокислот. В составе же сложных белков помимо собственно полипептидной цепи имеются небелковые компоненты, представленные углеводами (гликопротеиды), липидами (липопротеиды), нуклеиновыми кислоты (нуклеопротеиды), ионами металла (металлопротеиды), фосфатной группой (фосфопротеиды), пигментами (хромопротеиды) и т. д.
В зависимости от выполняемых функций различают несколько классов белков. Самый многообразный и наиболее специализированный класс составляют белки с каталитической функцией — ферменты, обладающие способностью ускорять химические реакции, протекающие в живых организмах. В этом качестве белки участвуют во всех процессах синтеза и распада различных соединении в ходе обмена веществ, в биосинтезе белков и нуклеиновых кислот, регуляции развития и дифференцировки клеток. Транспортные белки обладают способностью избирательно связывать жирные кислоты, гормоны и другие органические и неорганические соединения и ионы, а затем переносить их с током крови и лимфы в нужное место (например, гемоглобин участвует в переносе кислорода от легких ко всем клеткам организма). Транспортные белки осуществляют также активный транспорт через биологические мембраны ионов, липидов, сахаров и аминокислот.
Структурные белки выполняют опорную или защитную функцию; они участвуют в формировании клеточного скелета. Наиболее распространены среди них коллаген соединительной ткани, кератин волос, ногтей и перьев, эластин клеток сосудов и многие другие. В комплексе с липидами они являются структурной основой клеточных и внутриклеточных мембран.
Ряд белков выполняет защитную функцию. Например, иммуноглобулины (антитела) позвоночных, обладая способностью связывать чужеродные патогенные микроорганизмы и вещества, нейтрализуют их болезнетворное воздействие на организм, препятствует размножению раковых клеток. Фибриноген и тромбин участвуют в процессе свертывания крови. Многие вещества белковой природы, выделяемые бактериями, а также компоненты ядов змей и некоторых беспозвоночных относятся к числу токсинов.
Некоторые белки (регуляторные) участвуют в регуляции физиологической активности организма в целом, отдельных органов, клеток или процессов. Они контролируют транскрипцию генов и синтез белка; к их числу относятся пептидно-белковые гормоны, секретируемые эндокринными железами. Запасные белки семян обеспечивают питательными веществами начальные этапы развития зародыша. К ним относят также казеин молока, альбумин яичного белка (овальбумин) и многие другие. Благодаря белкам мышечные клетки приобретают способность сокращаться и в конечном итоге обеспечивать движения организма. Примером таких сократительных белков могут служить актин и миозин скелетных мышц, а также тубулин, являющиеся компонентом ресничек и жгутиков одноклеточных организмов; они же обеспечивают расхождение хромосом при делении клеток.
Белки-рецепторы являются мишенью действия гормонов и других биологически активных соединений. С их помощью клеткой воспринимается информация о состоянии внешней среды. Они играют важную роль в передаче нервного возбуждения и в ориентированном движении клетки (хемотаксисе). Преобразование и утилизация энергии, поступающей в организм с пищей, а также энергии солнечного излучения тоже происходит при участии белков биоэнергетической системы (например, зрительного пигмента родопсина, цитохромов дыхательной цепи). Существует также множество белков с другими, порой довольно необычными функциями (например, в плазме крови некоторых антарктических рыб содержатся белки, обладающие свойствами антифриза).
Вся информация о структуре того или иного белка «хранится» в соответствующих генах в виде последовательности нуклеотидов и реализуется в процессе матричного синтеза. Сначала информация с помощью фермента ДНК-зависимой РНК-полимеразы передается (считывается) с молекулы ДНК на матричную РНК (мРНК), а затем в рибосоме на мРНК, как на матрице в соответствии с генетическим кодом при участии транспортных РНК, доставляющих аминокислоты, происходит формирование полипептидной цепи.
Выходящие из рибоcoмы синтезированные полипептидные цепи, самопроизвольно сворачиваясь, принимают свойственную данному белку конформацию и могут подвергаться посттрансляционной модификации. Модификациям могут подвергаться боковые цепи отдельных аминокислот (гидроксилированию, фосфорилированию и т. д.). Именно поэтому в коллагене, например, встречается гидроксипролин и гидроксилизин (см. Аминокислоты). Модификация может сопровождаться и разрывом полипептидных связей. Таким путем, например, происходит образование активной молекулы инсулина, состоящего из двух цепей, соединенных дисульфидными связями.
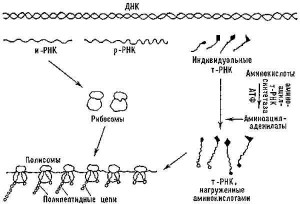
Рис. 6. Общая схема биосинтеза белков.
Белки являются важнейшими компонентами пищи животных и человека. Пищевая ценность белков определяется содержанием в них незаменимых аминокислот, которые в самом организме не образуются. В этом отношении растительные белки менее ценны, чем животные: они беднее лизином, метионином и триптофаном, труднее перевариваются в желудочно-кишечном тракте. Отсутствие незаменимых аминокислот в пище приводит к тяжелым нарушениям азотистого обмена.
В процессе пищеварения белки расщепляются до свободных аминокислот, которые после всасывания в кишечнике поступают в кровь и разносятся ко всем клеткам. Часть из них распадается до простых соединений с выделением энергии, используемой на разные нужды клеткой, а часть идет на синтез новых белков, свойственных данному организму. (Р. А. Матвеева, Энциклопедия Кирилл и Мефодий)
- амилоидный — amyloid;
- анионный — anionic [cathodic];
- антивирусный — antiviral;
- аутоиммунный — autoimmune;
- аутологичный — autologic;
- бактериальный — bacterial;
- белок Бенс-Джонса — Bence Jones protein;
- вирусиндуцируемый — virus induced;
- вирусный — virus;
- вирусный неструктурный — virus nonstructural;
- вирусный структурный — virus structural;
- вирусоспецифический — virus specific;
- высокомолекулярный — high molecular weight;
- гемсодержащий — heme;
- гетерологичный — foreign [heterologous];
- гибридный — hybrid;
- гликозилированный — glycated;
- глобулярный — globular;
- денатурированный — denaturated;
- железосодержащий — iron;
- желточный — yolk;
- животный белок — animal protein;
- защитный — defensive [protective];
- иммунный — immune;
- иммуногенный — immunologically relevant;
- кальцийсвязывающий — calcium binding;
- кислый — acidic;
- корпускулярный — corpuscular;
- мембранный — membrane;
- миеломный — myeloma;
- микросомный — microsomal;
- белок молока — milk protein;
- моноклональный — monoclonal immunoglobulin;
- мышечный белок — muscle protein;
- нативный — native;
- негистоновый — nonhistone;
- неполноценный — partial [incomplete];
- нерастворимый — insoluble;
- неусвояемый — insoluble;
- неферментный — nonenzyme;
- низкомолекулярный — low molecular weight;
- новый белок — new protein;
- общий — whole [crude];
- онкогенный — oncoprotein;
- белок основной фазы — anionic [cathodic];
- белок острой фазы (воспаления) — protein of acute phase;
- пищевой — food;
- белок плазмы крови — plasma protein;
- плацентарный — placenta;
- разобщающий — uncoupling;
- белок регенерирующего нерва — protein of regenerating nerve;
- регуляторный — regulatory;
- рекомбинационный — recombinant;
- рецепторный — receptor;
- рибосомный — ribosomal;
- связывающий — binding;
- секреторный белок — secretory protein;
- С-реактивный — C-reactive;
- белок сыворотки молока — whey protein, lactoprotein;
- тканевый — tissue;
- токсический — toxic;
- химерный — chimeric;
- цельный — whole;
- цитозольный — cytosolic;
- щелочной белок — anionic [cathodic] protein;
- экзогенный — exogenous [external];
- эндогенный — endogenous [internal] protein.
Более подробно о белках читайте в литературе:
- Волькенштейн М. В., Молекулы и жизнь[en] , М., 1965, гл. 3 — 5;
- Гауровиц Ф., Химия и функции белков, пер. с англ., [2 изд.], Москва, 1965;
- Сисакян Н. М. и Гладилин К. Л., Биохимические аспекты синтеза белка, в кн.: Успехи биологической химии, т. 7, М., 1965, с. 3;
- Степанов В. М. Молекулярная биология. Структура и функция белков. М., 1996;
- Шамин А. Н., Развитие химии белка, М., 1966;
- Белки и пептиды. М., 1995-2000. Т. 1-3;
- Биосинтез белка и нуклеиновых кислот, под ред. А. С. Спирина, М., 1965;
- Введение в молекулярную биологию, пер. с англ., М., 1967
- Молекулы и клетки. [Сб. ст.], пер. с англ., М., 1966, с. 7 — 27, 94 — 106;
- Основы биохимии: Перевод с английского М., 1981. Т. 1;
- Проблема белка. М., 1995. Т. 1-5;
- The Proteins. New York, 1975-79. 3 ed. V. 1-4.
источник
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 |
Санкт-Петербургский государственный технический университет
Методы определения вторичной структуры белков
Инфракрасная спектроскопия и спектроскопия кругового дихроизма.
1. Спектры кругового дихроизма белков
1.1 Явление кругового дихроизма
1.2 Методы анализа спектров кругового дихроизма белков
1.3 Работа с пакетом программ STRUCTURE по анализу спектров КД белков
2. Инфракрасные спектры поглощения белков
2.1 Поглощение белков в ИК-области
2.2 Методы анализа ИК-спектров белков
2.3 Работа с пакетом программ STRUC по анализу ИК-спектров белков
Хромофоры белковых молекул (то есть химические группы в молекуле белка, ответственные за поглощение света на определенных длинах волн) можно разделить на три класса: пептидные группы, боковые группы аминокислотных остатков и простетические группы. Спектроскопические методы исследования вторичной структуры белка основаны на изучении спектров именно пептидных хромофоров, поскольку конформация пептидных групп и определяет тот или иной тип вторичной структуры белка — a-спираль, b-структуру и др. Изучение поглощения света пептидными группами белка обычно проводится в ультрафиолетовом и в инфракрасном диапазонах. Как показывают эксперименты, простая адсорбционная спектроскопия белков в неполяризованном ультрафиолетовом свете мало пригодна для анализа вторичной структуры белка. Более ценную информацию можно извлечь из спектров кругового дихроизма белка. Инфракрасные спектры поглощения белка также пригодны для анализа его вторичной структуры [1]. Ниже будет рассмотрено применение методов измерения кругового дихроизма и инфракрасной спектроскопии для анализа вторичной структуры белка.
Белки, как практически все биологические молекулы, вследствие своей пространственной асимметрии обладают оптической активностью. При прохождении через оптически активную среду плоскополяризованный свет становится эллиптически поляризованным. Эллиптичность света q является одной из мер оптической активности. Она определяется как арктангенс отношения малой и большой осей эллипса. Другим параметром, характеризующим оптическую активность, является отклонение большой оси эллипса от направления поляризации падающего света, называемое оптическим вращением (или дисперсией оптического вращения) j.
Если представить плоскополяризованную волну Е в виде суммы двух волн противоположной круговой поляризации Е=ЕL+ЕR, то можно показать, что величина j пропорциональна разности показателей преломления среды для этих волн nL-nR, а величина q — разности коэффициентов экстинции eL-eR. Таким образом, оптическое вращение и появление эллиптической поляризации у плоскополяризованного света при прохождении его через оптически активную среду можно объяснить различным замедлением (nL¹nR) и поглощением (eL¹eR) двух его составляющих ЕL и ЕR, поляризованных по кругу. Разность Dn=nL-nR называют круговым двулучепреломлением, а разность De=eL-eR — круговым дихроизмом. Зависимости этих величин от длины волны называют спектрами дисперсии оптического вращения (ДОВ) и кругового дихроизма (КД).
На самом деле, ДОВ и КД являются проявлениями одного и того же физического явления, а их спектры можно выводить один из другого. Поэтому на практике достаточно измерять лишь один из этих двух спектров. Спектры КД более удобны для использования на практике, поскольку содержат узкие, хорошо разрешимые полосы. Этим объясняется то, что в настоящее время метод измерения КД используется гораздо более широко, чем ДОВ, несмотря на то, что он требует гораздо более сложного экспериментального оборудования.
КД легко измерить путем попеременного пропускания через образец лево — и правополяризованного по кругу света и регистрации соответствующей разницы поглощений, поскольку эллиптичность выходящего из оптически активного образца света обычно очень мала, и ее точное измерение весьма затруднительно. Однако, разность поглощений обычно пересчитывают в значения эллиптичности. Для того, чтобы можно было сравнивать результаты, полученные при исследовании разных образцов, пользуются значениями так называемой молярной эллиптичности:
где С — молярная концентрация, а l — длина оптического пути.
В случае белков главной целью измерения спектров КД является определение содержания в них вторичных структур разных типов. Если доля ароматических аминокислот в белке не очень велика, его оптическая активность в области от 180 до 240 нм определяется главным образом полипептидным остовом. Многочисленные эксперименты показали, что алифатические боковые группы аминокислотных остатков белка также не дают заметного вклада в спектр КД в этой области. Следовательно, в первом приближении белковую молекулу можно рассматривать просто как комбинацию участков полипептидным остова, находящихся в конформациях a-спирали, b-структуры и беспорядочного клубка.
Поглощение света пептидной группой
в ультрафиолетовом диапазоне определяется электронными переходами в ее электронных оболочках. В этом процессе основное участие принимают три молекулярных орбитали пептидной группы: n-орбиталь — несвязывающая орбиталь, на которой располагается неподеленная пара 2py-электронов атома кислорода, p-орбиталь — связывающая орбиталь, на которой располагаются 2pz-электрон атома кислорода и 2pz-электрон атома углерода, в значительной степени делокализованные по атомам кислорода, углерода и азота, и p*-орбиталь — разрыхляющая орбиталь, на которой в основном состоянии электроны отсутствуют. Два электронных перехода с наименьшей энергией наблюдаются при возбуждении электрона с n-орбитали на p*-орбиталь (n®p* переход) и с p-орбитали на p*-орбиталь (p®p* переход). n®p* переходу в пептидах соответствует слабая полоса поглощения 210-220 нм, а p®p* переходу гораздо более сильная полоса с максимумом вблизи 190 нм (характерная для a-спиральной конформации).
КД различных типов вторичной структуры белка можно оценить по результатам измерения КД гомополипептидов известной конформации (например, поли-L-лизина), после чего определить вклад каждой из структур в спектр КД исследуемого белка. Однако, такой подход имеет ряд больших недостатков. Во-первых, участки упорядоченной вторичной структуры модельных гомополипептидов имеют значительно большую длину, чем длина типичных участков в глобулярных белках. Во-вторых, их конформация может сильно отличаться от конформации, наблюдаемой у элементов вторичной структуры реальных белков. Кроме этого, среди гомополипептидов нельзя найти «стандартов» для b-изгибов. И, наконец, хотя вклад в КД от взаимодействий между хромофорами уменьшается как квадрат расстояния между ними, должен существовать определенный вклад от взаимодействия между участками с различной вторичной структурой. Эти взаимодействия нельзя адекватно смоделировать, рассматривая протяженные гомополимеры. Поэтому на практике спектры КД гомополипептидов не используются. Вместо этого в качестве базисных берут спектры КД белков, структура которых известна из данных рентгеноструктурного анализа. Различные подходы к анализу исследуемого спектра КД на основе этого базисного набора определяют различия между методами, которые будут описаны ниже.
Метод «эталонных спектров» [2,3]. Методы предсказания вторичной структуры белков по их спектрам КД основаны на предположении о том, что спектры КД различных структурных форм, составляющих белковую молекулу, дают аддитивный вклад в спектр КД белка в целом. Это можно записать в следующем виде:

где 




Эталонные спектры 

Принимая в рассмотрение в качестве структурных классов a-спираль (H), b-структуру (b), b-изгиб (t) и “неупорядоченную” форму (R), можем написать:
(«2») 
Суммируя экспериментальные данные, вместо 


где 




где 





Здесь 
Параметры 






-3.73×10
-3.72×10
+10.1×10
(«3») Эти параметры для глобулярных белков с достаточно большой точностью можно считать постоянными. Попытки оценить 

источник