Его вызывает вирус, проникающий в организм при контакте крови с инфицированным биологическим материалом, в том числе, остающимся на маникюрных принадлежностях, медицинских инструментах, машинках для нанесения татуировок, которые не были нужным образом продезинфицированы. Вирус может передаваться и при половом контакте.
Для диагностики болезни проводится анализ на гепатит В путем забора крови пациента.
Заражение происходит половым и бытовым путем, тип распространения — гематогенный (через кровь). При инфицировании вирус проникает в гепатоциты (клетки печени), в которых продуцируется в дальнейшем. Посредством кровотока болезнь стремительно распространяется по организму. Вирус В (HBV) характеризуется высокой устойчивостью к воздействиям температуры и кислоты, способен сохранять поражающие свойства в течение полугода.
Если гепатит В проявил первые симптомы, прежде чем начать терапию и лечение, необходимо сдать анализы. Исследование крови является достоверным способом установки заражения гепатитом. Проводится в лабораторных условиях. Материал для анализа на гепатит В сдается натощак: с последнего приема пищи должно пройти минимум 8 часов.
Для выявления в крови вируса гепатита В применяются анализы трех типов, характеризующих присутствие вируса в крови:
- анализ на наличие в материале ДНК HBV путем исследования полимеразной цепной реакции;
- качественное исследование присутствия белка Anti-HBc IgG и антигена HBsAg (встречаются у здоровых, инфицированных и переболевших);
- анализ на выявления белков HBeAg и Anti-HBc IgM (характеризуют обострение болезни).
Для полноты картины рекомендуется одновременно провести исследования по нескольким маркерам.
Наиболее распространенными анализами на гепатит В является иммунологические. Их суть — выявить в крови антитела, выработанные организмом или печенью. Пробы носят качественный и количественный характер. Анализы на гепатит В и их расшифровка, как правило, содержат информацию о нескольких характерных белках. При проведении пробы исследуются следующие антитела:

Положительный маркер говорит о присутствии вируса, но встречается и у абсолютно здоровых людей. Если в крови присутствует менее 0,05 МЕ/мл, то результат считается отрицательным. Если значение концентрации антитела выше, анализ признается положительным.
Обнаруживается практически у каждого инфицированного пациента. Сохранения показателей на высоком уровне может говорить о переходе болезни в хроническую форму течения. Положительный маркер говорит о нахождении болезни в периоде обострения, затяжном выздоровлении. HBeAg является крайне плохим признаком. Больной очень заразен. В норме — белок в крови не обнаруживается.
Существует два типа антител Anti-НВс: IgG и IgM. Присутствие в крови IgM является признаком течения острой формы, высокой заразности больного и возможности перерохода заболевания в хроническую форму. В норме присутствие IgM не допускается. IgG — благоприятный показатель. Маркер указывает на сформировавший иммунитет организма против гепатита В.
При выявлении в крови маркера можно делать вывод о благоприятном течении заболевания и формировании защитного иммунитета у больного.
Маркер сигнализирует о выздоровлении и формировании иммунитета.

Итоговая расшифровка показывает, имеются ли следы генного присутствия возбудителя в клетках печени.
Если при проведении исследования соблюдаются все принципы, то результат обладает абсолютной точностью. Метод используется для постановки диагноза, применяется в процессе лечения и при противовирусной терапии.
- Качественное ПЦР по итогу имеет всего два значения: «обнаружено» и «не обнаружено». Процедура проводится каждому пациенту с подозрением на гепатит. При средней чувствительности теста на ПЦР в диапазоне от 10 до 500 МЕ/мл, при низких содержаниях ДНК вируса в крови, генный материал обнаружен не будет.
- Количественное ПЦР. В отличие от качественного, указывает не только на гепатит В. Количественный анализ указывает насколько норма здорового человека далека от показателей больного в числовом выражении. Метод позволяет оценить стадию заболевания и назначить лечение. Чувствительность теста ПЦР при количественном следовании выше, чем при качественном методе. В основе лежит подсчет выявленной ДНК, который выражается в копиях на миллилитр или МЕ/мл.
Кроме того, количественное ПЦР дает понимание воздействия лечения и корректности подобранной терапии. В зависимости от количества генного материала вируса может быть принято решение о сокращении срока лечения или, наоборот, о его продлении и усилении.
Метод биохимического анализа является обязательным для получения полной клинической картины течения заболевания. Этот диагностический метод дает понимание о работе внутренних органов (печени, почек, желчного пузыря, щитовидной железы и других). Расшифровка дает понимание о скорости обмена веществ в организме, возможных патологиях метаболизма. Развернутые показатели укажут на недостаток витаминов, макроэлементов и минералов, необходимых для здоровья и жизни человека.
Сдать анализ на гепатит можно в любом другом диагностическом центре (Инвитро, Гемотест и др). Биохимический анализ крови при выявлении гепатита В включает следующие компоненты.

Количество и концентрация в крови при вирусном заболевании постоянно меняется, поэтому исследования проводятся не реже, чем раз в квартал. АЛТ отражает не только активность вируса гепатита, но и степень вызванных им нарушений в печени. Уровень АЛТ возрастает при повышении количества токсических веществ печеночного происхождения и в присутствие вируса.
Белок является составляющей важнейших органов человека: печени, нервной ткани, ткани почек, скелета и мышц. Фермент участвует и в построении самой главной мышцы — сердца. Высокие показатели АСТ у больного с гепатитом В может сигнализировать о фиброзе печени. Аналогичная ситуация возникает при алкогольном, медикаментозном или любом другом токсическом поражении клеток печени.
Зашкаливающие показатели являются признаком разрушения печени на клеточном уровне. Необходимо учитывать при постановке диагноза соотношение АСТ и АЛТ (коэффициент де Ритиса). Одновременное повышение концентрации обоих ферментов — признак некроза печени.
Вещество образуется в селезенке и печени, как результат распада гемоглобина в их тканях. Этот компонент входит в состав желчи. Выделяют две фракции белка: прямой билирубин (связанный) и непрямой билирубин (свободный). При возрастании в крови связанного билирубина имеет смысл подозревать гепатит или другие поражения печени. Это непосредственно связано с цитолизом печеночных клеток.
Если возрастает количество непрямого билирубина, то, скорее всего, присутствует поражение паренхимотозной ткани либо синдром Жильбера. Высокий уровень билирубина по результатам анализа может стать следствием непроходимости желчных протоков. При уровне билирубина свыше 30 микромоль на литр у больного проявляется желтушный оттенок кожи, моча становится темной, а белки глаз изменяют свой цвет.
Синтез этого белка происходит в печени. Если его количество снижено, то это свидетельствует об уменьшении синтеза ферментов в органе вследствие возникновения тяжелых поражений печеночных клеток.
Если количество общего белка становится существенно ниже, чем принятая норма, то это говорит о замедлении функционирования печени.
Фермент, используемый при обнаружении механической желтухи и холециститов. Возрастание уровня ГГТ является сигналом токсического поражения печени. Может провоцироваться хронических алкоголизмом и бесконтрольным употреблением медикаментов. Белок особо чувствителен к токсинам и алкоголю, под их влиянием его активность растет стремительно. Сохранение высокой концентрации ГГТ в крови в течение длительного времени говорит о тяжелых поражениях печени.
Является продуктом белкового обмена, происходящего в печени. Резкое снижение уровня — сигнал замедления работы органа.
Снижение уровня белковых фракций является признаком патологии печени.
Диагностирование гепатита В представляет собой совокупное исследование показателей. Только их комплексный анализ позволяет сделать выводы об инфицировании пациента. Рассмотрим расшифровку анализа на гепатит В. Для сравнения приведена норма веществ в крови.
Таблица. Расшифровка анализа на гепатит В.
| Наименование вещества | В норме | При инфицировании |
|---|---|---|
| Исследования на анти-тела при гепатите В | ||
| HBsAg | Отрицательный маркер | Положительный маркер (иногда обнаруживается у здоровых людей) |
| HBeAg | Отрицательный маркер | Положительный маркер (характерен для хронического и острого состояния) |
| Anti-НВс IgG | Положительный (свидетельствует об формировании иммунитета к заболеванию) /отрицательный маркер | Отрицательный |
| Anti-НВс IgM | Отрицательный маркер | Положительный маркер (гепатит в стадии обострения или хронического течения, повышенная заразность) |
| Anti-НВе | Положительный (формирование иммунитета)/отрицательный маркер | Положительный (благоприятное течение)/отрицательный маркер |
| Anti-HBs | Положительный (формирование иммунитета)/отрицательный маркер | Положительный (благоприятное течение)/отрицательный маркер |
| Метод ПЦР | ||
| Качественное ПЦР | Отрицательный | Положительный |
| Качественное ПЦР | Отрицательный | «Не обнаружено» — генный материал вируса не присутствует или его количество слишком мало; Менее 3,6*10^2 МЕ/мл — низкая концентрация генного материала; 2*10^4 МЕ/мл — средняя концентрация. Лечение должно быть основано на результатах биопсии печеночных клеток; 2*10^4 МЕ/мл — обостренное течение заболевания (обязательно применение противовирусных препаратов); 4,8*10^7 МЕ/мл — избыточное количество ДНК вируса в крови, крайне негативный показатель, высокая степень поражения печени. |
| Биохимический анализ крови | ||
| АЛТ | 6-37 МЕ/л | 500-3000 МЕ/л. |
| АСТ | У мужчин до 40-41 МЕ/л У детей до 50 МЕ/л | Свыше указанных норм |
| Билирубин | Непрямого — не более 17 мкмоль/л Всего — не более 20,5 мкмоль/л | Свыше указанных норм |
| Альбумин | От 35 до 50 г/л | Ниже указанной нормы |
| Общий белок | У взрослых от 65 до 84 г/л | Свыше указанной нормы |
| ГГТ | У мужчин — 10-71 ед/л У женщин — 6-42 ед/л | Свыше указанной нормы |
Ложноположительным называют результат, который возникает в виде положительной реакции на присутствие возбудителя вируса в крови при его отсутствии. Такой результат возможен при прохождении обследования на гепатит В и формируется под влиянием различных факторов. Встречается подобная реакция при:
- беременности;
- развитии онкологических заболеваний;
- тяжелых инфекционных проявлениях;
- перенесенной вакцинации;
- сбоев в работе иммунной системы.
Ложноположительный анализ на гепатит В возможен при нарушениях в ходе забора крови или во время процедуры проведения ее исследования. Анализы на гепатит В в этом случае необходимо сдать повторно. Во избежание подобного рекомендуется проходить дополнительное обследование методом ПЦР, которое без обнаружения генов гепатита В, полностью исключает заболевание.
Дополнительная интересная информация о гепатите В – в следующем видео:
источник
Коварство вирусных заболеваний, таких как гепатиты, заключается в том, что заражение происходит вмиг, но больной долгое время может даже не догадываться о том, что он инфицирован. Точно диагностировать болезнь и подобрать необходимую терапию помогают вовремя сделанные анализы. Давайте поговорим о них более подробно.
Под гепатитом понимают воспалительное заболевание печени. Оно может иметь как острую, так и хроническую форму. Чаще всего встречаются болезни вирусного характера. На сегодняшний день известно семь основных разновидностей вирусов гепатитов – это группы A, B, C, D, E, F и G. Однако, независимо от типа вируса, на начальном этапе болезнь протекает схоже: неприятные ощущения в правом подреберье, температура, слабость, тошнота, ломота во всем теле, потемнение мочи, желтуха. Все эти симптомы являются поводом для сдачи анализа на гепатит.
Следует знать, что заболевание может передаваться разными способами: через зараженную воду и пищу, через кровь, слюну, половым путем, при использовании чужих средств гигиены, в том числе бритвы, полотенца, маникюрных ножниц. Поэтому если симптомы не проявляются (а инкубационный период может длиться до двух месяцев и даже более), но у вас имеются предположения, что вы можете быть заражены, то тест на гепатит нужно сделать как можно скорее.
Кроме того, регулярно сдавать подобные анализы необходимо медицинским работникам, сотрудникам служб безопасности, специалистам по маникюру и педикюру, стоматологам, словом – всем, чья повседневная работа связана с соприкосновением с биологическими материалами других людей. Также тест показан специалистам, чья профессиональная деятельность сопряжена с поездками в экзотические страны.
Вызывается РНК-вирусом семейства Picornaviridae. Вирус передается через бытовые предметы и продукты питания, поэтому заболевание также называют «болезнь грязных рук». Симптоматика типичная для любого вида гепатита: тошнота, температура, боль в суставах, слабость. Затем проявляется желтуха. Инкубационный период длится в среднем 15–30 дней. Различают острую (желтушную), подострую (безжелтушную) и субклиническую (бессимптомную) формы болезни.
Выявить гепатит А позволяет анализ Anti-HAV-IgG (антитела класса IgG к вирусу гепатита А). Также данный тест помогает определить наличие иммунитета к вирусу гепатита А после вакцинации, это исследование особенно необходимо во время эпидемий. При клинических признаках гепатита А, контактах с больным, холестазе (нарушение оттока желчи) назначают Anti-HAV-IgM (антитела класса IgM к вирусу гепатита А). При этих же показаниях делают тест на определение РНК-вируса в сыворотке крови методом полимеразной цепной реакции (ПЦР) в плазме крови.
Вызывается вирусом HBV из семейства гепаднавирусов. Возбудитель очень устойчив к высоким и низким температурам. Гепатит В представляет серьезную опасность: около 2 миллиардов людей в мире инфицированы этим вирусом, а более 350 миллионов – больны им.
Заболевание передается через колюще-режущие предметы, кровь, биологические жидкости, при половых контактах. Инкубационный период может длиться от 2 до 6 месяцев, если в этот период не выявить и не начать лечить заболевание, то оно из острой может перейти в хроническую стадию. Течение болезни проходит со всеми симптомами, характерными для гепатита. В отличии от гепатита А при гепатите В нарушение функций печени носит более выраженный характер. Чаще развиваются холестатический синдром, обострения, возможны затяжное течение, а также рецидивы болезни и развитие печеночной комы. Нарушение правил гигиены и незащищенные случайные половые контакты являются поводом для проведения теста.
Для выявления этого заболевания назначают количественный и качественный тесты на определение HBsAg (Hepatitis B surface antigen, HBs-антиген, поверхностный антиген вируса гепатита B, австралийский антиген). Интерпретация показаний количественного анализа такова: и = 0,05 МЕ/мл – положительно.
Вирусное заболевание(ранее назывался «гепатит ни А, ни В»), передающееся через зараженную кровь. Вирус гепатита С (ВГC) относится к флавивирусам. Он весьма устойчив во внешней среде. Три структурных белка вируса имеют сходные антигенные свойства и обусловливают выработку антител anti-HCV-core. Инкубационный период заболевания может длиться от двух недель до полугода. Болезнь очень распространена: в мире около 150 миллионов человек инфицированы вирусом гепатита С и подвергаются риску развития цирроза или рака печени. Ежегодно более 350 тысяч человек умирают от связанных с гепатитом С болезней печени.
Гепатит С коварен тем, что может скрываться под видами других болезней. Желтуха при данном виде гепатита проявляется редко, повышение температуры тоже наблюдается не всегда. Отмечались многочисленные случаи, когда единственными проявлениями болезни были хроническая усталость и психические расстройства. Известны также случаи, когда люди, являясь носителями и переносчиками вируса гепатита С, годами не испытывали никаких проявлений болезни.
Диагностировать заболевание можно с помощью качественного анализа Anti-HCV-total (антитела к антигенам вируса гепатита C). Количественное определение РНК-вируса делается методом ПЦР. Результат интерпретируется следующим образом:
- не обнаружено: РНК гепатита С не выявлена или значение ниже предела чувствительности метода (60 МЕ/мл);
- 108 МЕ/мл: результат положительный с концентрацией РНК гепатита С более 108 МЕ/мл.
В группу риска возникновения рака печени относят больных гепатитом В и С. До 80% случаев первичного рака печени во всем мире фиксируется у хронических носителей этих форм заболевания.
Развивается только при наличии вируса гепатита B. Способы заражения аналогичны гепатиту В. Инкубационный период может длиться от полутора месяцев до полугода. Заболевание часто сопровождается отеками и асцитом (брюшной водянкой).
Болезнь диагностируется с помощью анализа на определение РНК-вируса гепатита D в сыворотке крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме реального времени, а также анализом на антитела класса IgM (Hepatitis delta virus, IgM antibodies, anti-HDV IgM ). Положительный результат теста означает наличие острой инфекции. Отрицательный результат теста фиксирует ее отсутствие либо ранний инкубационный период заболевания или позднюю стадию. Тест показан пациентам, у которых выявлен гепатит В, а также колющимся наркоманам.
Вакцинация против гепатита В защищает от заражения гепатитом D.
Инфекция часто передается через продукты и воду. Вирус нередко обнаруживается у жителей жарких стран. Симптомы схожи с гепатитом А. В 70% случаев болезнь сопровождается болевым синдромом в правом подреберье. У больных расстраивается пищеварение, ухудшается общее самочувствие, затем начинается желтуха. При гепатите Е тяжелое течение болезни, приводящее к смерти, встречается чаще, чем при гепатитах А, В и С. Исследование рекомендуется делать после посещения стран, где распространен этот вирус (центральная Азия, Африка).
Заболевание выявляется при проведении теста Anti-HEV-IgG (антитела класса IgG к вирусу гепатита Е). Положительный результат означает наличие острой формы заболевания либо свидетельствует о недавно проведенной вакцинации. Отрицательный – об отсутствии гепатита Е или о выздоровлении.
Этот тип заболевания на данный момент мало изучен, а сведения, собранные о нем, противоречивы. Возбудителей болезни два, один можно обнаружить в крови, другой – в фекалиях человека, которому было сделано переливание зараженной крови. Клиническая картина – такая же, как и при заболевании другими типами гепатита. Лечение, которое было бы направлено непосредственно на сам вирус гепатита F, пока не разработано. Поэтому проводится симптоматическая терапия.
Помимо анализа крови, для выявления этой болезни исследуют мочу и кал.
Развивается только при наличие других вирусов этой болезни – В, С и D. Он встречается у 85% наркоманов, вводящих психотропные вещества непродезинфецированной иглой. Также возможно заражение при нанесении татуировок, прокалывании ушей, иглоукалывании. Передается заболевание и половым путем. Долгое время оно может протекать без выраженной симптоматики. Течение болезни во многом напоминает гепатит С. Исходами острой формы заболевания могут быть: выздоровление, формирование хронического гепатита или длительное носительство вируса. Сочетание с гепатитом С может привести к циррозу.
Выявить болезнь можно с помощью анализа на определение РНК (HGV-RNA) в сыворотке крови. Показанием для проведения теста являются зафиксированные ранее гепатиты С, В и D. Также тест необходимо пройти наркоманам и тем, кто с ними контактирует.
Для анализов на все виды гепатита берут кровь из вены. Забор крови производится утром натощак. Специальной подготовки процедура не требует, однако накануне следует воздержаться от физических и эмоциональных перегрузок, отказаться от курения и употребления алкоголя. Обычно результаты тестов бывают готовы через сутки после забора крови.
Анализы на выявление гепатитов могут быть качественными (они указывают на наличие или отсутствие вируса в крови) или количественными (устанавливают форму заболевания, помогают контролировать течение болезни и эффективность терапии). Интерпретировать анализ и ставить диагноз на основании теста может только врач-инфекционист. Однако давайте в общих чертах рассмотрим, какими бывают результаты тестов.
Подобный результат говорит о том, что вируса гепатита в крови не обнаружено – качественный анализ показал, что тестируемый здоров. Ошибки быть не может, так как антиген проявляется в крови уже во время инкубационного периода.
Говорить о хорошем результате количественного анализа можно в том случае, если количество антител в крови ниже пороговой величины.
В случае положительного результата через некоторое время (по усмотрению врача) проводится повторный анализ. Дело в том, что повышенное содержание антител может быть вызвано, например, тем, что пациент недавно перенес острую форму гепатита, и антитела в крови все еще присутствуют. В иных случаях положительный результат свидетельствует об инкубационном периоде, наличии острого или вирусного гепатита или подтверждает то, что пациент является носителем вируса.
Согласно российскому законодательству, информация о положительных результатах серологических исследований на маркёры парентеральных вирусных гепатитов передается в отделы учета и регистрации инфекционных заболеваний соответствующих центров Госсанэпиднадзора.
В случае если тест был проведен анонимно, его результаты не могут быть приняты для оказания медицинской помощи. При положительном результате теста следует обратиться к врачу-инфекционисту для назначения дальнейшего обследования и проведения необходимой терапии.
Гепатит не приговор, в большинстве случаев острая форма заболевания полностью излечивается, хронический гепатит, при соблюдении определенных правил, кардинально не меняет качества жизни. Главное – вовремя обнаружить вирус и начать борьбу с ним.
В частных клиниках Москвы можно сдать анализы на выявление и конкретизацию вируса гепатита. Так, качественный анализ на гепатит А стоит в среднем 700 рублей, столько же на гепатит В; а вот количественный тест на поверхностный антиген вируса гепатита B обойдется примерно в 1300 рублей. Определение вируса гепатита G – в 700 рублей. А вот более сложный анализ, количественное определение РНК вируса гепатита С методом ПЦР, стоит около 2900 рублей.
В настоящее время не существует затруднений в проведении диагностики гепатитов, тем более в центральных областях развитых стран. А вот чтобы избежать подобных болезней, не стоит пренебрегать правилами личной гигиены. Также следует помнить о том, что случайные сексуальные контакты могут стать причиной болезни. Лучшей защитой от возможных заболеваний станет вакцинация – против большинства вирусов гепатита она давно и успешно практикуется.
Исследование на гепатит можно пройти в государственных, ведомственных и частных клиниках. Преимущество последних заключается в том, что там не требуется направление лечащего врача, а результаты готовятся оперативнее. Рекомендуем обратить внимание на лаборатории «ИНВИТРО». Эта сеть медицинских клиник специализируется на диагностике и анализах, обладает собственными лабораториями. Она предлагает пройти исследование на наличие всех типов гепатитов по следующим ценам: Anti-HAV-IgG – 695 рублей; HBsAg, качественный тест – 365 рублей; HBsAg, количественный тест – 1290 рублей; Anti-HBs – 680 рублей; Anti-HCV-total – 525 рублей; количественное определение РНК вируса гепатита С методом ПЦР – 2850 рублей; HDV-RNA – 720 рублей; HGV-RNA – 720 рублей; Anti-HEV-IgM и Anti-HEV-IgG – по 799 рублей за каждый. Ответственность перед пациентами и высокий уровень профессионализма сотрудников – визитная карточка «ИНВИТРО».
источник
Вирусный гепатит С — тяжелое заболевание, которое протекает с поражением печени. У восьмидесяти процентов больных оно переходит в хроническую форму. Вирус размножается в клетках печени — гепатоцитах — и вызывает их гибель. Отмершая ткань замещается очагами соединительной ткани, развивается фиброз.
По мере развития фиброза печень оказывается неспособна выполнять свои функции, начинается цирроз печени, который опасен своими осложнениями: повышением давления в системе портальной вены, желудочно-кишечными кровотечениями, нарушением свертывания крови, изменениями психики из-за повреждения ядер головного мозга токсическими продуктами.
Причина заболевания — заражение вирусом из семейства Flaviviridae, который относится к типу РНК-вирусов. Это значит, что генетический материал, по которому синтезируются белки возбудителя, закодирован в молекуле рибонуклеиновой кислоты. Заражение происходит через кровь, половым путем, и от беременной женщины к плоду. К сожалению, между инфицированием и началом выработки антител может пройти достаточно большое количество времени — от двух недель до шести месяцев. Это не дает определить заражение методом иммуноферментного анализа и начать лечение на ранних стадиях.
ПЦР — метод молекулярного анализа, который позволяет обнаружить генетический материал возбудителя уже на первой неделе после инфицирования с помощью полимеразной цепной реакции. Исследование обладает высокой специфичностью, точностью, и позволяет не только определить наличие или отсутствие вируса, но и его концентрацию и генотип.
Для исследования берут кровь пациента, в которой потенциально может находиться РНК вируса. В кровь добавляют праймеры — искусственно синтезированные участки искомого гена малой длины, и РНК-полимеразу — специальный фермент, который многократно увеличивает количество генетического материала возбудителя. С помощью специального аппарата проводят несколько циклов нагревания и охлаждения. Затем материал анализируют и сопоставляют с известными генами вируса, на основе чего делают заключение о наличии или отсутствии заражения.
Различают три вида ПЦР-анализа:
- Качественный анализ ПЦР . Первая стадия исследования. Он позволяет выявить генетический материал вируса в крови.
Количественный анализ ПЦР . Позволяет определить вирусную нагрузку — концентрацию генетического материала возбудителя в одном миллилитре крови. Это исследование проводят перед началом терапии, а затем на первой, четвертой, двенадцатой и (если курс длительный) двадцать четвертой неделе лечения, чтобы оценить его эффективность.
ПЦР-исследование назначают в следующих случаях:
- контакт с больным человеком, при котором могло произойти заражение;
- положительный результат иммуноферментного анализа;
- признаки цирроза печени: изменение размеров печени, увеличение селезенки, появление на животе подкожного венозного сплетения;
- появление симптомов поражения печени: боли в правой части живота, пожелтение кожных покровов;
- повышение активности АЛТ и АСТ в биохимическом анализе крови;
- перед началом лечения для определения вирусной нагрузки;
- с целью контроля за эффективностью антивирусной терапии;
- после окончания лечения для контроля за рецидивами;
- при наличии диагностированного гепатита B, для исключения смешанного поражения печени.
Расшифровкой ПЦР-анализа и иммуноферментного анализа на гепатит С должен заниматься гепатолог или инфекционист. Анализировать результаты ПЦР необходимо в комплексе с данными биохимического анализа крови, биопсии и УЗИ. Только квалифицированный врач сможет проанализировать результаты исследований и, основываясь на них, назначить правильное лечение.
В анализируемом биологическом материале обнаружен генетический материал возбудителя. Инфицирование подтверждено.
Инфицирование отсутствует, либо количество РНК возбудителя ниже границы чувствительности.
Нормальный показатель для здоровых людей. Означает, что в исследуемом материале отсутствует РНК гепатита С, либо его концентрация ниже порога чувствительности исследования.
Концентрация РНК ниже диапазона количественного определения. Такие результаты интерпретируют очень осторожно, соотносят их с данными других исследований, часто проводят повторное исследование.
Уровень вирусной нагрузки при данной концентрации считается низким. Обычно снижение количества вируса означает, что терапия идет успешно.
Уровень вирусной нагрузки при данной концентрации считается высоким.
Количество РНК выше верхнего предела диапазона количественного определения. Делать выводы о степени вирусной нагрузки при таком результате нельзя. Обычно в таких случаях тест повторяют с разведением образца крови.
Обнаружена РНК определенного генотипа
В биоматериале обнаружен вирус гепатита С определенного генотипа и субтипа. Результат кодируется римскими цифрами и латинскими буквами, например — 1а, 2b. Всего существует семь генотипов и шестьдесят семь субтипов, однако в России встречаются только три первых типа.
Обнаружена РНК вируса гепатита С
В крови обнаружена РНК редкого для России генотипа, который нельзя отнести к первому, второму или третьему типу. Необходимы дополнительные исследования.
Данный результат говорит о том, что пациент здоров, или о том, что колчество РНК возбудителя слишком мала.
Возможна ситуация, когда ПЦР-анализ на гепатит С отрицательный, а иммуноферментный анализ распознает антитела против вируса. Это значит, что пациент переболел гепатитом С в острой форме и излечился самостоятельно. Примерно двадцать случаев инфицирования заканчиваются самопроизвольным излечением, если организм пациента оказывает достаточное сопротивление инфекции.
Несмотря на то, что ПЦР — высокоточный анализ, его результаты могут быть искажены в следующих ситуациях:
- кровь транспортировалась в лабораторию в ненадлежащих условиях, был нарушен температурный режим;
- образец биоматериала был загрязнен;
- в крови находились остаточные следы гепарина и других антикоагулянтов;
- в исследуемом веществе оказались ингибиторы — вещества, которые замедляют или останавливают полимеразную цепную реакцию.
- Диагностика на ранних стадиях . ПЦР обнаруживает генетический материал возбудителя заболевания. С помощью иммунофлюоресцентного анализа можно определить только иммуноглобулины — вещества, которые организм вырабатывает в ответ на инфекцию. В случае заражения гепатитом С промежуток между заражением и началом иммунного ответа может составлять несколько недель и месяцев, в это время ИФА будет неэффективна. ПЦР даст ответ уже на первой неделе после заражения.
Низкая вероятность ошибки . В исследуемом материале определяют участок генетического материала, который характерен только для одного вида возбудителей. Это позволяет исключить ложные результаты. При ИФА возможны ошибки, так как один и тот же вид антител может выделяться против разных вирусов — такие антитела называют перекрестными.
Для ПЦР-анализа на гепатит С собирают венозную кровь. Обычно из вены пациента за один раз берут две порции крови: первую отправляют на ПЦР, а вторую на ИФА. Это делают для того чтобы более точно оценить, насколько сильно пациент заражен вирусом, и как иммунитет борется с ним.
Обычно от пациента требуют соблюдения следующих правил:
- анализ крови сдают с утра;
- перерыв между последним приемом пищи и сдачей крови должен составлять восемь-десять часов;
- за два-три дня до анализа нужно отказаться от жареной и жирной пищи, и алкоголя;
- в течение двадцати четырех часов перед анализом пациент должен избегать физических нагрузок: не переносить тяжестей, не посещать спортзал или бассейн.
источник
Вирусный гепатит В успешно лечится, если его вовремя обнаружить и правильно определить количество антител и антигенов в крови больного. С помощью иммуноферментного анализа на гепатит можно обнаружить присутствие маркеров вируса, но не могут установить точно стадию процесса.
Для количественной оценки применяют ПЦР диагностику. С помощью теста возможно посчитать количество маркеров, спрогнозировать течение болезни и вероятность излечения при помощи противовирусных препаратов.
Главное преимущество исследования — возможность обнаружить даже минимальные концентрации вируса, идентифицировать возбудителя на видовой стадии.
Вирус гепатита В отличается большой контагиозностью и устойчивостью к внешним воздействиям. Он сохраняет активность в следах крови больного до нескольких недель. Поэтому каждый человек подвержен риску заражения даже при условии соблюдения профилактики.
Для диагностики заболевания назначают следующие исследования:
| Иммуноферментный анализ крови на наличие антител к ВГВ | Это быстрый и информативный тест. Его недостатком является то, что исследование только дает информацию о присутствии антител, но не уточняет их количество. |
| Биохимический анализ крови | При начавшихся изменениях в печени в крови больного будет повышен уровень билирубина, щелочной фосфатазы и снижен уровень печеночных ферментов. Но на начальной стадии показатели будут находиться в пределах нормы. |
| ПЦР (полимеразная цепная реакция) | С ее помощью восстанавливают ДНК вируса, подсчитывают количественные показатели антител, уточняют стадию заболевания. То есть разное количество антител может свидетельствовать об остром этапе или о постпрививочном иммунитете. |

Родоначальником метода ПЦР (полимеразной цепной реакции) считается ученый из Норвегии Х. Клеппе. Он первый стал проводить амплификацию (восстановление) ДНК при помощи короткой цепочки ДНК, то есть синтетического праймера (своеобразной копии).
Однако, ученому не удалось реализовать свою идею. Похожие исследования сделал американский химик К.Муллис, который в 1993 был удостоен Нобелевской премии за свое изобретение. С тех пор ПЦР используют для установления отцовства, диагностики генетических болезней, обнаружения вирусов.
Суть реакции в том, что при помощи ферментов копируется определенный участок ДНК. Скопировать можно только участок, который соответствует заданным параметрам и если он есть в представленном образце. Для запуска реакции применяют следующие компоненты:
- Матричная ДНК с участком, подлежащим копированию.
- Праймеры, схожие по строению участку ДНК.
- Полимераза, то есть фермент, запускающий реакцию. Она должна быть термостабильной, то есть выдерживать перепады температур.
- Раствор с определенными параметрами, обеспечивающий прохождение реакции.
Реакция проводится в несколько этапов:
| Денатурация (прогревание) | Сначала раствор нагревают, в результате чего цепочки ДНК расходятся. |
| Стадия отжига | Раствор остужают, праймеры связываются с одноцепочечной матрицей. |
| Этап элонгации | Полимераза создает дочернюю цепь ДНК, достраиваются все фрагменты цепочки. Цепочка может расти до пределов, которые задаются количеством реагентов, затем достигает состояния плато. |
Для обнаружения гепатита в применяют два типа реакции: количественную и качественную.

Количественный ПЦР предполагает одновременное создание копий фрагментов ДНК и определение количества молекул. Измерение проводится после каждого этапа, то есть в режиме реального времени. Это достигается при помощи флюоресцентных зондов, которые включаются в цепочку молекул и светятся в определенный период исследования.
Данный способ применяют для обнаружения фрагментов ДНК, которые являются маркерами вируса гепатита. С помощью количественного метода удается точно выделить генотип вируса. Другими словами, подсчитывают количество копий генома ВГВ на количество клеток больного.
Количественный анализ дает ответы на следующие вопросы:
- С какой интенсивностью прогрессирует болезнь.
- Насколько эффективно проводимое лечение.
- Развилась ли резистентность к назначенным препаратам.
Также количественное измерение необходимо для диагностики хронической стадии инфекции. Если количество ДНК ниже 100 шт/мл при нормальном уровне трансаминаза, то человек является носителем вируса.
При острой фазе количество антител значительно выше.При антивирусной терапии повышение количества антител свидетельствует о развившейся устойчивости к лекарствам, это является сигналом для корректировки лечения.

Качественный ПЦР позволяет только установить присутствие возбудителя в крови. Если они отсутствуют, то пациент не заражен, при попадании возбудителя в кровь результат будет положительным.
Однако, с помощью качественной реакции невозможно уточнить геном вируса, этап заболевания. Поэтому для диагностики ВГВ проводят как количественное, так и качественное измерение.
Для проведения анализа методом полимеразной реакции необходима венозная кровь. Это необходимо сделать утром на голодный желудок.
Пациенту следует правильно подготовиться к исследованию:
- За 10 часов отказаться от пищи, можно пить только чистую воду.
- Накануне прекратить прием алкоголя, за 4 часа не курить.
- Перед обследованием стоит избегать физических и эмоциональных стрессов.
- За 2 суток перестать употреблять лекарства, если это невозможно, то необходимо предупредить лаборанта. Некоторые препараты оказывают влияние на конечный результат.

Интерпретировать данные качественного измерения несложно. Он дает либо положительный, либо отрицательный ответ.
При количественной реакции оценить полученные показатели можно в зависимости от числа копий ДНК. Единицей измерения является копий/мл.
Расшифровываются данные следующим образом:
- Если количество ДНК ВГВ менее 90, то инфекция отсутствует. У пациента развился поствакцинальный иммунитет, либо он излечился от болезни.
- При числе копий 2х100 говорят о носительстве вируса.
- Количество 2х106 свидетельствует о хронической стадии болезни.
- При ДНК более 2х109 пациент болен острой стадией гепатита.
Преимущества метода диагностики с помощью полимеразных реакцийи заключаются в следующем:
- Прямое обнаружение возбудителей. В отличие от него, метод ИФА дает информацию о присутствии антител к вирусу.
- Специфичность. То есть копируется именно участок ДНК, который имеется в образце биоматериала.
- Повышенная чувствительность. Метод может обнаружить даже единичные фрагменты клеток.
- Диагностика болезней в острой и в скрытой стадии. То есть, можно диагностировать болезнь на этапе доклинических проявлений.
У метода есть недостатки, которые приводят к ложным результатам. Самый существенный недостаток — вероятность загрязнения материала. Основным источником загрязнения являются плохо обработанные пробирки, руки лаборанта, реактивы.
В кровь может попасть часть ДНК от предыдущей реакции. Поэтому к лабораториям предъявляются повышенные санитарные требования: раздельные помещения, пластиковые пробирки, обработка лабораторий ультрафиолетом и т. д.
Ложноотрицательные результаты могут быть следствием сниженной чувствительности реакции. Это происходит в следующих ситуациях:
- пациент принимает лекарственные препараты, например, антикоагулянты;
- человек перед анализом перенес физическое напряжение (занятия спортом, тяжелая работа);
- заражение произошло недавно.
Если у пациента есть высокая вероятность инфицирования, а результат исследования отрицательный, ему необходимо повторное обследование.
Метод полимеразной цепной реакции является основным и самым информативным для диагностики ВГВ. Он позволяет не просто установить носительство инфекции, но и уточнить этап заболевания, оценить результаты лечения.
Для более точного диагноза применяют качественное и количественное измерение. К недостаткам способа можно отнести вероятность загрязнения, снижение чувствительности и довольно высокую цену.
Для того, чтобы результаты были наиболее достоверными, следует правильно подготовиться к исследованию и проводить его в клинике с соответствующей лицензией и хорошей репутацией.
Смотрите видео о ПЦР:
источник
М.И.Михайлов, Институт эпидемиологии и микробиологии им. Н. Ф. Гамалеи РАМН, Москва
При постановке диагноза «гепатит С» необходимо учитывать следующие наиболее важные факторы:
При этом основными направлениями работ, выполняемых лабораторными сотрудниками, являются:
Основой лабораторной диагностики гепатита С служат знания о ВГС, его репликации, информация о динамике появления и исчезновения маркеров инфицирования, а также современные иммунохимические и молекулярно-биологические методы детекции антигенов, антител и нуклеиновых кислот.
ВИРУС ГЕПАТИТА С. ВГС впервые был идентифицирован в 1988 году, когда группа исследователей во главе с М. Houghton и Choo Q.L, применив новые молекулярнобиологические методы исследования, клонировала и секвинировала геном вируса [I]. Частица вируса гепатита С имеет сферическую форму со средним диаметром около 50 нм [2,3]. Попытки визуального обнаружения и изучения строения вируса гепатита С предпринимались с момента открытия вируса, однако до сих пор отсутствуют хорошо документированные результаты этих исследований, что, возможно, связано с трудностями накопления вирусных частиц в необходимых количествах.
ВГСединственный член рода Hepacivirus в семействе Flaviviridae, в которое входят такие вирусы, как вирус диареи быков и лихорадки свиней (род Pestivirus) и вирус желтой лихорадки, вирус дэнге и GB-вирусы: GBV-A, GBV-B и GBV-C/HGV (род Flavivi-rus). Схема строения вируса гепатита С может быть представлена следующим образом (схема № 1). Нуклеокапсид содержит РНК вируса гепатита С. Сверху нуклеокапсид покрыт липидной оболочкой с утопленными в ней оболочечными белками, кодированными РНК ВГС. Геном вируса представлен однонитевой линейной молекулой РНК положительной полярности, протяженностью около 9600 нуклеотидов. Организация генома ВГС подобна другим флавивирусам. В нем выделяют две зоны, кодирующие структурные и неструктурные (функциональные) белки. Гены, кодирующие структурные белки, расположены у 5′ области генома вируса, а неструктурные у 3′ области. Ген ВГС имеет одну открытую рамку считывания (ОРС), единый полипептид (приблизительно в 3000 аминокислот), который под действием вирусных и клеточных протеаз нарезается на структурные и неструктурные белки.
Рис. 1. Структурные элементы HCV
К структурным белкам относят белки, кодированные Core, El и Е2 зонами РНК ВГС. Выявлено три формы С-белка ВГС: полноразмерная (р21) с молекулярной массой — 21 kD, усеченная (р19) и форма (р16), обнаруженная в ядрышках инфицированных гепатоцитов. На своей поверхности С-белок несет различные высококонсервативные В-клеточные эпитопы, существование которых чрезвычайно важно для выявления антител к ВГС в процессе лабораторной диагностики гепатита С.
Зоны РНК ВГС — Е1 и Е2 кодируют белки с молекулярной массой 31 и 70 kD . Эти белки имеют несколько участков N-гликозилирования; в Е1 белке определено до 6 таких участков, а в Е2 — 11. В участке Е2 заключена информация о небольшом белке — р7, который в структуре вируса не обнаружен.
Обозначение регионов, расположенных ближе к 3′- концу РНК ВГС — как зон, несущих информацию о неструктурных белках вируса, указывает на то, что эти белки не являются структурными компонентами вирусной частицы. В неструктурной зоне РНК ВГС выделяют участки, обозначенные как: NS2, NS3, NS4A, NS4B, NS5A и NS5B. Большинство из белков, кодированных неструктурными зонами РНК ВГС, необходимы для репликации вируса.
Сравнительный анализ нуклеотидных последовательностей РНК изолятов ВГС, полученных в различных регионах мира и даже в процессе заболевания от одного и того же пациента, выявил основную особенность этого вируса — высокую гетерогенность РНК. Положение о значительной генетической вариабельности РНК ВГС легло в основу теорий, объясняющих: длительное (иногда пожизненное) носительство вируса, частое развитие хронического заболевания, трудности в терапии и создании эффективных вакцинных препаратов. Наиболее значительные отличия последовательностей РНК ВГС сосредоточены в N-концевой части региона Е2, которую обозначают — «гипервариабельный регион» (HVR) [4].
В настоящее время определено 6 основных генотипов и свыше 100 субтипов ВГС. Генотипы 1а, 1в, 2а, 2в, 2с и За составляют более 90% HCV-изолятов, полученных в Северной и Южной Америке, Европе, России, Китае, Японии и Австралии/Новой Зеландии [5]. Генотипы 4, 5а и 6 соответственно регистрируются в Центральной и Южной Африке, Юго-Восточной Азии. В России и странах СНГ зарегистрировано преобладание генотипа 16 (не менее 68,9%) [6,7]. Считается, что пациенты, инфицированные генотипом 1 (особенно 1в), отвечают хуже на лечение по сравнению с пациентами, инфицированными другими генотипами вируса.
У больного ВГС циркулирует как популяция частиц вируса, у которых геномы отличаются друг от друга на 1-2% (квазиспецифичности) в результате мутаций, накапливающихся во время инфекции и/или попавших в организм пациента при заражении. Эти мутантные формы могут способствовать более активной репликации или могут помогать вирусу уклоняться от иммунного ответа организма и потенциально влиять на исход острой инфекции, различия в течении заболевания и ответе на интерферонотерапию [8].
ОПРЕДЕЛЕНИЕ АНТИ-ВГС. После открытия вируса ВГС и определения его роли в развитии посттрансфузионного гепатита — «ни А, ни В» перед исследователями стояла задача разработать методы, способные выявлять лиц с ВГС и пригодные для диагностики острого и хронического гепатита С. Было установлено, что антигены ВГС циркулируют в чрезвычайно низких концентрациях, и очевидно, что методический уровень конца 80-х годов XX века, применяемый для детекции вирусных антигенов, был явно недостаточен.
В 1989 году группа исследователей фирмы «Chiron Corporation» под руководством Q-L.Choo осуществила клонирование РНК ВГС и получила иммунореактивные олигопептиды, вступающие в реакцию с антителами, циркулирующими в крови больных хроническим гепатитом «ни А, ни В». Эти олигопептиды стали основой диагностических препаратов для выявления антител к ВГС. Это определило быстрый прогресс в разработке и промышленном выпуске диагностических препаратов. Основным методом, применяемым для детекции анти-ВГС, стал твердофазный иммуноферментный анализ, как метод, отвечающий требованиям практического здравоохранения -т.е. обладающий высокой чувствительностью, специфичностью и простотой проведения.
Учитывая, что ВГС персистирует в крови больных острым и хроническим гепатитом С одновременно с анти-ВГС, внимание разработчиков диагностических препаратов концентрировалось на создании тест-систем для детекции антител, обеспечивающих максимально полное выявление носителей вируса и максимально ранние сроки диагностики острой инфекции. Многообразие антигенов и антигенных детерминант, кодированных структурной и неструктурной зоной РНК ВГС, определило направление в конструировании диагностических препаратов выбором и аранжировкой олигопептидов, применяемых для их создания. За время, прошедшее с момента открытия ВГС, созданы диагностические системы трех поколений ( таблица 1).
Таблица 1
Диагностические препараты для выявления анти-ВГС [9]
Применяемые пептиды,
зоны РНК ВГС, в которых
они кодированы
Время первого
выявления
анти-ВГС от
начала желтухи
С22-3 Core
С200 NS3 и NS4
СЗЗс NS3
С 100-3 NS4
С22-3 Core
С200 NS3 и NS4
СЗЗс NS3
Пептид NS5
Введение дополнительных пептидов, прежде всего с22-3 (Core), в диагностические препараты 2-го и 3-го поколения позволило решить главную задачу, то есть увеличить чувствительность, специфичность и, самое главное, выявляемость анти-ВГС . Благодаря диагностикумам 3-го поколения удается выявлять до 97% носителей ВГС. Вместе с тем, определенную дискуссию вызвало решение о введении в диагностикум пептида, кодированного NS5 регионом РНК ВГС. По мнению некоторых исследователей, присутствие этого пептида не имеет принципиального значения для улучшения качества диагностического препарата. [10,11]. Однако антитела к NS5 могут быть выявлены в более ранние сроки инфекции, что улучшает качество лабораторной диагностики острого гепатита С. [12].
В настоящее время во всем мире, в том числе и в России, применяются диагностические препараты 3-го поколения. Пептиды, применяемые в диагностических препаратах, получены при помощи рекомбинантной технологии (например, диагностикумы фирм: «Диагностические препараты», г. Нижний Новгород; «Вектор» г. Новосибирск; «Roche»; «Abbott» и др.), или синтетической (000 МЦ «Авиценна» г. Санкт-Петербург; «Organon» и др.). Диагностикумы, в которых одновременно использованы оба вида пептидов, получили обозначения, как препараты 4-го поколения. По своим характеристикам эти препараты не обладают значимыми различиями. Сравнительные испытания, регулярно проводимые МЗ России, продемонстрировали сопоставимую чувствительность диагностических препаратов отечественных и зарубежных производителей.
Установлено, что применение диагностикумов 3-го поколения для выявления анти-ВГС среди иммунокомпетентного населения (например, доноров крови) оценивается в 98,8-100%. В то же время среди иммунокомпрометированных лиц, например, таких как пациенты после трансплантации почки, костного мозга или лица, инфицированные ВИЧ, этот показатель значительно ниже — 50 — 95% [12]. S.George с соавт. [13] продемонстрировали, что у 8,4% больных ВИЧ-инфекцией регистрируются ложно-негативные результаты выявления анти-ВГС. Причем у таких пациентов в процессе наблюдения может регистрироваться серореверсионный эффект, т.е. регистрация позитивного результата после серонегативного анти-ВГС периода [14].
Одна из наиболее важных проблем при проведении исследований на наличие анти-ВГС — ложнопозитивные результаты. Их появление может быть связано с неспецифическим взаимодействием компонентов реакции, возможными перекрестными реакциями с другими вирусными антигенами и многими другими факторами. Уровень ложно-позитивных результатов при выявлении анти-ВГС с различными диагностическими препаратами может достигать 10-20% [15,16]. Повышенный уровень таких результатов отмечен среди больных онкологическими и аутоиммунными заболеваниями, лиц с иммунодефицитными состояниями и больных сифилисом [16,17]. Существование ложнопозитивных результатов ставит перед лабораторным работником задачу их разграничения с истинным выявлением анти-ВГС. Для решения этой задачи служит обнаружение в образце сыворотки крови РНК ВГС. Однако отрицательный результат обнаружения РНК ВГС не позволяет говорить о наличии ложнопозитивного выявления анти-ВГС. Необходимо учитывать, что анти-ВГС могут изолированно циркулировать в крови пациента, который выздоровел после острого гепатита С (10-15%) или у которого произошла элиминация РНК ВГС в результате проводимой терапии.
КОНФИРМАЦИОННЫЕ (SUPPLEMENTAL) ТЕСТЫ. Для разграничения ложнопозитивных образцов и образцов, действительно содержащих антитела к ВГС, разработаны дополнительные (Supplemental) тесты. Наиболее часто в этих тестах используется принцип иммуноблота [например — тест RIBA («Ortho-Clinical Diagnostics»); «LiaTek HCV» (Organon Teknika)], когда на нитроцеллюлозной мембране адсорбируются в виде отдельных полос антигены, кодированные различными зонами РНК ВГС. Анти-ВГС взаимодействуют с адсорбированными антигенами с помощью меченных ферментом антител против Ig G человека с последующей их детекцией при помощи субстратного комплекса. Помимо иммуноблота в качестве дополнительных тестов также используют диагностические препараты для выявления анти-ВГС против конкретных антигенов, кодированных различными зонами РНК ВГС [«Спектр 4» («Имбио», г. Нижний Новгород; РекомбиБест АНТИ-ВГС-СПЕКТР» — ЗАО «Вектор Бест», г. Новосибирск; ИФА- Анти-НСУ-Спектр, НПО «Диагностические системы», г. Нижний Новгород].
Разработка и внедрение этих тестов идет параллельно с внедрением скрининговых тестов для выявления анти-ВГС, повторяя принцип расширяющегося спектра использованных пептидов в каждом последующем поколении диагностических препаратов. Так, диагностикум RIBA-III отличается от предыдущего поколения добавлением пептида, кодированного зоной NS5. Принципы, позволяющие подтвердить позитивный результат выявления анти-ВГС, прежде всего включают: возможность (в некоторых случаях) получения более четких результатов ферментативной реакции при взаимодействии с отдельными пептидами, а также применение в диагностикуме расширенного спектра пептидов, которые не используются в скрининговых тестах. Только введение новых пептидов позволяет повысить диагностическую ценность подтверждающих тестов.
Трактовка полученных результатов, например в таком тесте, как RIBA-III, включает три возможных ответа : позитивный, негативный и неопределенный результат. Последний из них выдается в случае отсутствия четких показаний (согласно инструкции, прилагаемой к диагностическому набору), позволяющих определенно судить о наличии или отсутствии анти-ВГС в исследуемом образце. Соотношение спектра регистрируемых ответов при проведении подтверждающих тестов колеблется в зависимости от характеристик групп пациентов, у которых первично выявлены анти-ВГС [18]. По данным J.M. Pawlotsky с соавт. [19], в половине случаев результатов, трактуемых как «неопределенные», удается обнаружить РНК ВГС. На наш взгляд, правомочность ответа — «неопределенный результат выявления анти-ВГС», выдаваемого лабораторным работником клиницисту, очевидна не только при проведении подтверждающего теста, но и рутинном исследовании на наличие анти-ВГС. Необходимость такой трактовки полученных результатов является отражением современного состояния лабораторной диагностики гепатита С.
ОПРЕДЕЛЕНИЕ IgM АНТИ- ВГС. В настоящее время созданы и промышленно выпускаются диагностические наборы для выявления IgM анти-ВГС фирмами: «Вектор Бест»; «Диагностические системы»; «Имбио», «Abbott» и др. На этапе конструирования диагностических наборов были созданы наборы для ИФА, основой которых являлись пептиды, кодированные различными регионами РНК ВГС [20] . Выбор был остановлен на пептиде, кодированном Core регионом РНК ВГС и выявлении антител к нему класса IgM. Так же как и при использовании тестов для выявления анти-ВГС (IgG), при исследовании IgM анти-ВГС могут быть зарегистрированы ложнопозитивные результаты. По данным Stevensona D.L. с соавт. [21], до 70% больных с хроническим гепатитам С с наличием IgM анти-ВГС одновременно имели повышенный уровень ревматоидного фактора, который способствует появлению ложнопозитивных результатов. Вместе с тем, по мнению Pawlotsky J.M., наличие ревматоидного фактора не влияет на качество выявления IgM анти-ВГС [22].
ОПРЕДЕЛЕНИЕ АНТИГЕНОВ ВГС. Возможность определения антигенов ВГС привлекала внимание исследователей сразу же после открытия вируса. Принципиальная возможность их тестирования была продемонстрирована К. Krawczynski с соавторами [23], которые иммуногистохимически обнаружили в печеночной ткани антигены ВГС, доказав специфичность иммунофлюоресцентного свечения. Применение поли- и моноклональных антител к различным антигенам ВГС установило наличие ВГС core Ag, антигенов, кодированных NS3 и NS4 зонами РНК ВГС, в ядре и цитоплазме гепатоцитов, у 60-90% больных хроническим ГС [24].Однако дальнейшие исследования продемонстрировали, что антигены ВГС удается обнаружить менее чем в 5% печеночных клеток.
Первые диагностические тест-системы («Ortho Antibody to Core Antigen (Murine Monoclonal) EL1SA Test System» и «Imucheck F-HCV Ag Core Kokusai») для выявления антигена ВГС появились на рынке иммунобиологических препаратов в 1999 году. В качестве цели детекции был избран Core антиген ВГС, который определяют при помощи твердофазного варианта ИФА, сконструированного на основе моноклональных антител. Первые исследования по применению этих тестов определили их высокую чувствительность, специфичность, и перспективность применения, прежде всего, в службе переливания крови [25,26]. Установлены:
МЕТОДЫ ОБНАРУЖЕНИЯ РНК ВГС. Современный этап лабораторной диагностики гепатита С можно охарактеризовать как этап начала широкого применения молекулярно — биологических методов выявления РНК ВГС. Подавляющее большинство методов выявления нуклеиновых кислот было апробировано для выявления РНК ВГС. Принципам конструирования диагностических препаратов и их применению для детекции вирусных ДНК или РНК посвящено значительное количество литературных обзоров, опубликованных как в отечественных [28], так и зарубежных изданиях [29]. Все эти методы можно разделить на две группы, в основе которых лежит применение принципов гибридизации без амплификации избранного участка нуклеиновой кислоты или с их амплификацией, что позволяет значительно повысить разрешающую способность метода.
Метод гибридизации основан на соединении меченных гибридизационных зондов (генноинженерные или синтетические молекулярные структуры, содержащие в себе нуклеотидные последовательности, комплементарные избранным участкам РНК). Учет результатов осуществляют по интенсивности сигнала, поступающего от метки в составе образовавшегося комплекса.
При гепатите С этот метод выявления РНК ВГС прежде всего нашел применение для ее идентификации непосредственно в гепатоцитах, в тестах обозначаемых — in situ hibidization [30]. Возможность непосредственной детекции РНК ВГС в ткани позволила обнаружить ее в мононуклеарных клетках крови, клетках слюнных желез и других тканях организма больного гепатитом С [31,32].
Метод гибридизации, применяемый для детекции РНК ВГС, позволяет продемонстрировать наличие негативных (репликативных) цепей РНК ВГС, что свидетельствует об активной репликации вируса [33].
Метод полимеразнной цепной реакции — в настоящее время наиболее широко применяемый методический прием, лежащий в основе практически всех молекулярно-биологических методов детекции РНК ВГС. Причем определение РНК ВГС возможно как в качественном, так и количественном варианте, что особенно важно для назначения, мониторинга и оценки эффективности применяемой терапии.
В качестве основных вариантов метода можно выделить:
Полимеразная цепная реакция — широко применяемый как в России, так и за рубежом метод детекции РНК ВГС. В его основе лежит многоцикловой процесс, напоминающий естественную репликацию нуклеиновой кислоты, причем каждый цикл состоит из последовательных этапов.
Из исследуемого материала (сыворотка или плазма крови, печеночный биоптат) выделяется РНК ВГС. Учитывая, что нуклеиновая кислота ВГС представлена РНК, а для амплификации необходима молекула кДНК, при помощи фермента — обратной транскриптазы, происходит образование однонитевых молекул кДНК ВГС. На следующем этапе к определенному участку каждой из цепей кДНК ВГС присоединяются т.н. праймеры — короткие олигонуклеотиды, комплементарные известным нуклеотидным последовательностям. Сравнение первичной структуры 5’UTR области генома различных изолятов ВГС выявило их незначительную изменчивость (между генотипами, гомология нуклеотидов — 92-98%, а внутри генотипа 98-99%). Это сделало предпочтительным выбор праймеров из этой зоны РНК ВГС и их применение в диагностических тест-системах, выпускаемых у нас в стране и за рубежом.
Далее, при помощи фермента ДНК- зависимой ДНК полимеразы происходит синтез новых участков ДНК. В настоящее время в качестве источника этого фермента чаще всего используют бактерии Thermophilus termus (Tth-полимераза) или Thermophilus aquaticus (Taq-полимераза). Обладая термостабильностью в присутствии ионов марганца и магния, этот фермент может быть одновременно использован для синтеза комплементарных одноцепочечных молекул кДНК ВГС и амплификации избранных участков кДНК. На завершающем этапе одного цикла реакции, при помощи ДНК полимеразы происходит синтез новых цепей комплементарных кДНК ВГС. Многократное повторение циклов реакции приводит к накоплению фрагментов кДНК ВГС, которые возможно зарегистрировать при помощи электрофореза в полиакриламидном геле с последующей визуальной детекцией или же с применением гибридизации с олигонуклеотидными зондами, что увеличивает чувствительность и специфичность применяемых диагностических препаратов. Применение праймеров, меченных ферментами, позволяет проводить учет результатов ПЦР при помощи иммуноферментного анализа.
Постоянная цель, стоящая перед исследователями, конструирующими диагностические системы для выявления РНК ВГС, — повышение чувствительности и специфичности. Этой цели служит вариант ПЦР, обозначенный — «гнездовой ПЦР» (nested PCR) [34]. Отличительной особенностью этого метода от «классического» является одновременное использование двух пар праймеров, одна из которых комплементарно связывается с внутренним участком ампликона, полученного после первого раунда амплификации. Вместе с тем считается, что при этом варианте ПЦР более высок риск контаминации образцов, что может привести к ложноположительным результатам [35] .
Острая потребность в определении РНК ВГС и сложности, связанные с крупномасштабным производством высокочувствительных и специфичных диагностических наборов для ПЦР диагностики, определили широкое применение препаратов, изготовленных в научных лабораториях. Сравнение этих тест-систем, так называемых — «домашних» тестов («in house tests»), продемонстрировало их высокую вариабельность по чувствительности и специфичности, а также отсутствие воспроизводимости результатов между лабораториями и сериями диагностических препаратов. Так, при проведении первого Европейского цикла «внешнего» контроля качества оценки выявления РНК ВГС (1996 г.) из 136 лабораторий только 22 (16%) смогли абсолютно правильно определить наличие или отсутствие вирусной РНК в предоставленных контрольных образцах [36]. Подобный результат отмечен и в нашей стране, во время проведения аналогичной работы в рамках Федеральной системы внешнего контроля качества (2001 г.), когда из 14 участвующих лабораторий лишь 3 (21,4%) смогли правильно решить поставленную задачу [37].
Причины появления ложнонегативных и ложнопозитивных результатов выявления РНК ВГС разнообразны. При ложноотрицательных результатах:
— потеря или разрушение РНК ВГС в ходе подготовки к реакции клинического материала;
— наличие в образце ингибиторов, влияющих на различные компоненты ПЦР. Эти ингибиторы представлены различными химическими или белковыми субстанциями. Например: наличие в спермальной жидкости ингибиторов обратной транскриптазы не позволяло обнаружить РНК ВГС и говорить о возможности реализации полового пути передачи гепатита С [38]; наличие гепаприна [39]; высокий уровень криоглобулинов в сыворотке крови [40];
— несоблюдение теплового режима хранения и транспортировки клинического материала. При ложнопозитивных результатах:
— контаминация между пробами (при обработке образцов и/или работе с реакционной смесью), в том числе и контаминацией позитивным контрольным образцом;
— контаминация продуктами предшествующий амплификации (ампликонами), которые могут загрязнять исследуемые образцы и растворы через аэрозоли или лабораторное оборудование.
Массовое внедрение ПЦР диагностики по определению РНК ВГС поставило перед органами практического здравоохранения задачи перехода на новый уровень проведения лабораторных исследований. Выделение изолированных зон для осуществления основных этапов ПЦР (для подготовки проб; проведения амплификации; для учета полученных результатов); отдельный комплект для каждого этапа реакции лабораторной одежды, автоматических пипеток; существование стандартных диагностических наборов и самое главное — наличие высококвалифицированных лабораторных сотрудников позволяет снизить уровень появления ложных результатов.
Первый стандартизированный набор для определения РНК ВГС («AmplicorTM HCV», «Roche Diagnostic Systems») изготовлен в 1993 году. За прошедшие годы наборы для выявления РНК ВГС прошли эволюцию, основной целью которой стало повышение их чувствительности и специфичности. При конструировании «Amplicor TM HCV» использовано несколько оригинальных методических приемов, позволяющих выявлять 100 и выше копий РНК ВГС в мл., а также бороться с возможными случаями контаминации образцов и растворов, применяемых в наборе. Использование фермента — амперазы и дезиксиуридинтрифосфата (dUTP) позволяет разрушать в первом цикле амплификации предшествующие апликоны, которыми могла произойти контаминация. Разрушение амперазы в конце первого цикла амплификации (при +55 С) не позволяет ферменту разрушать ампликоны, избранные в качестве мишени. Принципиальным новшеством стало введение внутреннего контроля. Смысл этого новшества заключается во введении в каждый исследуемый образец последовательности, подобной амплифицируемому участку РНК ВГС, которая в дальнейшем выявляется с помощью соответствующих праймеров в реакции амплификации в аналогичном режиме. Отсутствие позитивной реакции при выявлении внутреннего контроля свидетельствует о наличии ложнонегативного результата реакции на наличие РНК ВГС в исследуемом образце. Диагностикумом следующего поколения стал препарат, обозначенный — «HCV Amplicor 2,0», при использовании обладающий пределом чувствительностью 50 молекул РНК ВГС.
Систему выявления РНК ВГС при помощи наборов фирмы «Roche» нельзя рассматривать в отрыве от их приборного обеспечения, определяющего высокое качество тестирования. Разработчики метода стремились к полной автоматизации всех этапов реакции. Воплощением этой идеи стала система «COBASAmpliPrepTM», позволяющая полностью автоматизировать процесс выделения РНК ВГС, амплификации и детекции, тем самым уменьшить риск получения ложнопозитивных и ложнонегативных результатов, сохранив при этом высокую чувствительность и специфичность [41].
Лигазная цепная реакция выявления РНК BГC.(LCR). Метод основан на способности фермента «ДНК- зависимой ДНК-лигазы» сшивать (лигировать) разрывы фосфодиэфирной связи в ДНК в присутствии АТФ и ионов Mg 2+. Так же как и при проведении «классической» ПЦР для выявления РНК ВГС, первый этап LCR — обратная транскрипция с получением кДНК ВГС. Далее ДНК-лигаза осуществляет связывание двух пар праймеров (комплементарных 5′ некодированной зоне РНК ВГС), которые в дальнейшем амплифицируются. Детекция продуктов амплификации LCR осуществляется при помощи учета реакции антиген-антитело. Каждый из двух прайеров метится различным гаптеном. Первый из них захватывается антителами, адсорбированными на микрочастицах. После процедуры промывания при помощи второй пары антител, меченных флуоресцентной меткой, происходит их избирательное взаимодействие с гаптеном в амплификационном продукте с последующим проведением субстратной реакции и учетом на флюориметре.
Чувствительность этого метода составляет около 200 копий РНК ВГС в мл, что позволяет его использовать для решения различных клинико-диагностических задач [42]. В настоящее время диагностические наборы выявления РНК ВГС, основанные на LCR, изготовлены фирмой «Abbott».
Nucleic Acids Seaquencence Amplification — NASBA —метод детекции РНК ВГС основан на одновременном действии трех ферментов: обратной транскриптазы вируса миелобластомы птиц, РНК-азы Н и РНК-полимеразы Т7 [43.]. В отличие от RT PCR на первом этапе не проводится обратная транскрипция РНК ВГС. При помощи использованных ферментов удается получить более 10(9) копий участка кДНК ВГС в течение 90 минут [44]. Возможность проведения реакции при небольших температурах (+41 С) значительно упрощает работу и позволяет отказаться от оборудования, обеспечивающего циклические изменения высоких температур. Учет результатов реакции осуществляется при помощи электрохемилюминесценции. Несмотря на то, что по своей чувствительности NASBA близка к RT PCR, метод широко не используется для выявления РНК ВГС. В настоящее время проводится разработка варианта метода, сочетающего принципы проведения NASBA и «Real-time RT PCR».
Метод транскрипционно опосредованной амплификации (Transcription-mediated amplification — ТМА) отличается от ПЦР и LCR прежде всего тем, что непосредственно амплифицируются фрагменты РНК ВГС , а не кДНК ВГС. На начальном этапе реакции к РНК ВГС присоединяется праймер (№1) и с помощью фермента (обратной транскриптазы) синтезируется копия молекулы мишени — кДНК. Обратная транскриптаза, обладая также активностью РНКазы-Н, разрушает вирусную РНК в гибриде РНК-кДНК. Далее к молекуле кДНК присоединяется второй праймер с последующей достройкой двухцепочечной ДНК при помощи обратной транскриптазы. При помощи другого фермента -РНК-полимеразы происходит транскрипция РНК с кДНК, что приводит к образованию от 100 до 1000 копий ампликона РНК ВГС в одном цикле реакции. К этим РНК-апликонам присоединяется праймер № 2 с дальнейшим синтезом кДНК-копий и разрушением молекулы РНК. Присоединение праймера №1 на кДНК с последующей достройкой двухцепочечной ДНК запускает следующий цикл амплификации. Учет результатов реакции осуществляют на люменометре, так как образовавшиеся РНК-ампликоны специфически взаимодействуют с ДНК-зондами, меченными хемилюминафорами.
В качестве преимуществ ТМА-метода при выявление РНК ВГС отмечают:
Сравнительные исследования по детекции РНК ВГС при помощи ТМА и другими методами продемонстрировали высокий уровень совпадений результатов [45].
Сочетание принципов гибридизации и амплификации лежит в основе метода выявления РНК ВГС, обозначенного как «Метод гибридизации с использованием разветвленных зондов или Branched DNA assay (bDNA) [46]. В отличие от ПЦР в данном тесте осуществляется амплификация не молекул кДНК ВГС, а сигнала. Реакция проводится в 96 луночных планшетах, на которых адсорбированы фрагменты РНК ВГС из 5′ нетранслируемой зоны и core-гена РНК ВГС. За счет последующего связывания с синтетической молекулой разветвленной ДНК и гибридизацией с пробой, меченной щелочной фосфотазой с усилителем и последующей ферментативной реакцией достигается резкое увеличение полученного сигнала. В настоящее время на диагностическом рынке появились диагностикумы третьего поколения (Вауег 3.0 Hepati-tis С Virus RNA Quantitation by bRNА), обладающие чувствительностью, позволяющей выявлять 520 IU/ml (2500 копий РНК ВГС).
КОЛИЧЕСТВЕННОЕ ВЫЯВЛЕНИЕ РНК ВГС. Для оценки концентрации РНК ВГС применяют количественный вариант ПЦР. Первоначально концентрацию РНК ВГС пытались охарактеризовать порядковыми величинами, например»+»,»++» и т.д., визуально отражающими интенсивность полос, полученных при электрофорезе продуктов амплификации, или же методом конечных разведений, т.е по наличию позитивного результата в конечной точке титрования. Трудности стандартизации всех этапов ПЦР не позволяют объективно оценить концентрацию РНК ВГС, что приводит к существенным ошибкам трактовки полученных результатов.
В настоящее время результаты исследования выражают в количественных единицах: количество копий РНК ВГС, содержащихся в 1 мл., в абсолютном или логарифметическом выражении (log 10). Исходя из того, что концентрация обнаруженной РНК ВГС отражает количество вирусных частиц, данный показатель обозначают как «вирусный эквивалент (eq)», с добавлением приставки k (килограмм, тысяча) или М (миллион). Еще одним способом выражения количества вирусных частиц являются их весовые эквиваленты. Например, в граммах или пикограммах (1 pg соответствует приблизительно 1 миллиону eq). Разнообразие применяемых величин создает трудности трактовки результатов, полученных в различных лабораториях. Поэтому комитет экспертов ВОЗ по биологической стандартизации изготовил «международный стандартный образец», содержащий РНК ВГС (лиофильновысушенная сыворотка крови, содержащая РНК ВГС 1-го генотипа), концентрация которой выражена в международных единицах (IU/mL) [47]. Специальные коэффициенты позволяют пересчитывать полученные показатели концентрации в международные единицы.
Для определения концентрации РНК ВГС применяют практически все варианты ПЦР. При этом к диагностическим препаратам предъявляется ряд специфических требований, важнейшим из которых является строгая линейность результатов, т.е. увеличение сигнала регистрируемой реакции при увеличении концентрации РНК ВГС в исследуемом образце. Применение внутренних стандартов с различным содержанием РНК ВГС позволяет избежать многих методических ошибок, которые могут отразиться на конечном результате реакции [28]. Чувствительность применяемых диагностикумов (Amplicor HCV Monitor v2.0; LCx HCV RNA Quantitative Assay) позволяет выявлять РНК ВГС, начиная с 50 копий в мл [48,49], что особенно важно для прогнозирования эффективности избранной противовирусной терапии.
ПЦР в реальном времени («Real-time RT PCR») —один из наиболее перспективных вариантов количественного метода выявления РНК ВГС. Метод и его аппаратное обеспечение совместно разработаны специалистами фирм «Roche» и «Percin Elmer». Принцип метода заключается в способности гидролизовать последовательности кДНК в направлении 5′—- 3′. В реакции применяется специальный зонд, меченный двумя флюоресцентными красителями, имеющими близкие максимумы поглощения и флюоресценции. При наличии продуктов амплификации Tag-полимераза расщепляет зонд, что приводит к предотвращению переноса энергии от одной молекулы красителя к другой, и тем самым предотвращает выход кванта света. Специальный прибор осуществляет учет реакции и математическое моделирование кинетики флюоресценции на каждом этапе реакции, что позволяет получить информацию об исходной концентрации РНК ВГС.
Отличительной особенностью «ПЦР в реальном времени» считают возможность получать информацию о наличии РНК ВГС непосредственно в процессе реакции, что позволяет уменьшить время анализа в сочетании с высокой чувствительностью и линейностью получаемых результатов [50]. По данным Татьяны Яшиной с соавторами, данный метод позволяет выявлять от 200 копий РНК ВГС в мл. [51].
МЕТОДЫ ГЕНОТИПИРОВАНИЯ РНК ВГС. Определение принадлежности ВГС к определенному генотипу и субтипу нашло свое применение для решения не только чисто научных, но и практических вопросов. Например: поиск источника инфекции во время вспышек гепатита С или прогнозирование эффективности применяемой терапии.
«Золотой стандарт» генотипирования ВГС — непосредственное определение первичной структуры РНК ВГС с его последующим филогенетическим анализом [52], что позволяет четко охарактеризовать данный изолят вируса. Получить эту информацию возможно при использовании следующих вариантов секвенирования:
Несмотря на точность получаемого результата, метод непосредственного секвенирования не используется в практическом здравоохранении из-за технических сложностей проведения исследования и высокой стоимости работ. Вместе с тем наличие информации о первичной структуре РНК ВГС является референтным методом генотипирования, а наличие приборов для автоматического секвинирования упрощает получение результата.
В настоящее время в большинстве случаев для генотипирования РНК ВГС применяются методы, основанные на использовании ПЦР с типоспецифическими праймерами. Впервые генотипирование РНК ВГС проведено Н. Okamoto с соавторами в 1992 году при помощи RT-ПЦР [53], включающего два этапа амплификации. Первый из них проводился с универсальными, для всех генотипов ВГС, праймерами, второй со смесью типоспецифических праймеров с получением специфических продуктов амплификации различной длины. О наличии того или иного генотипа судили по размеру амплифицированного продукта. В качестве праймеров используются типоспецифические зонды, информация о которых расположена в 5’UTR, Core или NS5 — областях РНКВГС[54].
Гибридизация амплифицированных продуктов с адсорбированными геноспецифическими зондами (из 5′-нетранслируемой зоны РНК ВГС), адсорбированными на нитроцеллюлозной мембране, лежит в основе теста — обозначенного «INNO-LiPA HCV, INNO-GENETICS» [55]. Первоначально с помощью этого теста удавалось типировать генотипы: la; lb; 2a; 2b;3a; 3Ь; 4 и 5а. В дальнейшем тест-системы 2-го поколения «INNO-LiPA HCV II , INNOGENETICS» позволяют различать все 6 генотипов и дополнительно 2с; 2d; 2i; 3с; 4a-h; 6а и 10а. [56]
Методический арсенал определения генотипов ВГС не ограничивается вышеперечисленными способами и включает в себя разнообразные методы:
СЕРОТИПИРОВАНИЕ Анти-ВГС стало возможным благодаря исследованиям P.Simmonds с соавторами, установившим наличие антител, направленных к генотипспецифичным эпитопам, информация о которых кодирована NS4 зоной РНК ВГС [60]. При помощи диагностикума для ИФА, сконструированного на основе синтетических пептидов, удалось разграничить случаи гепатита С, вызванные вирусами 1, 2 и 3 генотипа (89% совпадения с результатами генотипирования). Разработка тестсистем с использованием синтетических и рекомбинантных антигенов, кодированных NS4 и Core зонами РНК ВГС, позволила расширить перечень типируемых вариантов вируса, а также судить о наличии подтипов (1а, lb, 2a, 2Ь, За, и 4а) [61,62]. В настоящее время осуществляется коммерческий выпуск диагностических препаратов для проведения серотипирования как в плашечном варианте проведения ИФА — «Мurех НС 1-6 Serotyping Assay, Murex Diagnostics», так и в варианте «иммуноблот» — RIBA HCV Serotyping Assay, Chiron Diagnostics. Сравнительные данные результатов серотипирования и генотипирования РНК ВГС продемонстрировали высокий уровень совпадения результатов, достигая 95% [62].
Серотипирование анти- ВГС по сравнению с генотипированием РНК ВГС обладает такими преимуществами, как простота проведения реакции и более низкая стоимость. Вместе с тем, этот метод ни в коем случае не может заменить генотипирование. Результаты серотипирования анти-ВГС свидетельствуют о типовой принадлежности анти-ВГС при текущей или ранее перенесенной инфекции. В некоторых случаях (наиболее часто у больных гемофилией) регистрируется одновременное выявление анти-ВГС различных подтипов, что может свидетельствовать о множественном инфицировании различными субтипами и генотипами ВГС [63]. Кроме того, у пациентов с гепатитом С на фоне выраженного иммунодефицитного состояния РНК могут быть единственным маркером, что делает невозможным проведение серотипирования.
ВЫЯВЛЕНИЕ и ТРАКТОВКА РЕЗУЛЬТАТОВ ТЕСТИРОВАНИЯ СЕРОЛОГИЧЕСКИХ МАРКЕРОВ ВГС-ИНФЕКЦИИ. Наличие широкого спектра серологических маркеров текущей или предшествующей ВГС инфекции, а также современная методологическая база позволяют решить многие задачи лабораторной диагностики и профилактики гепатита С. В таблице № 2 представлены серологические маркеры ВГС инфекции и наиболее важные направления их тестирования.
Таблица 2
Диагностическая значимость маркеров текущей или предшествующей ВГС инфекции
Подтвер-
ждение
результата
+ анти-ВГС
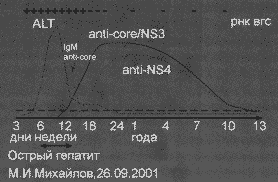
Одной из главных задач лабораторной диагностики гепатита С является постановка диагноза и разграничение острого от хронического гепатита С при помощи выявления серологических маркеров инфицирования. Так же как и при других острых вирусных гепатитах, серологические маркеры инфицирования ВГС последовательно появляются и исчезают по ходу инфекции и процесса выздоровления (Рисунок 2).
РНК ВГС удается обнаружить на 7 — 21-й день после инфицирования ВГС, а анти-ВГС на 20 — 150-й день (в среднем 50-й день) [64]. Спектр анти-ВГС может различаться в зависимости от периода острого гепатита. Считается, что первыми удается определить антитела, кодированные Core и NS5 зоной РНК ВГС. Анти-ВГС к белкам, кодированным NS4 зоной, в острую фазу гепатита С отсутствуют [65]. Сравнительное изучение уровня концентраций анти-ВГС, спектра анти-ВГС и РНК ВГС у больных острым и хроническим гепатитом продемонстрировало некоторые различия [66]. На наш взгляд, эти различия могут быть связаны с индивидуальными особенностями инфекционного процесса, что снижает их диагностическую ценность.
Рис. 2. Острый гепатит С
По аналогии с лабораторной диагностикой гепатита А и В ожидали, что определение антител к ВГС класса IgM будут иметь столь же большое диагностическое значение как IgM анти-ВГА и IgM анти-НВс. Однако данные тестирования сывороток крови больных острым и хроническим гепатитом С на наличие IgM анти-ВГС указывают на частое их выявление среди этих больных — 50-93% и 50-70% соответственно [67,68], эти результаты свидетельствуют, что обнаружение IgM анти-ВГС не может быть использовано как маркер острой ВГС инфекции.
Отсутствие маркера, претендующего на роль «золотого» стандарта острого гепатита С, определяет необходимость комплексной оценки полученных результатов, основанных на динамическом наблюдении за пациентом.
Не менее важное направление использования высокочувствительных методов тестирования РНК ВГС — снижение риска развития посттрансфузионного гепатита С. Необходимость таких работ определяется наличием фазы «окна», т.е. временем между первым обнаружением РНК ВГС и появлением анти-ВГС , а также существованием доноров крови (больных хроническим гепатитом С), у которых имеются РНК ВГС при отсутствии анти-ВГС. Современная система контроля донорской крови на наличие ВГС включает только тестирование анти-ВГС, риск заражения гепатитом С сохраняется. Исходя из этого правомерна постановка вопроса о тестировании крови на наличие РНК ВГС современными методами (методы NAT — «nucleic acid amplification test»). Фактор, ограничивающий эту работу, — высокая цена исследований. Для сокращения затрат рекомендуется тестирование пулов сывороток крови (от 8 до 96 образцов) с последующим поиском позитивного образца в случае выявления РНК ВГС в пуле сывороток. Учитывая фактор разведения искомой РНК ВГС при пулировании сывороток крови, принципиальным становится вопрос о применении наиболее чувствительных методов детекции. Считается, что использование диагностических наборов для NAT — с чувствительностью 50-100 IU/mL позволяет значительно уменьшить риск посттрансфузионного гепатита С.
Несомненно, перечень вопросов, которые можно решить при тестировании всего спектра маркеров ВГС-инфекции, не исчерпывается этими двумя направлениями. Наличие современных методов тестирования в совокупности со знанием их возможностей открывает широкие перспективы научных и прикладных работ по гепатиту С.
источник