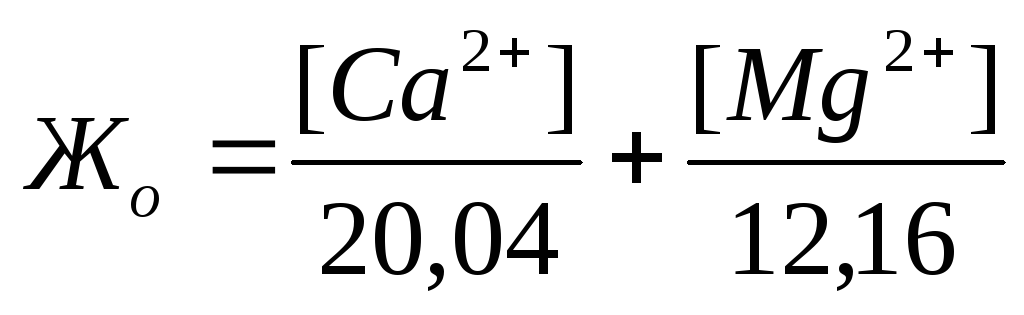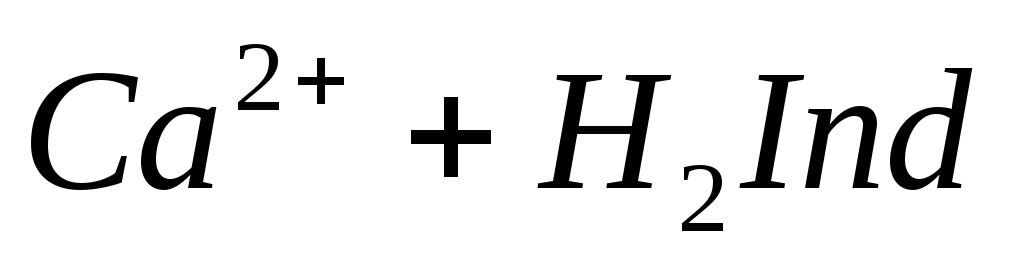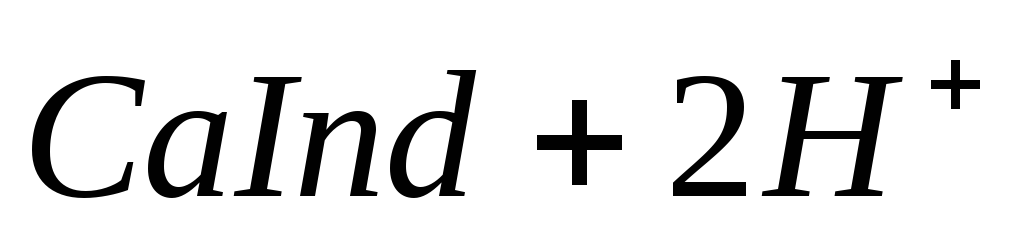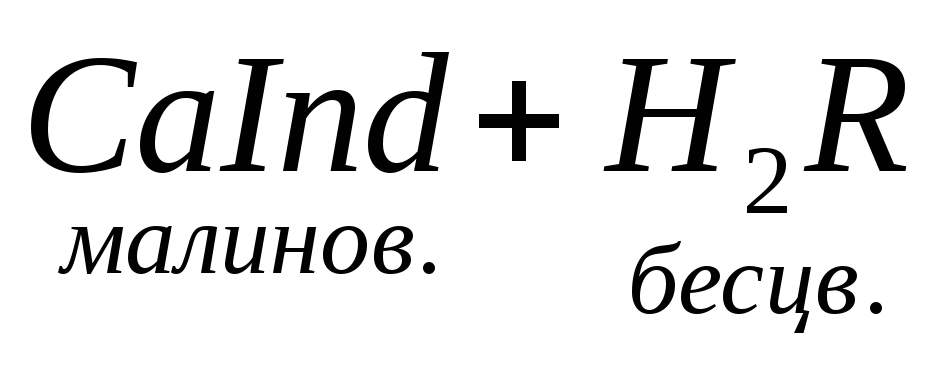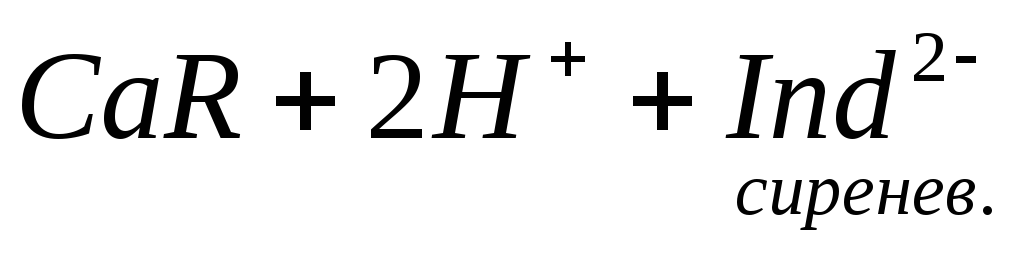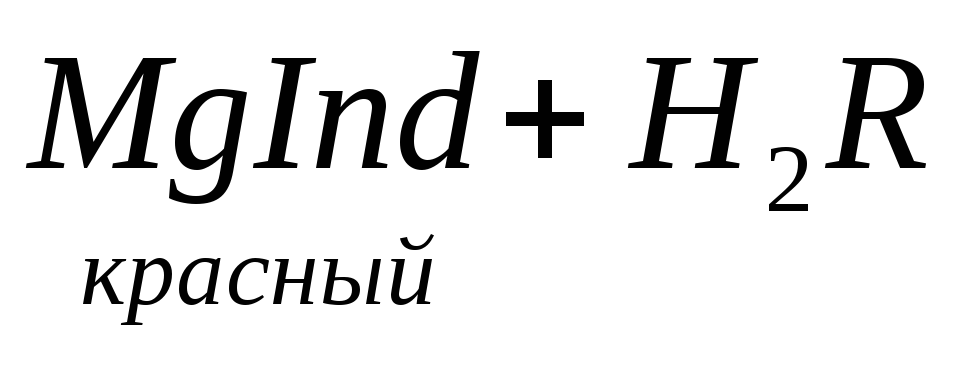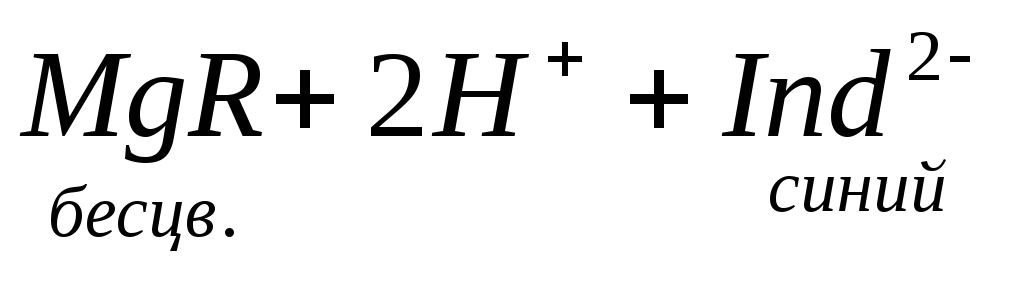Берут около 0,05—0,1 г полученного для анализа вещества и растворяют в 4—5 млдистиллированной воды. По таблице растворимости делают заключение, какие соли могут присутствовать в растворе.
Прежде чем приступить к анализу, обращают внимание на окраску и реакцию раствора. По окраске раствора можно сделать предварительное заключение о наличии или отсутствии тех или иных ионов, например: Си 2+ , Со 2+ , Ni 2+ , Fе 3+ , Сr 3+ , СrО4 2 — , Сr2О7 2 — и др. Щелочная реакция раствора свидетельствует о присутствии в растворе гидроксидов или солей сильных оснований и слабых кислот (Nа2S, К2СО3, СН3ОООNа и т. п.). Кислая реакция указывает на присутствие в растворе свободных кислот, кислых солей или солей сильных кислот и слабых оснований (NН4С1, ZпС12, А1С13 и т. п.). Нейтральная реакция указывает, что в растворе могут быть соли сильных кислот и сильных оснований (КС1, Nа2SО4) или соли слабых кислот и слабых оснований, подобных NН4СН3СОО.
После предварительного испытания раствора анализа вещества
•приступайте к открытию катионов и анионов.
Обнаружение катионов.
Из отдельных проб раствора при помощи групповых реактивов определите, катионы каких аналитических групп присутствуют в растворе.
Испытание на катионы первой группы.К 3—4 каплям исследуемого раствора прибавьте 2—3 капли раствора карбоната натрия Nа2СО3. Если осадок не выпадает, то в растворе могут присутствовать только катионы первой группы. В отдельной пробе открывают катионы первой группы.
Испытание на катионы второй группы.Если при действии карбоната натрия Nа2СО3 на испытуемый раствор выпадает осадок, то берут новую пробу этого раствора (10—12 капель) и прибавляют 2—3 капли 2 н раствора соляной кислоты. В случае появления осадка добавляют соляной кислоты до полного осаждения. Осадок отделяют центрифугированием, промывают водой и обнаруживают в нем катионы второй группы.
Испытание на катионы третьей группы.К 2—3 каплям анализируемого раствора прибавляют столько же 2 н раствора серной кислоты и нагревают. Выпадение осадка указывает на присутствие катионов третьей группы, которые открываются характерными для них реакциями.
Испытание на катионы четвертой группы. Если при действии соляной и серной кислот осадков не образуется, то к 2—3 каплям анализируемого раствора добавляют избыток гидроксида натрия (5—6 капель). Растворение первоначально выпавшего осадка свидетельствует о присутствии катионов четвертой группы.
Испытание на катионы пятой группы. Если при действии избытка раствора гидроксида натрия осадок не растворяется, это указывает о наличии катионов пятой группы.
Испытание на катионы шестой группы. Если при действии на испытуемый раствор избытком раствора аммиака осадок растворяется, то это признак присутствия катионов шестой группы.
После этого приступают к обнаружению катионов.
Обнаружение анионов.
Установление присутствия тех или иных катионов в исследуемом растворе значительно облегчает обнаружение анионов. Пользуясь таблицей растворимости, можно заранее предсказать наличие в исследуемом растворе отдельных анионов. Например, если соль хорошо растворяется в воде и в нейтральном водном растворе обнаружен катион Ва 2+ , то этот раствор не может содержать анионы SO4 2 — , СO3 2 — , SO3 2 — .
Определив предварительно присутствие отдельных групп анионов, обнаруживают их соответствующими групповыми и характерными для них реакциями. В зависимости от присутствия тех или иных анионов и катионов схемы анализа могут быть самыми различными. Например, водный раствор исследуемого вещества имеет нейтральную реакцию. При действии на отдельную пробу его раствором соляной кислоты образуется осадок, который растворяется в горячей воде. Это позволяет сделать вывод, что в растворе присутствует катион Рb 2+ . Проверяют катион Рb 2+ частной реакцией с иодидом калия КI. Далее обнаруживают анионы. Ими могут быть только анионы третьей группы, так как только они образуют с катионом Рb 2+ растворимые в воде соли.
Испытание на анионы первой группы. К 2—3 каплям нейтрального или слабощелочного раствора добавляют 2 капли раствора хлорида бария. Если осадок выпадает, то присутствуют анионы первой группы.
Испытание на анионы второй группы. 2 капли раствора подкисляют 2 каплями 2 н раствора азотной кислоты и добавляют каплю раствора нитрата серебра. Выпадение осадка указывает на присутствие анионов второй группы.
Испытание на анионы третьей группы. Если при испытании на анионы первой и второй групп осадки не выпали, то, возможно, присутствуют анионы третьей группы.
Дата добавления: 2015-11-05 ; просмотров: 508 | Нарушение авторских прав
источник
Берут около 0,05—0,1 г полученного для анализа вещества и растворяют в 4—5 млдистиллированной воды. По таблице растворимости делают заключение, какие соли могут присутствовать в растворе.
Прежде чем приступить к анализу, обращают внимание на окраску и реакцию раствора. По окраске раствора можно сделать предварительное заключение о наличии или отсутствии тех или иных ионов, например: Си 2+ , Со 2+ , Ni 2+ , Fе 3+ , Сr 3+ , СrО4 2 — , Сr2О7 2 — и др. Щелочная реакция раствора свидетельствует о присутствии в растворе гидроксидов или солей сильных оснований и слабых кислот (Nа2S, К2СО3, СН3ОООNа и т. п.). Кислая реакция указывает на присутствие в растворе свободных кислот, кислых солей или солей сильных кислот и слабых оснований (NН4С1, ZпС12, А1С13 и т. п.). Нейтральная реакция указывает, что в растворе могут быть соли сильных кислот и сильных оснований (КС1, Nа2SО4) или соли слабых кислот и слабых оснований, подобных NН4СН3СОО.
После предварительного испытания раствора анализа вещества
•приступайте к открытию катионов и анионов.
Из отдельных проб раствора при помощи групповых реактивов определите, катионы каких аналитических групп присутствуют в растворе.
Испытание на катионы первой группы.К 3—4 каплям исследуемого раствора прибавьте 2—3 капли раствора карбоната натрия Nа2СО3. Если осадок не выпадает, то в растворе могут присутствовать только катионы первой группы. В отдельной пробе открывают катионы первой группы.
Испытание на катионы второй группы.Если при действии карбоната натрия Nа2СО3 на испытуемый раствор выпадает осадок, то берут новую пробу этого раствора (10—12 капель) и прибавляют 2—3 капли 2 н раствора соляной кислоты. В случае появления осадка добавляют соляной кислоты до полного осаждения. Осадок отделяют центрифугированием, промывают водой и обнаруживают в нем катионы второй группы.
Испытание на катионы третьей группы.К 2—3 каплям анализируемого раствора прибавляют столько же 2 н раствора серной кислоты и нагревают. Выпадение осадка указывает на присутствие катионов третьей группы, которые открываются характерными для них реакциями.
Испытание на катионы четвертой группы. Если при действии соляной и серной кислот осадков не образуется, то к 2—3 каплям анализируемого раствора добавляют избыток гидроксида натрия (5—6 капель). Растворение первоначально выпавшего осадка свидетельствует о присутствии катионов четвертой группы.
Испытание на катионы пятой группы. Если при действии избытка раствора гидроксида натрия осадок не растворяется, это указывает о наличии катионов пятой группы.
Испытание на катионы шестой группы. Если при действии на испытуемый раствор избытком раствора аммиака осадок растворяется, то это признак присутствия катионов шестой группы.
После этого приступают к обнаружению катионов.
Установление присутствия тех или иных катионов в исследуемом растворе значительно облегчает обнаружение анионов. Пользуясь таблицей растворимости, можно заранее предсказать наличие в исследуемом растворе отдельных анионов. Например, если соль хорошо растворяется в воде и в нейтральном водном растворе обнаружен катион Ва 2+ , то этот раствор не может содержать анионы SO4 2 — , СO3 2 — , SO3 2 — .
Определив предварительно присутствие отдельных групп анионов, обнаруживают их соответствующими групповыми и характерными для них реакциями. В зависимости от присутствия тех или иных анионов и катионов схемы анализа могут быть самыми различными. Например, водный раствор исследуемого вещества имеет нейтральную реакцию. При действии на отдельную пробу его раствором соляной кислоты образуется осадок, который растворяется в горячей воде. Это позволяет сделать вывод, что в растворе присутствует катион Рb 2+ . Проверяют катион Рb 2+ частной реакцией с иодидом калия КI. Далее обнаруживают анионы. Ими могут быть только анионы третьей группы, так как только они образуют с катионом Рb 2+ растворимые в воде соли.
Испытание на анионы первой группы. К 2—3 каплям нейтрального или слабощелочного раствора добавляют 2 капли раствора хлорида бария. Если осадок выпадает, то присутствуют анионы первой группы.
Испытание на анионы второй группы. 2 капли раствора подкисляют 2 каплями 2 н раствора азотной кислоты и добавляют каплю раствора нитрата серебра. Выпадение осадка указывает на присутствие анионов второй группы.
Испытание на анионы третьей группы. Если при испытании на анионы первой и второй групп осадки не выпали, то, возможно, присутствуют анионы третьей группы.
источник
Проведение анализа. Для проведения анализа твердую пробу обычно растворяют в подходящем растворителе: в воде, в водных растворах кислот
Растворение пробы
Для проведения анализа твердую пробу обычно растворяют в подходящем растворителе: в воде, в водных растворах кислот, в органических растворителях, в растворах, содержащих комплексообразующие компоненты, и т.д.
Вначале проверяют растворимость пробы в дистиллированной воде при комнатной температуре, затем – при нагревании. При этом выясняют, растворяется ли проба в воде полностью или частично. Если проба не растворяется в воде, то испытывают ее растворимость в водных растворах разбавленных и концентрированных кислот: в уксусной СН3СООН, хлороводородной (соляной) НСl, азотной НNО3, серной H2SО4 и т.д. Если вещество не растворяется ни в разбавленных, ни в концентрированных кислотах, то испытывают его растворимость в царской водке – смеси концентрированных азотной и хлороводородной кислот (1ч. НNО3 и 3,6 ч. НСl, по объему).
При необходимости проверяют растворимость пробы в подходящих органических растворителях или в растворах, содержащих различные реагенты.
Если твердая проба не растворяется ни в одном из использованных растворителей, то в ряде случаев ее переводят в растворимое состояние обработкой при нагревании (обычно – повторной) насыщенными растворами соды Na2CО3, поташа К2СО3 или же сплавлением части пробы с этими солями, гидросульфатами щелочных металлов (NaHSО4), пиросульфатом калия К2S2О7 с щелочами и другими веществами. При такой обработке, например, некоторые катионы переходят в растворимые в водных кислотах карбонаты, основные соли, гидроксиды, оксиды.
После перевода пробы в раствор последний подвергают анализу.
Для обеспечения низкого предела обнаружения при анализе обычно используют ряд приемов. Рассмотрим некоторыеиз них на примере отдельных реакций.
1. Микрокристаллоскопический анализ. Для обнаружения ионов магния обычно применяют реакцию осаждения его в виде MgNH4P04 6H20 с пределом обнаружения – около10 мкг магния. При проведении этой же реакции микрокристаллоскопическим методом предел обнаружения понижается до 0,6 мкг.
2. Капельный анализ. Диметилглиоксим образует с ионами никеля в нейтральных, уксуснокислых и аммиачных растворах ярко-красный осадок. При выполнении реакции на капельной пластинке предел обнаружения никеля составляет – 0,16 мкг; в пробирке же можно обнаружить только 1,4 мкг никеля в 1 мл. Предел обнаружения можно снизить до 0,015 мкг, если каплю анализируемого раствора нанести на фильтровальную бумагу, пропитанную диметилглиоксимом.
3. Флотация. Осадок диметилглиоксимата никеля флотируется на границе раздела фаз вода — изоамиловый спирт или вода — диэтиловый эфир. При этом предел обнаружения никеля понижается до 0,002 мкг.
4. Экстракция. Диэтилдитиокарбаминаты образуют с ионами меди (II) внутрикомплексное соединение красного цвета, хорошо растворимое в хлороформе и тетрахлориде углерода, предел обнаружения меди — 0,01 мкг.
5. Метод «умножающихся реакций». «Умножающиеся реакции» — ряд последовательных реакций, в результате которых получается новое вещество в количестве, во много раз превышающем первоначальное количество обнаруживаемого вещества. Коэффициент умножения может достигать десятков и сотен.
6. Каталитические реакции. Окисление тиосульфат-ионов ионами железа (III) ускоряется в присутствии ионов меди.
Время обесцвечивания тиоцианата железа тиосульфатом натрия в отсутствие меди около 2 мин. В присутствии ионов меди раствор обесцвечивается мгновенно. Предел обнаружения меди — 0,02 мкг.
7. Люминесцентные реакции. В нейтральных и уксуснокислых растворах ионы алюминия образуют с морином комплексное соединение, способное к интенсивной зеленой флуоресценции при дневном и ультрафиолетовом освещении. Предел обнаружения алюминия — 0,2 мкг. Предел обнаружения можно снизить до 0,005 мкг, если нанести каплю анализируемого раствора на фильтровальную бумагу, пропитанную раствором морина. После обработки пятна раствором НС1 наблюдают светло-зеленую флуоресценцию.
8. Реакции на носителях. В присутствии ионов германия на поверхности анионообменника, обработанного раствором гема-токсилина, появляется фиолетовое или черное окрашивание. Поверхность сорбента в отсутствие германия окрашена в желтый цвет. Предел обнаружения германия — 0,003 мкг.
Контрольные вопросы и задания
1. Дайте определение понятиям «качественный» и «количественный» анализ, «инструментальные методы анализ» и другим терминам.
2. Перечислите основные аналитические признаки и виды аналитических реакций, а также подробнее охарактеризуйте какой-нибудь тип аналитической реакции (с примером).
3. Какие типы аналитических реакций (реагентов) бывают (приведите примеры)?
4. Какими показателями можно охарактеризовать чувствительность аналитической реакции (метода)?
5. Каковы особенности отбора проб веществ различного физического состояния и какие пробы бывают?
6. Как правильно растворять пробу и каковы приемы для повышения чувствительности анализа?
1. Фадеева В.И., Шеховцева Т.Н., Иванов В.М. и др. Основы аналитической химии. Практическое руководство. Учеб. пособие для вузов. /Под ред. Ю.А. Золотова. М.: Высш. шк., 2001. – 463 с.
2. Харитонов Ю.Я. Аналитическая химия (аналитика). В 2 книгах. Кн. 1. Общие теоретические основы. Качественный анализ. Учебн. для вузов. – М.: Высш. шк., 2001. – 615 с.
Дата добавления: 2014-12-26 ; Просмотров: 1208 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
Цветность природных вод колеблется от единиц до тысяч градусов. Предельное значение цветности для питьевой воды — 30 градусов.
Бытовое и химическое понимание цветности не всегда совпадает. Вода может быть почти оранжевой от оксидов железа, но это считается не цветностью, а мутностью, и отфильтровывается обычным бумажным фильтром.
Высокая цветность воды ухудшает ее органолептические свойства и оказывает отрицательное влияние на развитие водных растительных и животных организмов в результате резкого снижения концентрации растворенного кислорода в воде, который расходуется на окисление соединений железа и гумусовых веществ. Но сам по себе показатель цветности не говорит о характере загрязнения, но если он высокий, значит какое-то загрязнение есть.
Мутность воды может быть вызвана самыми разнообразными причинами — присутствием карбонатов, гидроксидов алюминия, высокомолекулярных органических примесей гумусового происхождения, появлением фито- и изопланктона, а также окислением соединений железа и марганца кислородом воздуха.
- 1. Взвеси из грязи, ила, глины в воде. Взвеси в поверхностных водах (пруды, озера, родники), особенно после дождей.
- 2. Песок, мелкий гравий, грязевой или глинистый осадок. Несет песок из еще непромытой новой скважины или дефектный сетчатый экран.
- 3. Хлопья ржавчины в воде, красноватый цвет воды и бурый осадок. Вода с повышенной кислотностью вымывает железо из трубопроводов.
- 4. В воде серые нитевидные волокна. Во входной воде содержится органика — водоросли и т.д.
Высокая мутность является признаком наличия в воде неких примесей, возможно токсичных, кроме того, в мутной воде лучше развиваются различные микроорганизмы. В России мутность воды определяют фотометрическим путем сравнения проб исследуемой воды со стандартными суспензиями. Результат измерений выражают в мг/дм3 при использовании основной стандартной суспензии каолина или в ЕМ/дм3 (единицы мутности на дм3) при использовании основной стандартной суспензии формазина.
Согласно СанПиН 2.1.4.1175-02 «Гигиенические требования к качеству воды нецентрализованного водоснабжения. Санитарная охрана источников» мутность воды должна находиться в диапазоне 2,6-3,5 ЕМ/дм3.
Водородный показатель, рН↑ Наверх
В зависимости от уровня рН воды можно условно разделить на несколько групп:
- сильнокислые воды 9.5
- Для питьевой и хозяйственно-бытовой воды оптимальным считается уровень рН в диапазоне от 6 до 9 единиц.
Общая жесткость↑ Наверх
Жесткость воды – содержание в ней растворенных солей кальция и магния. Суммарное содержание этих солей называют общей жесткостью.
Величина общей жесткости в питьевой воде не должна превышать 10,0 oЖ. Особые требования предъявляются к технической воде для различных производств, так как накипь может выводить технику из строя.
Проверить воду на жесткость необходимо перед её использованием в любых технических агрегатах, связаных с нагревом и кипением воды. Не спешите покупать фильтр, чтобы снизить жесткость воды, может быть она и так в пределах нормы.
Подробнее про вред жесткой воды вы можете узнать из следующей статьи .
Окисляемость перманганатная↑ Наверх
Этот показатель отражает общую концентрацию органики в воде. Природа органических веществ может быть самой разной — и гуминовые кислоты почв, и сложная органика растений, и химические соединения антропогенного происхождения.
Поверхностные воды имеют более высокую окисляемость по сравнению с подземными. Это понятно — органика из почвы и растительного опада легче попадает в поверхностные воды, чем в грунтовые, чаще всего ограниченные глинистыми водоупорами. Вода равнинных рек как правило имеет окисляемость 5-12 мг О2 /дм3, рек с болотным питанием — десятки миллиграммов на 1 дм3. Подземные воды имеют в среднем окисляемость на уровне от сотых до десятых долей миллиграма О2 /дм3.
ПДК питьевой воды по перманганатной окисляемости согласно СанПиН 2.1.4.1175-02 «Гигиенические требования к качеству воды нецентрализованного водоснабжения. Санитарная охрана источников» составляет 5,0-7,0 мг/дм3.
Общая минерализация↑ Наверх
Общая минерализация — суммарный количественный показатель содержания растворенных в воде веществ. Этот параметр также называют содержанием растворимых веществ или общим солесодержанием, так как растворенные в воде вещества как правило находятся именно в виде солей.
К числу наиболее распространенных относятся неорганические соли (в основном бикарбонаты, хлориды и сульфаты кальция, магния, калия и натрия) и небольшое количество органических веществ, растворимых в воде.
Нефтепродукты↑ Наверх
К сожалению, загрязнение воды нефтепродуктами — явление очень распространенное. Промышленные стоки, аварии при нефтеперевозке, стоки с АЗС и автотранспорта — все это приводит к загрязнению поверхностных водотоков.
Нефтепродукты опасны для здоровья и ухудшают органолептические качества воды — придают ей стойкий «нефтяной» запах.
Предельно допустимая концентрация нефтепродуктов в воде составляет 0,1 мг/дм3.
Анализ воды на хлор необходим в первую очередь для воды, прошедшей процедуру хлорирования.
Остаточный хлор присутствует в питьевой водопроводной воде. Он весьма летуч и небольшие его концентрации быстро улетучиваются из воды. Но при высоких концентрациях свободный хлор представляет серьезную опасность для здоровья человека. В природных водоемах он присутствовать не должен.
Как правило, концнентрации аммиака в воде не достигают опасных значений, но он вступает в реакцию с другими соединениями, в результате чего возникают более токсичные вещества.
ПДК аммиака в воде 2,0 мг/дм3.
Анализ воды на фенол важен для природных и сточных вод. Необходимо проверять воду на содержание фенола если есть подозрение в загрязнении водотоков промышленными стоками.
Фенолы — соединения нестойкие и подвергаются биохимическому и химическому окислению. Многоатомные фенолы разрушаются в основном путем химического окисления.
Однако при обработке хлором воды, содержащей примеси фенола, могут образовываться очень опасные органические токсиканты — диоксины.
Анализ воды на нитриты делается для вод поверхностных и приповерхностных водотоков. Проверять содержание нитритов в воде особенно важно при анализе воды из колодцев и родников.
Повышенное содержание нитритов указывает на усиление процессов разложения органических веществ в условиях медленного окисления NO2 в NO3, это указывает на загрязнение водоема. Содержание нитритов является важным санитарным показателем.
ПДК нитритов в воде составляет 3 мг/дм3. Нитриты значительно опаснее нитратов, поэтому их содержание в воде контролируется более строго.
Способы устранения нитритов из воды: обратный осмос для дома , обратный осмос для квартиры . Селективность мембраны обратного осмоса составляет по нитритам 89%-96%.
Наибольшие концентрации нитратов обнаруживаются в поверхностных и приповерхностных подземных водах, наименьшие – в глубоких скважинах. Очень важно проверять на содержание нитратов воду из колодцев, родников, водопроводную воду, особенно в районах с развитым сельским хозяйством.
Смертельная доза нитратов для человека составляет 8-15 г. При длительном употреблении питьевой воды и пищевых продуктов, содержащих значительные количества нитратов, возрастает концентрация метгемоглобина в крови. Снижается способность крови к переносу кислорода, что ведет к неблагоприятным последствиям для организма. ПДК нитратов в воде составляет 45 мг/дм3.
Способы устранения нитритов из воды: обратный осмос для дома, обратный осмос для квартиры. Селективность мембраны обратного осмоса составляет по нитратам 60%, остаточные нитраты удаляются специальной нитратселективной смоле Purolite А-520.
Присутствие хлоридов объясняется присутствием в породах наиболее распространенной на Земле соли – хлорида натрия. Повышенное содержание хлоридов объясняется загрязнением водоема сточными водами. ПДК хлоридов в воде составляет 350 мг/дм3.
Повышенные содержания сульфатов ухудшают органолептические свойства воды и оказывают физиологическое воздействие на организм человека – они обладают слабительными свойствами.
Если сам активный хлор быстро улетучивается из воды, то хлороформ и другие хлорорганические соединения остаются в ней надолго, и сами по себе из воды не уйдут. Необходима доочистка питьевой воды. Но не следует спадать в панику- в обычно содержание этих веществ в воде не вызывает острого отравления. Потенциальный риск для здоровья относят к отдаленным последствиям хронического отравления.
Питьевая вода с концентрацией фтора более 0,2 мг/л является основным источником его поступления в организм. Воды поверхностных источников характеризуются преимущественно низким содержанием фтора (0,3-0,4 мг/л). Высокие содержания фтора в поверхностных водах являются следствием сброса промышленных фторсодержащих сточных вод или контакта вод с почвами, богатыми соединениями фтора. Максимальные концентрации фтора (5-27 мг/л и более) определяют в артезианских и минеральных водах, контактирующих с фторсодержащими водовмещающими породами.
При гигиенической оценке поступления фтора в организм важное значение имеет содержание микроэлемента в суточном рационе, а не в отдельных пищевых продуктах. В суточном рационе содержится от 0,54 до 1,6 мг фтора (в среднем 0,81 мг). Как правило, с пищевыми продуктами в организм человека поступает в 4-6 раз меньше фтора, чем при употреблении питьевой воды, содержащей оптимальные его количества (1 мг/л).
Фтор является устойчивым компонентом природных вод. Колебания концентрации фтора в течение года невелики (обычно не более, чем в два раза).
Повышенное содержание фтора в воде (более 1,5 мг/л) оказывает вредное влияние на людей и животных, у населения развивается эндемический флюороз. Отмечается характерное поражение зубов, нарушение процессов окостенения скелета, истощение организма. Содержание фтора в питьевой воде лимитируется. Установлено, что систематическое использование населением фторированной воды снижает и уровень заболеваний , связанных с последствиями одонтогенной инфекции (ревматизм, сердечно-сосудистая патология, заболевания почек и др.).
ПДК фтора составляет 1,5 мг/л.
Отличительная особенность калия — его способность вызывать усиленное выведение воды из организма. Поэтому пищевые рационы с повышенным содержанием элемента облегчают функционирование сердечно-сосудистой системы при ее недостаточности, обусловливают исчезновение или существенное уменьшение отеков.
Дефицит калия в организме ведет к нарушению функции нервно-мышечной (парезы и параличи) и сердечно-сосудистой систем и проявляется депрессией, дискоординацией движений, мышечной гипотонией, гипорефлек-сией, судорогами, артериальной гипотонией, брадикардией, изменениями на ЭКГ, нефритами, энтеритами и др. ПДК калия составляет 20 мг/дм3.
В поверхностных водах натрий мигрирует преимущественно в растворенном состоянии. Концентрация его в речных водах колеблется от 0,6 до 300 мг/3 в зависимости от физико-географических условий и геологических особенностей водных объектов. В поземных водах концентрация натрия колеблется в широких пределах — от миллиграммов до десятков граммов в 1 литре. Это определяется глубиной залегания подземных вод и другими условиями гидрогеологической обстановки.
Биологическая роль натрия крайне важна для большинства форм жизни на Земле, включая человека. Организм человека содержит около 100 г натрия. Ионы натрия активируют ферментативный обмен в организме человека. Избыточное содержание натрия в воде и пище приводит к гипертензии и гипертонии.
ПДК натрия составляет 200 мг/дм3.
Концентрация кальция в поверхностных водах имеет заметные сезонные колебания: весной содержание ионов кальция повышено, что связано с легкостью выщелачивания растворимых солей кальция из поверхностного слоя почв и пород.
Жесткие требования предъявляются к содержанию кальция в водах, питающих паросиловые установки, так как в присутствии карбонатов, сульфатов и ряда других анионов кальций образует прочную накипь. Данные о содержании кальция в воде необходимы так же при решении вопросов, связанных с формированием химического состава природных вод, их происхождением, а так же при исследовании карбонатно-кальциевого равновесия. ПДК кальция находится в диапазоне 25- 130 мг/дм3.
В речных водах содержание магния обычно колеблется от нескольких единиц до десятков миллиграммов в 1 литре. Содержание магния в поверхностных водах меняется в течение года, значительно снижаясь в период половодья.
Катион магния активирует в организме человека ферменты, участвующие в переносе фосфатных групп, синтезе и распаде АТФ, превращении многих витаминов, в частности В6, в активные коферменты. Магний чрезвычайно важен для нормального функционирования нервной системы. Дефицит магния снижает устойчивость организма к инфекциям, стрессовым ситуациям и острым нарушениям мозгового кровообращения. Содержание магния в организме взрослого человека около 20 г. Но и превышение предельно допустимых концентраций магния в воде вредно. ПДК составляет 5-65 мг/дм3.
Концентрация железа в воде зависит от рН и содержания кислорода в воде. Железо в воде колодцев и скважин может находится как в окисленной, так и в востановленной форме, но при отстаивании воды всегда окисляется и может выпадать в осадок. Много железа растворено в кислых бескислородных подземных водах.
Вода из крана холодной воды поступает прозрачная, но со временем, особенно при нагревании, приобретает бурую окраску. Белье при стирке приобретает желтоватый оттенок. Потемнение кофе, чая и других напитков.
Анализ воды на железо необходим для самых разных типов воды — поверхностных природных вод, приповерхностных и глубинных подземных вод, сточных вод промышленных предприятий.
Содержащая железо вода (особенно подземная) сперва прозрачна и чиста на вид. Однако даже при непродолжительном контакте с кислородом воздуха железо окисляется, придавая воде желтовато-бурую окраску. Уже при концентрациях железа выше 0,3 мг/дм3 такая вода способна вызвать появление ржавых потеков на сантехнике и пятен на белье при стирке. При содержании железа выше 1 мг/дм3 вода становится мутной, окрашивается в желто-бурый цвет, у нее ощущается характерный металлический привкус. Все это делает такую воду практически неприемлемой как для технического, так и для питьевого применения.
Наличие в воде растворенного (двухвалентного железа) в количестве выше 0,3 мг/л . Железо в концентрациях выше 0,3 мг/л вызывает бурые подтеки на водопроводной арматуре, сантехнике, пятна на посуде и белье после стирки.
ПДК железа в воде 0,3 мг/дм3.
Растворимые соединения меди ядовиты. Поэтому предметы хозяйственного обихода — самовары, чайники, кастрюли и т. д., сделанные из меди, покрывают внутри слоем олова — лудят, защищая медь от растворения и предупреждая возможность пищевых отравлений. Хроническая интоксикация медью и ее солями может приводить к функциональным расстройствам нервной системы, печени и почек, изъязвлению и перфорации носовой перегородки, аллергодерматозам.
Цинк содержится в воде в виде солей и органических соединений. При больших концентрациях он придает воде вяжущий привкус. Цинк может нарушать обмен веществ, особенно сильно он нарушает метаболизм железа и меди в организме.
Цинк попадает в воду с промышленными стоками, вымывается из оцинкованных труб и иных коммуникаций, может накапливаться и поступать в воду из ионообменных фильтров.
Анализ воды на свинец важен для поверхностных вод питьевых и сточных вод. Необходимо проверить воду на содержание свинца, если есть подозрения в попадании в водоток промышленных стоков.
Для всех регионов России свинец — основной антропогенный токсичный элемент из группы тяжелых металлов, что связано с высоким индустриальным загрязнением и выбросами автомобильного транспорта, работающего на этилированном бензине.
Свинец накапливается в теле, костях и поверхностных тканях. Свинец влияет на почки, печень, нервную систему и органы кровообразования. Пожилые и дети особенно чувствительны даже к низким дозам свинца.
В природные воды кадмий поступает при выщелачивании почв, полиметаллических и медных руд, в результате разложения водных организмов, способных его накапливать. Соединения кадмия выносятся в поверхностные воды со сточными водами свинцово-цинковых заводов, рудообогатительных фабрик, ряда химических предприятий (производство серной кислоты), гальванического производства, а также с шахтными водами.
ПДК составляет 0,001 мг/дм3.
На Земле никель почти всегда встречается совместно с кобальтом и главным образом в виде смеси соединений никеля с кобальтом и мышьяком (купферникель), с мышьяком и серой (никелевый блеск), с железом, медью и серой (пентландит) и другими элементами. Его относительно мало в поверхностных водах, в живом веществе.
ПДК никеля в питьевой воде в России составляет О,1 мг/л.
В природные воды соединения кобальта попадают в результате процессов выщелачивания их из медноколчедановых и других руд, из почв при разложении организмов и растений, а также со сточными водами металлургических, металлообрабатывающих и химических заводов. Некоторые количества кобальта поступают из почв в результате разложения растительных и животных организмов.
Концентрация марганца в поверхностных водах подвержена сезонным колебаниям.
Факторами, определяющими изменения концентраций марганца, являются соотношение между поверхностным и подземным стоком, интенсивность потребления его при фотосинтезе, разложение фитопланктона, микроорганизмов и высшей водной растительности, а также процессы осаждения его на дно водных объектов.
Ртуть — в обычных условиях — жидкий, летучий металл. Очень опасное и токсичное вещество. ПДК ртути в воде — всего 0,0005 мг/дм3.
Ртуть поражает центральную нервную систему, особенно у детей, кровь, почки, вызывает нарушение репродуктивной функции. Особенно опасна метилртуть — металл-органическое соединение, образующиеся в воде при наличии ртути. Метилртуть очень легко всасывается тканями организма и очень долго из него выводится.
Практически все загрязнение воды ртутью имеет искусственное происхождение — ртуть попадает в природные водотоки из сточных вод промышленных производств.
Мышьяк — один из самых известных ядов. Это металл, токсичный для большинства живых существ. При отравлении мышьяком поражается центральная и периферическая нервная система, кожа, периферическая сосудистая система.
Неорганический мышьяк более опасен, чем органический, трехвалентный более опасен, чем пятивалентный. Главным источником мышьяка в воде являются промышленные стоки.
Предельно допустимая концентрация (ПДК) мышьяка в воде — 0,05 мг/дм3. Такая величина отражает очень высокую токсичность мышьяка.
Пестициды — это группа разнообразных веществ, используемых в сельском хозяйстве для борьбы с сорняками, насекомыми и грызунами, включает около пятидесяти наименований. Среди пестицидов есть сравнительно безвредные, но все в той или иной степени ядовиты, и, по крайней мере, четыре-пять из них способствуют возникновению рака (канцерогенны). С полей они попадают в водоёмы, а оттуда могут проникнуть в питьевую воду. Если концентрации самых опасных пестицидов очень малы, порядка нанограмм-микрограмм на литр, они не наносят организму существенного вреда.
Бактериология и паразитология↑ Наверх
Очень опасно присутствие в питьевой воде микроорганизмов, особенно бактерий из группы кишечных палочек и энтеровирусы, поражающих желудочно-кишечный тракт, а также вирус гепатита. Они попадают в воду из городских канализаций, разносятся сточными водами с полей, удобряемых навозом. Дожди и разливы рек смывают навоз в водоемы, где микрофлора начинает бурно размножаться. Чтобы обеззаразить воду от микроорганизмов, её хлорируют.
Растворенный в воде радон действует двояко. С одной стороны, он вместе с водой попадает в пищеварительную систему, а с другой стороны, люди вдыхают выделяемый водой радон при ее использовании. Дело в том, что в тот момент, когда вода вытекает из крана, радон выделяется из нее, в результате чего концентрация радона в кухне или ванной комнате может в 30-40 раз превышать его уровень в других помещениях (например, в жилых комнатах). Второй (ингаляционный) способ воздействия рабона считается более опасным для здоровья.
Можно ли бороться с радоном в воде? Да и достаточно эффективно. Один из наиболее результативных методов борьбы с радоном — аэрирование воды («пробулькивание» воды пузырьками воздуха, при котором практически весь радон в прямом смысле «улетает на ветер»). Поэтому тем, кто пользуется муниципальной водой беспокоиться практически не о чем, так как аэрирование входит в стандартную процедуру водоподготовки на городских водоочистных станциях. Что же касается индивидуальных пользователей скважинной воды, то исследования показали достаточно высокую эффективность активированного угля.
Этот познавательный материал мы разместили специально для посетителей нашего ресурса, что бы вы смогли прочитать ознакомится с тем, что попадает к вам в организм с водой из водопроводных труб, колодцев, скважин.
Как мы уже писали ранее в нашем блоге вода это жизнь, а чистая вода это здоровая и полноценная жизнь.
источник
- Вы здесь:
- Качество
- Методики и тесты
- Метод определения содержания нерастворимых в воде веществ в жидких формах БАД
Сухим остатком, или сухими веществами, называется все то, что остается от продукта при сушке, после удаления из него влаги. Количество сухих веществ достигает приблизительно 10 — 20%, из них около 2 — 5 % являются нерастворимыми в воде соединениями. Это воск, крахмал, некоторые азотистые соединения, протопектин, входящий в состав клеточных стенок клетчатки. Сами по себе эти соединения не оказывают вредного воздействия на организм, но не растворяясь в воде, особенно еще и в большом количестве, влияют на качество продукции. Например, для производства жидких форм БАД в качестве сырья используют сухие экстракты. И плохорастворимые соединения кроме того что дают осадок, еще и в значительно меньшем процентном отношении «отдают» все свои биологически активные вещества. В нормативной документации, в частности Государственной фармакопеи, указаны нормы содержания сухого (нерастворимого в воде) остатка на каждый вид продукции или сырья.
Существуют различные методы определения сухих веществ в пищевых продуктах:
— высушивание в шкафу (сушильном);
 |
| Рис. 1. Высушивание фильтра в сушильном шкафу |
Этот показатель очень важен при производстве жидких форм БАД (каплей, сиропов). Ведь нерастворимые в воде вещества будут давать осадок и замутнение, что повлияет на качество готовой продукции. Случается, что недобросовестные поставщики вместо качественного сырья, например экстрактов, поставляют такие, в которых в большом количестве содержаться плохо растворимые компоненты. На контрактном производстве ООО «КоролевФарм» при входном контроле сырья измерение массовой доли сухого остатка является обязательной процедурой, которая входит в общую систему контроля качества выпускаемой продукции, которая гарантирует производство качественной продукции. И эта продукция соответствует требованиям нормативной документации и Государственной фармакопеи.
Определение нерастворимых в воде веществ проводят в Аналитической лаборатории на участке физико-химических испытаний (ФХИ) методом высушивания в сушильном шкафу определяют массовую долю сухих, нерастворимых в воде, веществ. В лаборатории для этого есть все необходимые реактивы, материалы, аппаратура:
— эксикатор с фарфоровой вставкой;
Перед проведением испытания инженер-химик высушивает кружки фильтровальной бумаги в сушильном шкафу при температуре 105 0 С в течение 30 мин (рис. 1). Диаметр фильтра при этом должен соответствовать размеру воронки Бюхнера. Далее Сотрудник лаборатории охлаждает бумагу в эксикаторе (рис. 2) и взвешивает на весах. Потом кружок фильтровальной бумаги помещает в воронку Бюхнера, приливая при этом маленькими порциями дистиллированную воду, плотно прижимает фильтр ко дну воронки.
Берем навеску подготовленной пробы, помещаем в стакан, объем которого 400 см 3 . Для разного вида испытуемого образца, берем навеску определенной массы. Так для сушеных овощей — 0,5 г, для соков с мякотью 100,00 г, для джемов и варенья – 25,00 г. Для стальных видов продуктов навеску рассчитываем по формуле m , где Х — значение в процентах количества сухих (нерастворимых) веществ в продукте (предполагаемое).
Доливаем в стакан приблизительно 250 мл горячей воды дистиллированной, перемешиваем содержимое, далее нагреваем до кипения (рис. 3) и при слабом кипячении выдерживаем около 5-10 мин.
Потом смесь переносим в воронку Бюхнера и фильтруем при разрежении (рис. 4). При этом надо обязательно следить за качеством фильтрата. Он должен быть прозрачным. Если частички проникают в фильтрат, тогда надо поменять марку фильтровальной бумаги и, может быть, изменить режим разрежения в колбе.
Содержимое на фильтре промываем горячей водой (500-700 мл), добавляя порциями (по 100-120 мл).
Остаток пробы продукта вместе с фильтром (рис. 5) помещаем в выпарительную чашку и сушим в сушильном лабораторном шкафу около 2,5 ч., выдерживая температуру 105 0 С. После этого нашу пробу охлаждаем в эксикаторе и взвешиваем на лабораторных весах.
Обработка результатов.
Массовая доля сухих веществ в съедобной части продукта, нерастворимых в воде (Х) вычисляем по формуле:
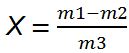
m1- вес фильтра с остатком продукта (высушенного) в г;
m2- вес самого высушенного фильтра в г;
m3- вес навески испытуемого продукта (образца) в г.
Все результаты получаем в процентах. Инженер-химик фиксирует их и выдает в виде протокола, который передается в отдел контроля качества. Также в протоколе указывается о соответствии или не соответствии данного образца нормативной документации. Специалисты отдела контроля качества на основании полученных протоколов выдают паспорт на сырье. Если результаты соответствуют спецификации, в которой указаны все требования с учетом особенностей выпускаемого продукта, то согласно разработанного и утвержденного процесса, сырье поступает на производство. В случае несоответствии полученных результатов спецификации или сопроводительным документам, сырье бракуется и возвращается обратно поставщику в соответствии процедуре, утвержденной в двустороннем порядке.
источник
В отличие от анализа индивидуальных соединений при анализе смеси неорганических веществ, как правило, желательно лишь установить, какие катионы или анионы содержит данная смесь или какие индивидуальные соединения входят в состав исследуемой смеси (фазовый анализ). Например, при анализе минералов важно знать не только их элементарный состав но и содержание определенных соединений — свободной и связанной и т. п.
В основном задача сводится к выполнению систематического анализа смеси катионов и анионов.
Смесь подвергают предварительным испытаниям (см. § 2) и затем делят на три порции, в одной из которых открывают катионы (см. гл. IX, § 1), в другой, после соответствующей подготовки, — анионы (см. гл. XII, § 25), а третью оставляют на случай проверки. Открытие катионов предшествует исследованию анионов, так как в присутствии некоторых катионов в растворе не может присутствовать ряд анионов.
Например, если данное для анализа вещество растворимо в воде и анализ показал, что в нем присутствуют катионы бария и серебра, то искать в растворе этого вещества и бессмысленно. Можно начинать анализ и с обнаружения анионов.
Если анализируемое вещество представляет собой бесцветный, прозрачный и нейтральный раствор, то, естественно, следует предположить, что в нем отсутстзуют окрашенные ионы и такие катионы и анионы, которые в нейтральном растворе, соединяясь, образуют осадки. Например, если найдены катионы IV группы, то в данных условиях отсутствуют фосфаты, карбонаты, сульфиды и т. если найдены катионы кальция, то отсутствуют карбонаты, фосфаты, оксалаты и т. д.
Характер среды испытуемого раствора указывает на вероятность присутствия или отсутствия некоторых катионов и анионов. Если, например, среда исследуемой смеси сильнощелочная, раствор пахнет аммиаком и бесцветен, то отсутствуют ионы и катионы, образующие в щелочном растворе осадки гидроокисей (например, и т. п.), а также все окрашенные анионы и катионы, образующие в щелочном растворе растворимые соединения (например, и т. п.). В этом случае можно предполагать присутствие солей щелочных металлов, образованных слабыми кислотами: цианидов, алюминатов, карбонатов, сульфитов, тиоарсенатов, станнитов, станнатов, фосфатов, арсенатов, плюмбитов, цинкатов, ванадатов, вольфраматов, молибдатов и т. п.
Еслр исследуемый раствор окрашен, сильно пахнет аммиаком и не содержит осадка, то, следовательно, отсутствуют катионы, осаждаемые раствором в виде гидроокисей (например, и т. п.), и анионы, дающие в щелочном растворе осадки в сочетании с некоторыми катионами (например, ); вероятно, присутствуют катионы, не осаждаемые гидроокисью аммония (например, и т. п.) и образующие с аммиаком комплексные соединения (например, ) и т. д.
В дальнейшем все сделанные предварительные наблюдения должны учитываться как при выборе схемы хода анализа, так и при окончательном выводе о составе смеси.
В каждом отдельном случае, используя теоретические знания, приобретенные при изучении курса аналитической химии, и практический опыт, накопленный в процессе выполнения лабораторных работ, выбирают наиболее рациональный вариант систематического или дробного метода анализа. При этом также учитывают количество имеющегося исследуемого вещества. Если располагают малым количеством анализируемого вещества, то применяют прецмущественно полумикро-, микро-и капельный методы анализа.
Систематический анализ. Для отделения ионов, затрудняющих дальнейший анализ смеси катионов, анализируемое вещество обрабатывают карбонатом натрия: твердые вещества сплавляют с или его смесями с другими соединениями, растворы кипятят с раствором , т. е. делают содовую вытяжку. При этом в осадок выпадают нерастворимые карбонаты, оксикарбонаты и гидроокиси. В растворе остаются все растворимые соли, а также натриевые соли кислот.
Осадок карбонатов, оксикарбонатов и гидроокисей сохраняют для анализа катионов, а раствор используют для анализа анионов.
Для отделения анионов, мешающих анализу катионов, вместо содовой вытяжки применяют также хроматографический метод (см. гл. VI, §22).
1) в карбонатный раствор частично переходят , гидроокиси которых обладают амфотерными свойствами, и и др., гидроокиси и оксикарбонаты которых не осаждаются в присутствии органических оксисоединений (винной кислоты и ее солей, глицерина, лимонной кислоты и т. п.);
2) при обработке нерастворимых соединений карбонатом натрия не все анионы с одинаковой легкостью переходят в карбонатный раствор. Некоторые соединения тяжелых металлов (сульфиды, галогениды, фосфаты и др.) остаются в осадке вместе с гидроокисями, карбонатами и оксикарбонатами.
Поэтому соответствующие катионы и анионы открывают не только в осадке или в растворе, но и в осадке и в карбонатном растворе. Так поступают в тех случаях, когда некоторые катионы не обнаруживаются в карбонатном осадке, а а нионы — в карбонатном растворе.
Большое значение в этом случае приобретают отдельные способы идентификации нерастворимых веществ (см. ниже).
Систематический ход анализа катионов описан в гл. IX, § 1, анионов в гл. XII, § 25.
источник
ГОСТ 29337-92 Сульфат аммония технический. Гравиметрический метод определения содержания вещества, не растворимого в воде
Текст ГОСТ 29337-92 Сульфат аммония технический. Гравиметрический метод определения содержания вещества, не растворимого в воде
ГРАВИМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ВЕЩЕСТВА,
ИПК ИЗДАТЕЛЬСТВО СТАНДАРТОВ Москва
Ammonium sulphate for industrial use.
Determination of matter insoluble in water content. Gravimetric method
Настоящий стандарт устанавливает гравиметрический метод определения содержания вещества, не растворимого в воде, в техническом сульфате аммония.
Дополнительные требования, отражающие потребности народного хозяйства, выделены курсивом.
Метод основан на растворении пробы для анализа в воде, фильтровании, высушивании и взвешивании вещества, не растворимого в воде.
Дистиллированная вода по ГОСТ 6709 или вода эквивалентной чистоты.
Барий хлористый по ГОСТ 4108, х. ч., раствор с массовой долей 10 %.
Обычная лабораторная аппаратура, а также оборудование, указанное ниже.
Фильтровальный тигель ТФ-32-ПОР 10 (16) по ГОСТ 25336 вместимостью 30 см 3 , диаметром фильтра 30 мм и степенью пористости Р 10 и 16 (размер пор от 4 до 16 мкм).
Стакан В-1-1000 ТС по ГОСТ 25336.
Весы лабораторные общего назначения типа ВЛР-200 по ГОСТ 24104* не ниже второго класса точности или весы другого типа с наибольшим пределом взвешивания 200 г, ценой наименьшего деления не более 1 ■ 10
Шкаф сушильный электрический типа 2В-151 по ТУ 64—1—1411—78.
Эксикатор типа 2—250 по ГОСТ 25336.
Термометр типа 4-Б—2 по ГОСТ 28498.
* С 1 июля 2002 г. введен в действие ГОСТ 24104—2001.
Издание официальное Перепечатка воспрещена
© Издательство стандартов, 1992 © ИПК Издательство стандартов, 2004
100 г испытуемого образца взвешивают с точностью до 0,1 г.
Пробу для анализа помещают в химический стакан вместимостью 1000 см 3 и растворяют в 500 см 3 воды, поддерживая температуру от 20 до 25 °С.
Испытуемый раствор фильтруют под вакуумом через фильтровальный тигель, предварительно высушенный при температуре (110+5) °С до постоянной массы и взвешенный с точностью до 0,0001 г.
Тигель и химический стакан тщательно промывают водой. Проводят испытание хлористым барием, чтобы убедиться в полном отсутствии сульфатов в промывных водах. Тигель и его содержимое высушивают в сушильном шкафу при температуре (110+5) °С в течение 1 ч. Охлаждают в эксикаторе и взвешивают с точностью до 0,0001 г. Повторяют высушивание, охлаждение и взвешивание до тех пор, пока результаты двух последовательных взвешиваний не будут отличаться более чем на 0,002 г.
3.4. Высушивание тигля с остатком проводят до постоянной массы, т. е. до получения расхождения между результатами двух последовательных взвешиваний не более 0,0001 г (результаты измерений записывают с точностью до четвертого десятичного знака).
Время охлаждения в эксикаторе тигля с осадком —1ч.
Время проведения анализа — 4 ч.
Содержание вещества, не растворимого в воде, (X) в процентах по массе определяют по формуле
где т() — массы пробы для анализа, г;
тх— масса не растворимого в воде вещества, г.
Допускаемая относительная суммарная погрешность результата измерения ±11 % при доверительной вероятности 0,95 (для массовой доли не растворимого в воде вещества, равной 0,01 %).
Оперативный контроль осуществляют по расхождению между результатами параллельных наблюдений.
За результат измерения принимают среднее арифметическое результатов двух параллельных наблюдений, абсолютное значение расхождения между которыми не превышает допускаемое расхождение, равное 0,002 %, при доверительной вероятности 0,95 (для массовых долей не растворимого в воде вещества 0,008—0,012 %).
1. ПОДГОТОВЛЕН И ВНЕСЕН Государственным научно-исследовательским и проектным институтом азотной промышленности и продуктов органического синтеза
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Госстандарта от 30.03.92 № 334 Настоящий стандарт подготовлен методом прямого применения международного стандарта ИСО 2994—74 «Сульфат аммония технический. Гравиметрический метод определения содержания вещества, не растворимого в воде» с дополнительными требованиями, отражающими потребности народного хозяйства
4. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
источник
Растворенный кислород находится в природной воде в виде молекул O2. На его содержание в воде влияют две группы противоположно направленных процессов: одни увеличивают концентрацию кислорода, другие уменьшают ее. К первой группе процессов, обогащающих воду кислородом, следует отнести:
· процесс абсорбции кислорода из атмосферы;
· выделение кислорода водной растительностью в процессе фотосинтеза;
· поступление в водоемы с дождевыми и снеговыми водами, которые обычно пересыщены кислородом.
Абсорбция кислорода из атмосферы происходит на поверхности водного объекта. Скорость этого процесса повышается с понижением температуры, с повышением давления и понижением минерализации. При каждом значении температуры существует равновесная концентрация кислорода, которую можно определить по специальным справочным таблицам, составленным для нормального атмосферного давления. Аэрация – обогащение глубинных слоев воды кислородом – происходит в результате перемешивания водных масс, в том числе ветрового, вертикальной температурной циркуляции и т.д.
Фотосинтетическое выделение кислорода происходит при ассимиляции диоксида углерода водной растительностью (прикрепленными, плавающими растениями и фитопланктоном). Процесс фотосинтеза протекает тем сильнее, чем выше температура воды, интенсивность солнечного освещения и больше биогенных (питательных) веществ (P, N и др.) в воде. Продуцирование кислорода происходит в поверхностном слое водоема, глубина которого зависит от прозрачности воды (для каждого водоема и сезона может быть различной, от нескольких сантиметров до нескольких десятков метров).
К группе процессов, уменьшающих содержание кислорода в воде, относятся реакции потребления его на окисление органических веществ: биологическое (дыхание организмов), биохимическое (дыхание бактерий, расход кислорода при разложении органических веществ) и химическое (окисление Fe 2+ , Mn 2+ , NO2 — , NH4 + , CH4, H2S). Скорость потребления кислорода увеличивается с повышением температуры, количества бактерий и других водных организмов и веществ, подвергающихся химическому и биохимическому окислению. Кроме того, уменьшение содержания кислорода в воде может происходить вследствие выделения его в атмосферу из поверхностных слоев и только в том случае, если вода при данных температуре и давлении окажется пересыщенной кислородом.
В поверхностных водах содержание растворенного кислорода варьирует в широких пределах – от 0 до 14 мг/дм 3 – и подвержено сезонным и суточным колебаниям. Суточные колебания зависят от интенсивности процессов его продуцирования и потребления и могут достигать
2,5 мг/дм 3 растворенного кислорода. В зимний и летний периоды распределение кислорода носит характер стратификации. Дефицит кислорода чаще наблюдается в водных объектах с высокими концентрациями загрязняющих органических веществ и в эвтрофированных водоемах, содержащих большое количество биогенных и гумусовых веществ.
Концентрация кислорода определяет величину окислительно-восстановительного потенциала и в значительной мере направление и скорость процессов химического и биохимического окисления органических и неорганических соединений. Кислородный режим оказывает глубокое влияние на жизнь водоема. Минимальное содержание растворенного кислорода, обеспечивающее нормальное развитие рыб, составляет около 5 мг/дм 3 . Понижение его до 2 мг/дм 3 вызывает массовую гибель (замор) рыбы. Неблагоприятно сказывается на состоянии водного населения и пересыщение воды кислородом в результате процессов фотосинтеза при недостаточно интенсивном перемешивании слоев воды.
В соответствии с требованиями к составу и свойствам воды водоемов у пунктов питьевого и санитарного водопользования содержание растворенного кислорода в пробе, отобранной до 12 часов дня, не должно быть ниже 4 мг/дм 3 в любой период года; для водоемов рыбохозяйственного назначения концентрация растворенного в воде кислорода не должна быть ниже
4 мг/дм 3 в зимний период (при ледоставе) и 6 мг/дм 3 – в летний.
Определение кислорода в поверхностных водах включено в программы наблюдений с целью оценки условий обитания гидробионтов, в том числе рыб, а также как косвенная характеристика оценки качества поверхностных вод и регулирования процесса очистки стоков (табл. 15). Содержание растворенного кислорода существенно для аэробного дыхания и является индикатором биологической активности (т.е. фотосинтеза) в водоеме.
Содержание кислорода в водоемах с различной степенью загрязненности
Уровень загрязненности воды и класс качества
источник
Требования, предъявляемые к качеству воды, могут быть самыми различными и определяются её целевым назначением. Для оценки качества пластовых, природных и сточных вод их образцы подвергают анализу. На основании результатов анализа делаются выводы о пригодности воды для конкретного вида потребления, возможности применения тех или иных методов очистки. Анализы подземных вод позволяют прогнозировать сопутствующие месторождения полезных ископаемых. При анализе вод для характеристики их свойств определяют химические, физические и бактериологические показатели. Основными показателями, определяющими пригодность воды для определенной отрасли народного хозяйства, являются химические, так как физические (содержание взвешенных частиц, температура, цвет, запах, плотность, сжимаемость, вязкость, поверхностное натяжение) и бактериологические (наличие бактерий) показатели зависят от химического состава воды.
К химическим показателям качества воды относятся:
состав растворенных газов.
Общее солесодержание характеризует присутствие в воде минеральных и органических примесей, количество этих примесей в виде общей минерализации, сухого и плотного остатков. Общая минерализация представляет собой сумму всех найденных в воде анализом катионов и анионов. Минерализацию выражают в миллиграмм-эквивалентах солей, находящихся в I л воды, или в процентах, то есть числом граммов растворенных веществ, содержащихся в 100 г раствора. Сухим остатком называется суммарное количество нелетучих веществ, присутствующих в воде во взвешенном, коллоидном и растворенном состоянии, выраженное в мг/л. Сухой остаток определяют путем выпаривания пробы воды, последующего высушивания при 105 о С и взвешивания. Плотный остаток – это сухой остаток, определенный из профильтрованной пробы воды. Следовательно, разница двух показателей соответствует содержанию взвешенных веществ пробы. Если сухой остаток прокалить при температуре 500-600 о С, то масса его уменьшится и получится остаток, называемый золой. Уменьшение массы происходит за счет сгорания органических веществ, удаления кристаллизационной воды, разложения карбонатов. Потери при прокаливании приближенно относят за счет органических примесей.
Жесткость воды обусловливается наличием в ней ионов Са 2+ и Mg 2+ . Для большинства производств жесткость воды является основным показателем её качества. В жесткой воде плохо пенится мыло. При нагревании и испарении жесткой воды образуется накипь на стенках паровых котлов, труб, теплообменных аппаратов, что ведет к перерасходу топлива, коррозии металлов и авариям.
Жесткость количественно выражается числом миллиграмм-эквивалентов ионов кальция и магния в 1 л воды (мг-экв/л); 1 мг-экв/л жесткости соответствует содержанию в воде 20,04 мг/л ионов Са 2+ или
12,16 мг/л ионов Mg 2 + . Различают жесткость общую, карбонатную и некарбонатную.
Карбонатная жесткость связана с присутствием в воде в основном гидрокарбонатов и карбонатов кальция и магния, которые при кипячении воды переходят в нерастворимые средние или основные соли и выпадают в виде плотного осадка:
Таким образом, при кипячении карбонатная жесткость устраняется. Поэтому она называется также временной жесткостью. Следует сказать, что при переходе HCO3 – в CO32 – и при выпадении карбонатов кальция и магния в воде остается некоторое количество ионов Са 2+ , Mg 2+ , CO32 – , соответствующее произведению растворимости СаСО3 и (MgOH)2CO3. В присутствии посторонних ионов растворимость этих соединений повышается.
Некарбонатная (постоянная) жесткость не разрушается кипячением. Она обусловливается присутствием в воде кальциевых и магниевых солей сильных кислот, главным образом сульфатов и хлоридов.
Общаяжесткость воды представляет собой сумму карбонатной и некарбонатной жесткости и обусловливается суммарным содержанием в воде растворенных солей кальция и магния. По величине общей жесткости принята следующая классификация природных вод:
Если известны концентрации (мг/л) в воде Ca 2+ , Mg 2+ и HCO3 – , то жесткость рассчитывается по следующим формулам:
Общая жесткость
Карбонатная жесткость равна концентрации (мг/л) [HCO3– ]; в случае, если содержание ионов кальция и магния в воде выше, чем количество гидрокарбонатов:
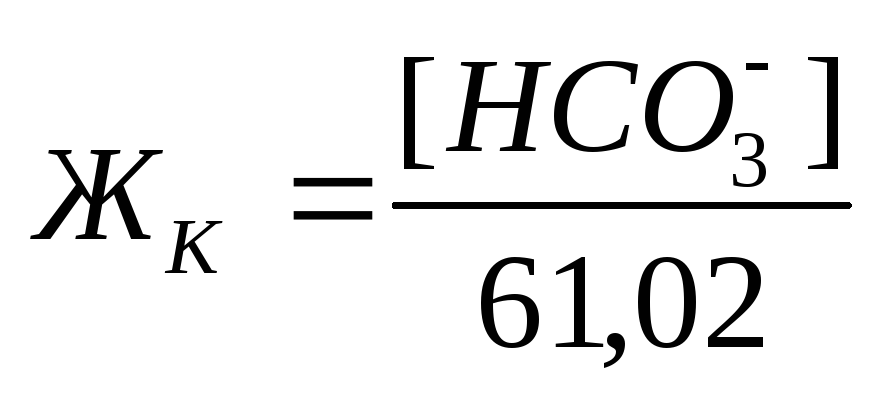
Если же количество гидрокарбонатов в воде превышает содержание ионов кальция и магния, то карбонатная жесткость соответствует общей жесткости. Разность между общей и карбонатной жесткостью составляет некарбонатную жесткость: ЖНК= ЖО– ЖК . Следовательно, ЖНК – это содержание Ca 2+ и Mg 2 + , эквивалентное концентрации всех остальных анионов, в том числе и некомпенсированных гидрокарбонатов.
Окисляемость характеризует содержание в воде восстановителей, к которым относятся органические и некоторые неорганические (сероводород, сульфиты, соединения двухвалентного железа и др.) вещества. Величина окисляемости определяется количеством затраченного окислителя и выражается числом миллиграммов кислорода, необходимого для окисления веществ, содержащихся в 1 л воды. Различают общую и частичную окисляемость. Общую окисляемость определяют обработкой воды сильным окислителем – бихроматом калия K2Cr2O7 или йодатом калия KIO3. Частичную окисляемость определяют по реакции с менее сильным окислителем – перманганатом калия КMnO4. По этой реакции окисляются только сравнительно легко окисляющиеся вещества.
Для полного окисления содержащихся в воде органических веществ, при котором происходят превращения по схеме
требуется количество кислорода (или окислителя в расчете на кислород), называемое химическим потреблением кислорода (ХПК) и выражаемое в мг/л.
При любом методе определения ХПК вместе с органическими веществами окисляются и неорганические восстановители, содержащиеся в пробе. Тогда содержание неорганических восстановителей в пробе определяют отдельно специальными методами и результаты этих определений вычитают из найденного значения ХПК.
Реакция среды характеризует степень кислотности или щелочности воды. Концентрация водородных ионов природных вод зависит главным образом от гидролиза солей, растворенных в воде, количества растворенных угольной кислоты и сероводорода, содержания различных органических кислот. Обычно для большинства природных вод величина рН изменяется в пределах 5,5-8,5. Постоянство рН природных вод обеспечивается наличием в ней буферных смесей. Изменение значения рН свидетельствует о загрязнении природной воды сточными водами.
Определение иона Cl – . В основу определения иона хлора положен аргентометрический метод Мора. Принцип анализа заключается в том, что при прибавлении к воде раствора AgNO3 образуется белый осадок хлорида серебра:
Определение хлорид-ионов ведут в интервале рН = 6,5 ÷ 10, чтобы одновременно с AgCl не выпадал осадок Ag2CO3. Проведению определения Сl – мешает наличие в воде ионов брома, йода, сероводорода, от которых освобождаются предварительной обработкой воды.
Определение иона SO42– . Метод определения сульфат-ионов основан на малой растворимости сульфата бария, количественно выпадающего в кислой среде при добавлении к воде раствора хлорида бария: Ba 2+ + SO42– = BaSO4↓
По массе образовавшегося осадка рассчитывают содержание иона SO42– .
Определение ионов CO32– и HCO3– . Эти ионы определяют титрованием пробы воды растворами серной или соляной кислот последовательно с индикаторами фенолфталеином и метилоранжем. Реакция нейтрализации протекает в две стадии.
Первые порции кислоты вступают в реакции с карбонат-ионом, образуя гидрокарбонат-ион:
Окраска фенолфталеина при рН = 8,4 переходит из розовой в бесцветную, что совпадает с таким состоянием раствора, когда в нем остаются лишь гидрокарбонаты. По количеству кислоты, пошедшей на титрование, рассчитывают содержание карбонат-иона. Расход кислот на титрование с фенолфталеином эквивалентен содержанию половины карбонатов, т.к. последние нейтрализуются только наполовину до HCO3 – . Поэтому общее количество CO32 – эквивалентно удвоенному количеству кислоты, затраченной на титрование. При дальнейшем титровании в присутствии метилоранжа происходит реакция нейтрализации гидрокарбонатов:
Метилоранж меняет окраску при pH = 4,3, т.е. в момент, когда в растворе остается только свободный диоксид углерода.
При расчете содержания ионов HCO3 – в воде следует из количества кислоты, пошедшей на титрование с метилоранжем, вычесть количество кислоты, идущей на титрование с фенолфталеином. Общее количество кислоты, затраченной на нейтрализацию ионов ОН – , СО32– и НСО3– , характеризует общую щелочность воды. Если рН воды ниже 4,3, то её щелочность равна нулю.
Определение ионов Ca 2+ , Mg 2+ . Имеется несколько методов обнаружения и определения содержания ионов Са 2+ и Mg 2+ . При добавлении в воду оксалата аммония (NH4)2C2O4 в случае присутствия ионов кальция образуется белый осадок оксалата кальция:
После отделения осадка оксалата кальция в воде можно определить ионы Mg 2+ с помощью раствора гидрофосфата натрия Na2HPO4 и аммиака. При наличии иона Mg 2 + образуется мелкокристаллический осадок соли магния:
Полученные осадки прокаливают и взвешивают. На основании полученных результатов вычисляется величина кальциевой и магниевой жесткости.
Наиболее быстрым и точным методом определения Са 2 + и Mg 2 + является комплексонометрический метод, основанный на способности двунатриевой соли этилендиаминотетрауксусной кислоты (трилон Б)
N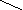
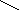
образовывать с ионами кальция и магния прочные комплексные соединения.
При титровании пробы воды трилоном Б происходит последовательное связывание в комплекс сначала ионов кальция, а затем ионов магния. Содержание ионов кальция определяют, титруя воду в присутствии индикатора — мурексида. Мурексид образует с ионами кальция малодиссоциированное комплексное соединение, окрашенное в малиновый цвет.
Ионы магния не дают комплекса с мурексидом. Трилон Б извлекает Са 2+ из его растворимого комплекса с мурексидом, вследствие чего окраска раствора, изменяется на сиреневую:
По количеству трилона Б, расходуемого на титрование, определяют содержание Са 2 + . Титрованием пробы воды трилоном Б в присутствии индикатора хромогена черного определяют суммарное содержание Са 2 + и Mg 2 + , то есть общую жесткость воды. Вода, содержащая Са 2 + и Mg 2 + , в присутствии хромогена черного окрашивается в красный цвет вследствие образования комплекса с Mg 2 + . При титровании воды в точке эквивалентности происходит изменение цвета на синий вследствие протекания следующей реакции:
Содержание Mg 2+ вычисляют по разности между общим содержанием (Са 2+ + Mg 2+ ) и содержанием Са 2 + . Трилонометрическое определение каждого иона производится при том значении рН, при котором этот ион образует с трилоном Б соединение более прочное, чем с индикатором. Для поддержания заданного значения рН к титруемому раствору добавляют буферные растворы. Кроме того, поддержание заданной величины рН обеспечивает определенную окраску индикатора. Общую жесткость воды определяют при рН > 9, кальциевую – при рН = 12.
Определение ионов Na + , K + . Производится вычислением по разности между суммой мг-экв найденных анионов и катионов, поскольку вода электронейтральна:
С достаточно высокой точностью все присутствующие в воде катионы можно определить эмиссионной спектроскопией сухого остатка.
Растворенные в воде газы определяют химическими методами или газовой хроматографией.
Определение диоксида углерода производят титрованием пробы воды щелочью в присутствии индикатора–фенолфталеина:
Определение растворенного кислорода производится йодометрическим методом.
Для анализа в пробу воды поcледовательно добавляют раствор хлорида марганца и щелочной раствор йодида калия. Метод основан на окислении свежеполученного гидроксида двухвалентного марганца содержащимся в воде кислородом:
Количество образовавшегося в воде бурого осадка гидроксида четырехвалентного марганца эквивалентно количеству растворенного кислорода. При последующем добавлении к пробе соляной или серной кислоты четырехвалентный марганец вновь восстанавливается до двухвалентного, окисляя при этом йодид калия. Это приводит к выделению свободного йода, эквивалентного содержанию четырехвалентного марганца, или, что то же самое, растворенного кислорода в пробе:
Выделившийся свободный йод определяется количественно путем титрования раствором тиосульфата натрия:
I2+ 2Na2S2O3
Йодометрический метод определения растворенного кислорода неприменим для вод, содержащих сероводород, так как сероводород вступает во взаимодействие с йодом и занижает результат. Во избежание этой ошибки предварительно связывают содержащийся в пробе сероводород в соединение, не препятствующее нормальному течению реакции. Для этой цели обычно используют хлорид ртути (II):
Определение H2S. Прежде чем приступить к количественному определению сероводорода, определяют его качественное присутствие по характерному запаху. Более объективным качественным показателем служат свинцовые индикаторные бумажки (фильтровальная бумага, пропитанная раствором ацетата свинца). При опускании в воду, содержащую сероводород, свинцовая бумага темнеет, принимая желтую (малое содержание), бурую (среднее содержание) или темно-коричневую (высокое содержание) окраску.
В водных растворах сероводород присутствует в трех формах: недиссоциированный H2S, в виде ионов HS – и S 2 – . Относительные концентрации этих форм в воде зависят от рН этой воды и в меньшей степени от температуры и общего солесодержания.
Если анализируемая вода не содержит веществ, реагирующих с иодом, то сероводород и его ионы можно определить следующим образом.
В основе количественного метода определения H2S лежит реакция окисления сероводорода йодом:
К точно отмеренному подкисленному раствору йода, взятого в избытке по отношению к ожидаемому содержанию сероводорода, прибавляют определенное количество воды. Количество йода, израсходованное на окисление сероводорода, определяется обратным титрованием остатка йода тиосульфатом. Разница между количеством раствора тиосульфата, соответствующим всему количеству взятого для анализа йода, и количеством этого же раствора, затраченного на титрование остатка йода в пробе, эквивалентна содержанию сероводорода в исследуемой пробе.
источник