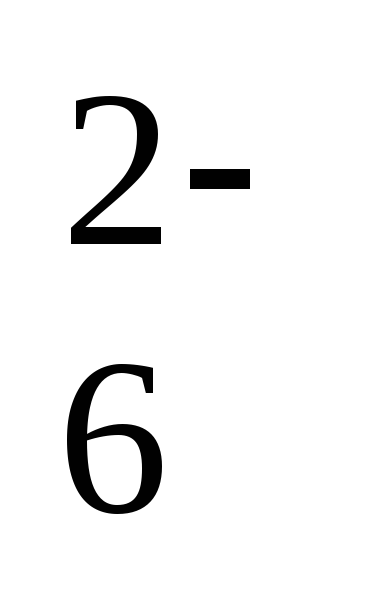В природной воде водоемов всегда присутствуют органические вещества. Их концентрации могут быть иногда очень малы (например, в родниковых и талых водах). Природными источниками органических веществ являются разрушающиеся останки организмов растительного и животного происхождения, как живших в воде, так и попавших в водоем с листвы, по воздуху, с берегов и т.п. Кроме природных, существуют также техногенные источники органических веществ: транспортные предприятия (нефтепродукты), целлюлозно-бумажные и лесоперерабатывающие комбинаты (лигнины), мясокомбинаты (белковые соединения), сельскохозяйственные и фекальные стоки и т.д. Органические загрязнения попадают в водоем разными путями, главным образом со сточными водами и дождевыми поверхностными смывами с почвы.
В естественных условиях находящиеся в воде органические вещества разрушаются бактериями, претерпевая аэробное биохимическое окисление с образованием двуокиси углерода. При этом на окисление потребляется растворенный в воде кислород. В водоемах с большим содержанием органических веществ большая часть РК потребляется на биохимическое окисление, лишая таким образом кислорода другие организмы. При этом увеличивается количество организмов, более устойчивых к низкому содержанию РК, исчезают кислородолюбивые виды и появляются виды, терпимые к дефициту кислорода. Таким образом, в процессе биохимического окисления органических веществ в воде происходит уменьшение концентрации РК, и эта убыль косвенно является мерой содержания в воде органических веществ. Соответствующий показатель качества воды, характеризующий суммарное содержание в воде органических веществ, называется биохимическим потреблением кислорода (БПК).
Определение БПК основано на измерении концентрации РК в пробе воды непосредственно после отбора, а также после инкубации пробы. Инкубацию пробы проводят без доступа воздуха в кислородной склянке (т.е. в той же посуде, где определяется значение РК) в течение времени, необходимого для протекания реакции биохимического окисления. Так как скорость биохимической реакции зависит от температуры, инкубацию проводят в режиме постоянной температуры (20±1)°С, причем от точности поддержания значения температуры зависит точность выполнения анализа на БПК. Обычно определяют БПК за 5 суток инкубации (БПК5)*, однако содержание некоторых соединений более информативно характеризуется величиной БПК за 10 суток или за период полного окисления (БПК10 или БПКполн соответственно). Погрешность в определении БПК может внести также освещение пробы, влияющее на жизнедеятельность микроорганизмов и способное в некоторых случаях вызывать фотохимическое окисление. Поэтому инкубацию пробы проводят без доступа света (в темном месте).
Величина БПК увеличивается со временем, достигая некоторого максимального значения – БПКполн, причем загрязнители различной природы могут повышать (понижать) значение БПК. Динамика биохимического потребления кислорода при окислении органических веществ в воде приведена на рис. 8.
Рис. 8. Динамика биохимического потребления кислорода:
а – легкоокисляющиеся («биологически мягкие») вещества – сахара, формальдегид, спирты, фенолы и т.п.;
в – нормально окисляющиеся вещества – нафтолы, крезолы, анионогенные ПАВ, сульфанол и т.п.;
с – тяжело окисляющиеся («биологически жесткие») вещества – неионогенные ПАВ, гидрохинон и т.п.
Таким образом, БПК – количество кислорода в миллиграммах, требуемое для окисления находящихся в 1 л воды органических веществ в аэробных условиях, без доступа света, при 20°С, за определенный период в результате протекающих в воде биохимических процессов. Ориентировочно принимают, что БПК5 составляет около 70% БПКполн, но может составлять от 10 до 90% в зависимости от окисляющегося вещества.
Особенностью биохимического окисления органических веществ в воде является сопутствующий ему процесс нитрификации, искажающий характер потребления кислорода (рис. 9).
Рис. 9. Изменение характера потребления кислорода при нитрификации.
Нитрификация протекает под воздействием особых нитрифицирующих бактерий – Nitrozomonas, Nitrobacter и др. Эти бактерии обеспечивают окисление азотсодержащих соединений, которые обычно присутствуют в загрязненных природных и некоторых сточных водах, и тем самым способствуют превращению азота сначала из аммонийной в нитритную, а затем и нитратную формы. Соответствующие процессы описываются уравнениями:
где: Q – энергия, высвобождающаяся при реакциях.
Процесс нитрификации происходит и при инкубации пробы в кислородных склянках. Количество кислорода, пошедшее на нитрификацию, может в несколько раз превышать количество кислорода, требуемое для биохимического окисления органических углеродсодержащих соединений. Начало нитрификации можно зафиксировать по минимуму на графике суточных приращений БПК за период инкубации. Нитрификация начинается приблизительно на 7-е сутки инкубации (см. рис. 9), поэтому при определении БПК за 10 и более суток необходимо вводить в пробу специальные вещества – ингибиторы, подавляющие жизнедеятельность нитрифицирующих бактерий, но не влияющие на обычную микрофлору (т.е. на бактерии – окислители органических соединений). В качестве ингибитора применяют тиомочевину (тиокарбамид), который вводят в пробу либо в разбавляющую воду в концентрации 0,5 мг/мл.
В то время как и природные, и хозяйственно-бытовые сточные воды содержат большое количество микроорганизмов, способных развиваться за счет содержащихся в воде органических веществ, многие виды промышленных сточных вод стерильны или содержат микроорганизмы, которые не способны к аэробной переработке органических веществ. Однако микробы можно адаптировать (приспособить) к присутствию различных соединений, в том числе токсичных. Поэтому при анализе таких сточных вод (для них характерно, как правило, повышенное содержание органических веществ) обычно применяют разбавление водой, насыщенной кислородом и содержащей добавки адаптированных микроорганизмов. При определении БПКполн. промышленных сточных вод предварительная адаптация микрофлоры имеет решающее значение для получения правильных результатов анализа, т.к. в состав таких вод часто входят вещества, которые сильно замедляют процесс биохимического окисления, а иногда оказывают токсическое действие на бактериальную микрофлору.
Для исследования различных промышленных сточных вод, которые трудно подвергаются биохимическому окислению, используемый метод может применяться в варианте определения полного БПК (БПКполн.).
Если в пробе очень много органических веществ, к ней добавляют разбавляющую воду. Для достижения максимальной точности анализа БПК анализируемая проба или смесь пробы с разбавляющей водой должна содержать такое количество кислорода, чтобы во время инкубационного периода произошло снижение его концентрации на 2 мг/л и более, причем остающаяся концентрация кислорода спустя 5 суток инкубации должна составлять не менее 3 мг/л. Если же содержание РК в воде недостаточно, то пробу воды предварительно аэрируют для насыщения кислородом воздуха**. Наиболее правильным (точным) считается результат такого определения, при котором израсходовано около 50% первоначально присутствующего в пробе кислорода.
В поверхностных водах величина БПК5 колеблется в пределах от 0,5 до 5,0 мг/л; она подвержена сезонным и суточным изменениям, которые, в основном, зависят от изменения температуры и от физиологической и биохимической активности микроорганизмов. Весьма значительны изменения БПК5 природных водоемов при загрязнении сточными водами.
Норматив на БПКполн. не должен превышать: для водоемов хозяйственно-питьевого водопользования – 3 мг/л, для водоемов культурно-бытового водопользования – 6 мг/л. Соответственно можно оценить предельно-допустимые значения БПК5 для тех же водоемов, равные примерно 2 мг/л и 4 мг/л.
Определение концентрации растворенного кислорода при анализе воды на БПК может выполняться различными методами. Наиболее распространен для определения РК при анализе БПК метод йодометрического титрования – метод Винклера (подробно описан в разделе «Растворенный кислород»).
Мешающее влияние на определение БПК оказывают процессы, происходящие в пробе в промежуток времени между отбором пробы и ее обработкой в лаборатории. Для исключения этого влияния начинать определение необходимо сразу же на месте отбора пробы. При этом следует соблюдать те же условия, что и при работе в лаборатории (хранение пробы в темноте, без доступа воздуха, при температуре 20°С).
Поскольку анализ на БПК связан с определением РК, мешающее влияние на результат анализа могут оказывать те же примеси, которые оказывают мешающее влияют на определение РК (взвешенные и окрашенные вещества, биологически активные взвешенные вещества, восстановители и окислители). Следует отметить, что мешающее влияние указанные компоненты оказывают, как правило, в концентрациях, встречающихся только в сточных и загрязненных поверхностных водах.
В полевом варианте предлагаемый метод определения БПК*** предусматривает определение БПК5 для относительно незагрязненных и обычно достаточно насыщенных кислородом природных поверхностных вод, поэтому аэрацию проб, добавление разбавляющей воды и введение ингибиторов нитрификации не проводится. Используемый метод применим для арбитражного анализа поверхностных и сточных вод при содержании органических веществ, соответствующем потреблению кислорода на их окисление до 6 мг/л. Однако при высоком содержании органических веществ в воде данный метод в предлагаемом, упрощенном, варианте не может дать точных результатов (весь РК расходуется еще до окончания 5-дневной инкубации), поэтому необходимо применять разбавление пробы незагрязненной аэрированной водой.
Альтернативным методом определения БПК может быть метод с электродным (потенциометрическим) измерением концентрации РК с помощью оксиметра. При этом следует иметь в виду все вышеизложенные особенности БПК как показателя качества воды, а также биохимические процессы, протекающие в пробе.
Оборудование, реактивы и принадлежности для определения растворенного кислорода методом Винклера (см. раздел «Растворенный кислород»); кислородные калиброванные склянки для инкубирования проб; чашки Петри; термостат-инкубатор, обеспечивающий поддержание температуры (20±1)°С.
1. Отберите пробы воды в кислородные склянки (не менее 3 шт.) как описано в методе определения РК.
Примечание. Для получения представительной пробы отбор проб воды проводите, по возможности, на удалении от берегов, дна, водных растений и т.п., которые могут быть источниками выделений в воду органических веществ или/и микроорганизмов.
2. В первой склянке сразу же фиксируйте кислород и определите концентрацию РК.
3. Другие склянки – инкубационные (две или больше) поместите в темноте в инкубатор через водяной затвор из чашки Петри, как показано на рисунке (это воспрепятствует контакту воды в склянке с воздухом).
Примечание. Инкубации желательно подвергнуть несколько проб, т.к. в случае получения ошибочных результатов (об этом можно судить по сходимости анализов проб, см. главу 3) выполнить анализ повторно будет уже невозможно.
4. По истечении 5 суток инкубации в склянках определите концентрацию остаточного РК как среднее арифметическое результатов по каждой инкубационной склянке.
5. Рассчитайте значение БПК5 в мг/л по формуле:
БПК5 = С1 – С2 ,
где: С1 – концентрация РК в первоначальной пробе, мг/л;
С2 – средняя концентрация РК по истечение периода инкубации, мг/л.
* Может определяться также БПК10 (за 10 суток) и БПКполн. (за 20 суток), при этом окисляется около 90 и 99% органических веществ соответственно.
** Для определения БПК необходимым фактором является не абсолютное количество РК в начале окисления, а достаточное его количество для окисления органических соединений. При этом после окисления остаточная концентрация РК в воде также должна иметь измеряемое значение.
*** Полевой вариант метода является адаптированным вариантом метода, приведенного в РД 52.24.420-95 и ИСО 5815.
источник
В природной воде водоемов всегда присутствуют органические вещества. Их концентрации могут быть иногда очень малы (например, в родниковых и талых водах). Природными источниками органических веществ являются разрушающиеся останки организмов растительного и животного происхождения, как живших в воде, так и попавших в водоем с листвы, по воздуху, с берегов и т.п. Кроме природных, существуют также техногенные источники органических веществ: транспортные предприятия (нефтепродукты), целлюлозно-бумажные и лесоперерабатывающие комбинаты (лигнины), мясокомбинаты (белковые соединения), сельскохозяйственные и фекальные стоки и т.д. Органические загрязнения попадают в водоем разными путями, главным образом со сточными водами и дождевыми поверхностными смывами с почвы. В естественных условиях находящиеся в воде органические вещества разрушаются бактериями, претерпевая аэробное биохимическое окисление с образованием двуокиси углерода. При этом на окисление потребляется растворенный в воде кислород. В водоемах с большим содержанием органических веществ большая часть РК потребляется на биохимическое окисление, лишая таким образом кислорода другие организмы. При этом увеличивается количество организмов, более устойчивых к низкому содержанию РК, исчезают кислородолюбивые виды и появляются виды, терпимые к дефициту кислорода. Таким образом, в процессе биохимического окисления органических веществ в воде происходит уменьшение концентрации РК, и эта убыль косвенно является мерой содержания в воде органических веществ. Соответствующий показатель качества воды, характеризующий суммарное содержание в воде органических веществ, называется биохимическим потреблением кислорода (БПК).
Определение БПК основано на измерении концентрации РК в пробе воды непосредственно после отбора, а также после инкубации пробы. Инкубацию пробы проводят без доступа воздуха в кислородной склянке (т.е. в той же посуде, где определяется значение РК) в течение времени, необходимого для протекания реакции биохимического окисления. Так как скорость биохимической реакции зависит от температуры, инкубацию проводят в режиме постоянной температуры (20±1)°С, причем от точности поддержания значения температуры зависит точность выполнения анализа на БПК. Обычно определяют БПК за 5 суток инкубации (БПК5), однако содержание некоторых соединений более информативно характеризуется величиной БПК за 10 суток или за период полного окисления (БПК10 или БПКполн соответственно). Погрешность в определении БПК может внести также освещение пробы, влияющее на жизнедеятельность микроорганизмов и способное в некоторых случаях вызывать фотохимическое окисление. Поэтому инкубацию пробы проводят без доступа света (в темном месте).
Таблица. Величины БПК5 в водоемах с различной степенью загрязненности
Степень загрязнения (классы водоемов)
Для водоемов, загрязненных преимущественно хозяйственно-бытовыми сточными водами, БПК5 составляет обычно около 70% БПКП.
Определение БПКп в поверхностных водах используется с целью оценки содержания биохимически окисляемых органических веществ, условий обитания гидробионтов и в качестве интегрального показателя загрязненности воды. Необходимо использовать величины БПК5 при контроле эффективности работы очистных сооружений.
В зависимости от категории водоема величина БПК5 регламентируется следующим образом: не более 3 мг О2/дм 3 для водоемов хозяйственно-питьевого водопользования и не более 6 мг О2/дм 3 для водоемов хозяйственно-бытового и культурного водопользования. Для морей (I и II категории рыбохозяйственного водопользования) пятисуточная потребность в кислороде (БПК5) при 20°С не должна превышать 2 мг О2/дм 3 .
Полным биохимическим потреблением кислорода (БПКП) считается количество кислорода, требуемое для окисления органических примесей до начала процессов нитрификации. Количество кислорода, расходуемое для окисления аммонийного азота до нитритов и нитратов, при определении БПК не учитывается. Для бытовых сточных вод (без существенной примеси производственных) определяют БПК20, считая, что эта величина близка к БПКП.
Полная биологическая потребность в кислороде БПКП для внутренних водоемов рыбохозяйственного назначения (I и II категории) при 20°С не должна превышать 3 мг О2/дм 3 .
Пробоотбор и подготовка воды к анализу
Для проведения физико-химического анализа воды необходимо правильно провести пробоотбор. В зависимости от цели исследования проба воды для анализа может быть получена несколькими способами:
путем однократного отбора всего количества воды, нужного для анализа;
смешением проб, отобранных через определенные промежутки времени в одном месте исследуемого водоема;
смешением проб, отобранных одновременно в разных местах исследуемого водоема.
При отборе проб воды используют посуду из бесцветного стекла или полиэтилена марок, разрешенных для контакта с питьевой водой. Посуда должна быть тщательно вымыта моющими средствами, многократно ополоснута водопроводной и дистиллированной водой, а непосредственно перед забором воды посуду несколько раз ополаскивают исследуемой водой. Пробки желательно использовать стеклянные или полиэтиленовые; корковые или резиновые пробки обертывают полиэтиленовой пленкой.
На практике удобно пользоваться банкой или бутылью. В местах с затрудненным доступом к воде банку или бутыль можно прикрепить к шесту. Для взятия проб с определенной глубины используются батометры (рисунок). При отсутствии данного прибора можно сделать самодельный батометр, состоящий из бутыли (1л), с прикрепленным к ней тонким прочным шнуром необходимой длины. Бутыль закрывают пробкой со шнуром и помещают в футляр, имеющий груз и петлю. К петле привязывают веревку с отметками, указывающими глубину погружения. На нужной глубине выдергивают пробку из бутыли и после наполнения емкости водой и поднимают ее.
Отбор проб воды на проточных водоемах производится в 1 км выше ближайшего по течению пункта водопользования (водозабор для питьевого водоснабжения, места купания, организованного отдыха, территория населенного пункта), а на непроточных водоемах и водохранилищах — в 1 км в обе стороны от пункта водопользования.
Обычно пробы в створе отбирают в трех точках (у обоих берегов и в фарватере); при ограниченных же технических возможностях или на не-
больших водоемах допускается отбор проб в одной-двух точках (в местах наиболее сильного течения). Чаще всего пробы отбирают в 5 — 10 м от берега на глубине 50 см. Объектом особого внимания должны стать загрязненные струи.
Если на реке имеется сброс сточных вод от промышленных предприятий, стоки животноводческих ферм и т. д., то отбор проб воды проводят ниже сброса на 500 м, что позволяет контролировать степень загрязнения воды в реке сточными водами (для сравнения следует взять пробу на 500 м выше сброса сточных вод).
Если предполагается, что в результате сброса сточных вод в придонных слоях накапливаются оседающие вредные вещества, которые могут стать источником вторичного загрязнения воды, отбирают придонные пробы на расстоянии 30 — 50 см от дна.
В водохранилищах, озерах, прудах, где течение воды резко замедленно, качество воды может быть неоднородным на различных участках (здесь возможно возникновение вторичных источников загрязнения), поэтому в этих водоемах обычно берут серию проб по глубине.
Сразу же после взятия пробы необходимо сделать запись об условиях сбора, направлении ветра, указать дату и час отбора воды.
Подготовка воды к анализу
Для получения достоверных результатов анализ следует проводить возможно быстрее. В воде происходят процессы окисления-восстановления, физико-химические, биохимические, вызванные деятельностью микроорганизмов, сорбции, десорбции, седиментации и т. д. Могут изменяться и органолептические свойства воды — запах, цвет и др. Некоторые вещества способны адсорбироваться на стенках сосудов (железо, алюминий, медь, кадмий, марганец и др.), а из стекла бутылей могут выщелачиваться микроэлементы. При невозможности исследовать воду в установленные для соответствующих показателей сроки (таблица) ее охлаждают или консервируют.
Биохимические процессы в воде можно замедлить, охладив ее до 4°С. В этих условиях медленнее разрушаются и многие органические вещества.
Универсального консервирующего средства не существует, поэтому пробы для анализа отбирают в несколько бутылей. В каждой из них на месте отбора пробу консервируют, добавляя различные реагенты (таблица). Подготовка воды непосредственно перед анализом заключается в следующем:
— консервированные пробы при необходимости нейтрализуют, а охлажденные нагревают до комнатной температуры (не на нагревательном приборе);

Находящиеся в природной и питьевой воде загрязняющие вещества имеют, как правило, очень маленькие концентрации. Для того чтобы определить присутствие этих загрязнителей следует провести концентрирование этих примесей.
Если при анализе проводилось концентрирование пробы, то при последующих расчетах необходимо учитывать объем исходного образца воды.
Метод определения концентрации РК
Определение концентрации РК в воде проводится методом Винклера, который широко используется для санитарно-химического и экологического контроля.
3.2 Метод определения концентрации РК основан на способности гидроксида марганца (II) окисляться в щелочной среде до гидроксида марганца (IV), количественно связывая при этом кислород. В кислой среде гидроксид марганца (IV) снова переходит в двухвалентное состояние, окисляя при этом эквивалентное связанному кислороду количество йода. Выделившийся йод титруют раствором тиосульфата натрия в присутствии крахмала.
Определение РК проводится в несколько этапов. Сначала в анализируемую воду добавляют соль Мn (II), который в щелочной среде реагирует с растворенным кислородом с образованием нерастворимого гидроксида Мn (IV) по уравнению:
2Мn 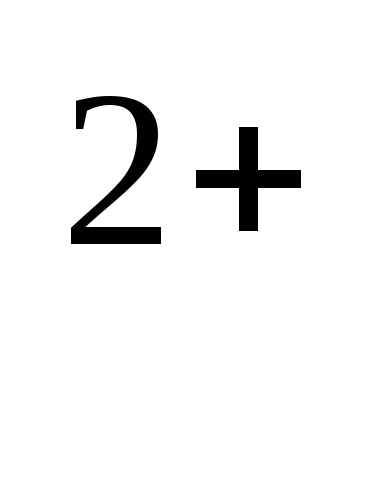



Таким образом, кислород «фиксируется» в пробе (количественно связывается). Кислород — неустойчивый компонент химического состава воды, поэтому фиксация должна быть проведена сразу после отбора пробы.
Далее к пробе добавляют раствор кислоты для растворения осадка и раствор йодида калия, в результате чего протекает химическая реакция с образованием свободного йода по уравнению:
2МnО(ОН)


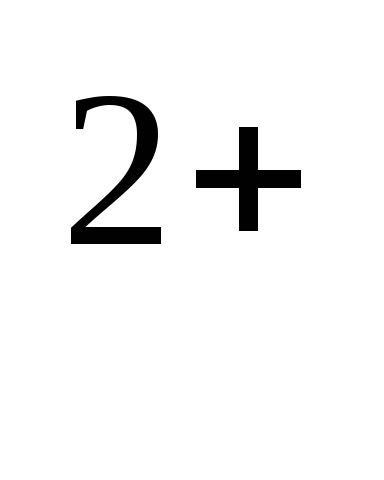


Затем свободный йод титруют раствором тиосульфата натрия в присутствии крахмала, который добавляют в качестве индикатора для определения точки эквивалентности. Реакции описываются уравнениями:
J

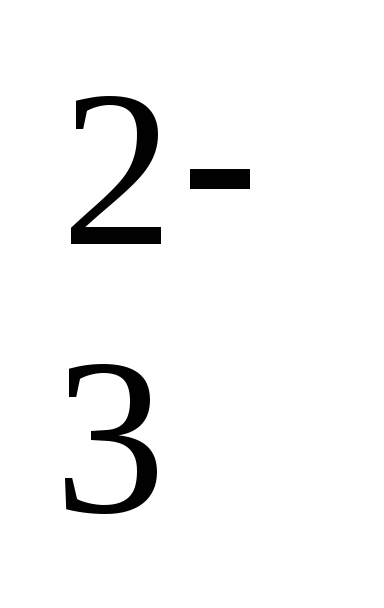


J 
В точке эквивалентности происходит обесцвечивание раствора.
3.3 По результатам титрования определяют абсолютное содержание РК в воде в мг О
Метод определения биохимического потребления кислорода основан на способности микроорганизмов потреблять растворенный кислород при биохимическом окислении органических и неорганических веществ в воде.
Биохимическое потребление кислорода определяют количеством кислорода в мг/дм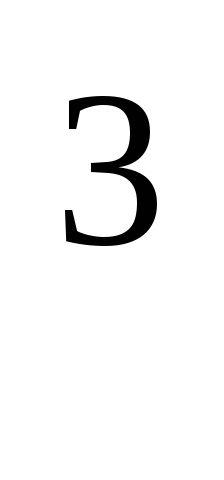
3.5 По разности содержания РК в воде до и после инкубации пробы в кислородной склянке при стандартных условиях (продолжительность инкубации — 5 суток при температуре 20±1°С без доступа света и воздуха) определяют БПК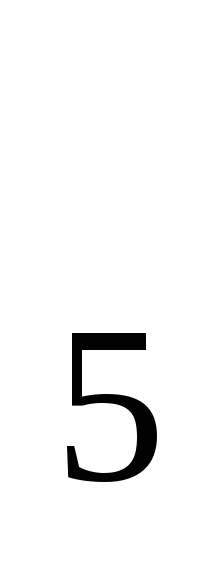
3.6 В поверхностных водах суши величина БПК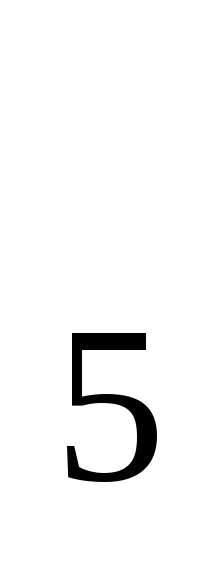

3.7 Мешающее влияние на аналитическое определение РК могут оказывать вещества (взвешенные и окрашенные, биологически активные, восстановители, реагирующие с выделившимся йодом, окислители, выделяющие йод из йодида калия) в концентрациях, встречающихся только в сточных и загрязненных поверхностных водах.
3.8 Точность выполнения анализа определяется:
качеством растворов, которое может ухудшиться при их загрязнении, хранении в негерметично закрытых склянках, в теплом месте или на свету, а также при хранении растворов слишком продолжительное время (без проведения периодического контроля);
чистотой используемой посуды для отбора проб и выполнения нализов;
полнотой учета мешающих примесей, которые могут присутствовать в анализируемой воде;
При работе с комплектом в полевых и лабораторных условиях руководствуются основными правилами техники безопасности, предусмотренными для химико-аналитических работ.
4.2 Методика выполнения анализа предусматривает использование щелочного раствора йодида калия и раствора серной кислоты. Следует избегать попадания щелочного и сернокислотного растворов на слизистые оболочки, кожные покровы, одежду, обувь, оборудование и т.п. При попадании на кожу или слизистые оболочки следует быстро и обильно промыть водой, при необходимости обратиться к специалисту в медицинское учреждение.
4.3. Едкие вещества требуют особого обращения:
хранения в специальном месте, недоступном для неспециалистов:
использования их только оператором (преподавателем);
Подготовка к проведению анализа
Подготовка к проведению анализа включает: проверку целостности мерной и др. посуды; проверку наличия растворов в склянках; приготовление растворов.
Раствор крахмала неустойчив при хранении. Для приготовления свежего — растворите содержимое капсулы в 10-15 мл холодной дистиллированной воды, полученную суспензию постепенно прилейте к 35-40 мл кипящей дистиллированной воды и кипятите 2-3 минуты. Раствор охладите.
По мере использования рабочего раствора тиосульфата натрия (0,02 моль/л экв.) приготовьте новый. Отберите мерной пипеткой 20,0 мл раствора тиосульфата натрия (0,1 моль/л экв.), поместите в мерную колбу вместимостью 100 мл, доведите объем раствора до метки дистиллированной водой, перемешайте раствор.
Оборудование и реактивы: Барометр любого типа; груша резиновая или медицинский шприц; колба коническая вместимостью 250–300 мл; склянка кислородная калиброванная (100–200 мл) с пробкой; мешалка (стеклянные шарик, палочка и т.п.) известного объема; пипетки мерные на 1 мл и 10 мл; термометр; раствор соли марганца; раствор серной кислоты (1:2); раствор тиосульфата натрия (0,02 моль/л экв.); раствор крахмала (0,5%); раствор йодида калия щелочной.
1. Добавьте в склянку с пробой анализируемой воды разными пипетками 1 мл раствора соли марганца, 1 мл раствора йодида калия, погружая пипетку с раствором в кислородную склянку на глубину 2-3 см, как показано на рисунке и по мере выливания раствора поднимайте пипетку вверх.
Излишек жидкости из склянки стечет через край на подставленную чашку Петри.
Слегка наклоните склянку, закройте пробкой. Излишек жидкости стечет через край. Следите, чтобы в склянке не осталось пузырьков воздуха.
Склянка не должна оставаться открытой.
2. Перемешайте содержимое склянки имеющейся внутри мешалкой, удерживая склянку рукой. Поместите склянку с зафиксированной пробой в темное место для отстаивания (не менее 10 минут и не более 24 часов).
Добавьте пипеткой 2 мл раствора серной кислоты.
Закройте склянку пробкой и перемешайте содержимое до полного растворения осадка.
5. Перенесите содержимое склянки в коническую колбу для титрования вместимостью 250 мл.
Примечание. Можно проводить титрование части пробы. Для этого из кислородной склянки в колбу для титрования перенесите цилиндром 50,0 мл обработанной пробы.
6. Заполните пипетку (бюретку), закрепленную в стойке-штативе раствором тиосульфата натрия (0,02 моль/л экв.) и титруйте пробу до слабо желтой окраски. Затем добавьте пипеткой 1 мл раствора крахмала (раствор в колбе синеет) и продолжайте титровать до полного обесцвечивания раствора.
7. Определите общий объем раствора тиосульфата натрия, израсходованного на титрование (как до, так и после добавления раствора крахмала).
источник
НДП 10.1:2:3.131-2016 Методика определения биохимического потребления кислорода после 5 дней инкубации (БПК5) в пробах питьевых, природных и сточных вод амперометрическим методом / 10 1 2 3 131 2016
АНАЛИТИЧЕСКИЙ ЦЕНТР ЗАО «РОСА»
Отдел физико-химических методов анализа
Сектор общего химического анализа
Генеральный директор ЗАО «РОСА»
__________________ А.В. ЧАМАЕВ
МЕТОДИКА ОПРЕДЕЛЕНИЯ
БИОХИМИЧЕСКОГО ПОТРЕБЛЕНИЯ КИСЛОРОДА
ПОСЛЕ 5 ДНЕЙ ИНКУБАЦИИ (БПК5)
В ПРОБАХ ПИТЬЕВЫХ, ПРИРОДНЫХ И СТОЧНЫХ ВОД
АМПЕРОМЕТРИЧЕСКИМ МЕТОДОМ
Сведения об организации-разработчике:
Адрес: 119297, Москва, ул. Родниковая, д. 7, стр. 35
1 Настоящее издание методики действует до выхода нового издания.
2 Разработчик оставляет за собой право вносить в методику изменения, которые не касаются принципа метода и диапазона измеряемых значений, а также процедур, которые могут оказывать влияние на значения приписанных показателей точности.
Начальник сектора общего химического анализа
Начальник отдела физико-химических методов анализа
Начальник отдела контроля качества
Настоящий нормативный документ устанавливает методику определения биохимического потребления кислорода после 5 дней инкубации (БПК5) амперометрическим методом. Методика распространяется на следующие объекты анализа: воды питьевые, воды природные пресные (поверхностные и подземные, в том числе источники водоснабжения), воды сточные (производственные, хозяйственно-бытовые, ливневые и очищенные).
Примечание — Допускается применение методики для анализа вод бассейнов и аквапарков, талых вод, технических вод и атмосферных осадков (дождь, снег, град).
Диапазон измерений массовых концентраций биохимического потребления кислорода в питьевых и природных водах от 0,5 до 1000 мг/дм 3 в пересчете на О2, в сточных водах — от 1,0 до 80000 мг/дм 3 в пересчете на О2.
Биохимическое потребление кислорода — это массовая концентрация растворенного в воде кислорода, потребленного на биохимическое окисление содержащихся в воде органических и (или) неорганических веществ за 5 суток инкубации при температуре (20 ± 1) °С без доступа воздуха и света. Этот показатель является некоторой условной мерой загрязнения вод органическими соединениями.
Для целей экологического контроля качества вод БПК определяют только в натуральной (взболтанной) пробе, чтобы учесть суммарное загрязнение находящимися в разных формах веществами. При эксплуатации очистных сооружений для оценки процесса очистки на разных ее этапах возможно определение БПК в натуральной (взболтанной), отстоянной в течение двух часов или фильтрованной пробе.
Пробы сильно загрязненной воды разбавляют специально приготовленной разбавляющей водой, содержащей неорганические питательные вещества в количестве, достаточном для нормального протекания аэробных биохимических процессов. При анализе стерильных вод, в них вносят микробную затравку.
Определению БПК мешают токсичные вещества (медь, свинец и другие тяжелые металлы, активный хлор и т.д.), которые подавляют биохимическое окисление. В таких случаях БПК можно определить после удаления из воды токсичных веществ или после соответствующего разбавления пробы, при котором устраняется действие токсинов.
При определении БПК сточных вод, обработанных веществами, содержащими активный хлор, влияние свободного или связанного хлора устраняют добавлением раствора тиосульфата натрия или выдерживают воду на свету в течение (1 — 2) часов.
Особенностью биохимического окисления органических веществ в воде является сопутствующий ему процесс нитрификации, искажающий характер потребления кислорода. Количество кислорода, пошедшее на нитрификацию, может в несколько раз превышать количество кислорода, требуемое для биохимического окисления органических соединений. Поэтому при определении БПК необходимо вводить в пробу специальные вещества — ингибиторы, подавляющие жизнедеятельность нитрифицирующих бактерий, но не влияющие на обычную микрофлору. В качестве ингибитора применяют раствор тиомочевины, который вводят в пробу либо в разбавляющую воду.
Блок-схема проведения анализа приведена в приложении А.
ГОСТ 12.0.004-90 Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения.
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования.
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности.
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание.
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков.
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия.
ГОСТ 2493-76 Реактивы. Калий фосфорнокислый двузамещенный 3-водный. Технические условия.
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия.
ГОСТ 3773-72 Реактивы. Аммоний хлористый. Технические условия.
ГОСТ 4147-74 Реактивы. Железо (III) хлорид 6-водный. Технические условия.
ГОСТ 4172-76 Реактивы. Натрий фосфорнокислый двузамещенный 12-водный. Технические условия.
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия.
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия.
ГОСТ 4460-77 Кальций хлористый. Технические условия.
ГОСТ 4523-77 Реактивы. Магний сернокислый 7-водный. Технические условия.
ГОСТ 6344-73 Реактивы. Тиомочевина. Технические условия.
ГОСТ 6709-72 Вода дистиллированная. Технические условия.
ГОСТ 17792-72 Электрод сравнения хлорсеребряный насыщенный образцовый 2-го разряда.
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия.
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры.
ГОСТ 27068-86 Реактивы. Натрий серноватистокислый (натрия тиосульфат) 5-водный. Технические условия.
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний.
ГОСТ 29169-91 Посуда лабораторная стеклянная. Пипетки с одной отметкой.
ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования.
ГОСТ 31861-2012 Вода. Общие требования к отбору проб.
ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты.
ГОСТ Р 52501-2005 Вода для лабораторного анализа. Технические условия.
ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания.
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства. измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания.
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике.
ТУ 6-09-1678-86 Фильтры обеззоленные (белая, красная, синяя ленты).
ТУ 25-11-834-73 Мешалка магнитная. Технические условия.
ТУ 6-09-1181-89 Бумага индикаторная универсальная для определения PH 1 — 10 и 7 — 14. Технические условия.
ТУ 6-09-2540-87 Стандарт-титры (фиксаналы, нормадозы).
Примечание — Если ссылочный стандарт заменен (изменен), то следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
Настоящая методика обеспечивает получение результатов измерений с погрешностью, не превышающей значений, приведенных в таблице 1.
Диапазон измерений, мг/дм 3
Показатель повторяемости
(относительное среднеквадратическое отклонение повторяемости), σ r , %
Показатель воспроизводимости
(относительное среднеквадратическое отклонение воспроизводимости), σ R , %
Показатель точности
(границы относительной погрешности при доверительной вероятности 0,95), ±δ, %
источник
Значение БПК используется для количественной характеристики присутствующих в воде биохимически разрушающихся загрязнений, разложение которых сопровождается изменением кис-. , лородного баланса водоемов. БПК.5 составляет согласно Терио для бытовых сточных вод около 70%. . от соответствующего значения ХПК, показывающего количество , кислорода, нужное для полного окисления всех органических за-. : грязнений.[ . ]
Учитывая длительность выполнения анализов по БПК (5, 10, 20 суток), для оперативного контроля и управления режимом биохимической очистки вод рекомендуется в каждом отдельном случае в условиях установившегося режима поступления и состава вод иметь график, функционально устанавливающий взаимосвязь между ХПК и БПК. Время выполнения анализа по ХПК (экспресс-методика) около 20 мин. Это позволит вовремя вносить коррективы в технологический режим и сохранить жизнеспособность биоценозов. Способность сточных вод к биохимической очистке характеризуется биохимическим показателем, т.е. отношением БПКп /ХПК.[ . ]
Количество органических веществ, выраженное в величинах БПК.5 в различных дисперсных фракциях городской сточной жидкости, показано в табл. 11.[ . ]
Если на высоконагружаемый фильтр сточная жидкость подается с БПК 5 нач, а уходит после прохождения фильтра и вторичного отстойника с БПК5кои, при суточном слое нагрузки на биофильтр Л м (это все равно, что м;3/м2 сутки ), то Мй,(-=БПК5нач Л, а М Мвн-ЪПК5конХ ХЛ = Л(БПК5ка„-БПК5кок).[ . ]
Для очистки сточных вод, содержащих органические соединения с БПК = 5-ч-Ю г/л, применяется анаэробный биохимический процесс в метантенках. Процесс наиболее полно протекает при 45—55°С без доступа воздуха (термофильное сбраживание). Часто метантенки используют для обработки осадков из первичных и вторичных отстойников, после чего осадки легко фильтруются, отделяются и обезвреживаются. В результате распада органических соединений образуются метан, углекислый газ, водород, азот, сероводород, которые сжигают с использованием теплоты отходящих газов для обогрева метантенков.[ . ]
Количество взвешенных веществ, поступающих на фильтры, обычно составляет 10—12,5 мг/л при БПК 5,8—6,8 мг/л. Фильтрат содержит 1,3—2,9 мг/л взвешенных веществ, БПК при этом снижается до 2 мг/л. Таким образом, содержание взвешенных веществ при фильтровании снижается на 70—90%, а БПК на 65—75%.[ . ]
Подробного рассмотрения требует биохимическая потребность сточных вод в кислороде БПК.5. Это объясняется не только тем; что БПК5 сточных вод является одним из показателей, который непосредственно используется для расчетов по спуску сточных вод в водоемы, но и трудностью правильного определения этого показателя. Определение БПКб сточной жидкости сопряжено с большими ошибками, которые чаще всего объясняются специфичностью производственных сточных вод, содержащих наряду с органическими веществами, легко окисляющимися биохимически (т. е. при участии микрофлоры воды), также бактерицидные вещества, которые в малых концентрациях могут тормозить процесс биохимического окисления органических веществ сточных вод. Так, органические ¡кислоты (муравьиная, уксусная, молочная и др.), гликоли, ацетон, метанол и др. окисляются в воде, повышая величину биохимического потребления кислорода БПК5, а соединения меди, никеля, кадмия, цинка, кобальта и другие ингредиенты производственных сточных вод уже в малых концентрациях способны тормозить биохимическое потребление кислорода.[ . ]
Рассмотрим пример, помещенный на яомопрамме в виде пунктирных линий. При пятисуточной БПК— 5 = 56,24 мг/л и константе скорости ¡потребления кислорода /0=0,04 ¡полная БПК будет равна 153 мг/л.[ . ]
Иногда для количественной оценки органических веществ подземных вод используется метод БПК-5 (биохимического потребления кислорода после 5-суточного хранения пробы воды). При этом окисление органических веществ происходит под действием микроорганизмов. Значения ХПК и БПК-5 могут быть близкими в случае, если в воде присутствуют биохимически легко окисляющиеся органические вещества (при этом ХПК = = 1,4 БПК).[ . ]
Содержание органических веществ в воде и сточных водах можно определить косвенным методом по показателям БПК.5, БПКполн, а также ХПК. Значения этих показателей учитываются при расчете нагрузки на сооружения биологической очистки сточных вод, выборе конструкции биоокислителей и проверке правильности анализа сточных вод [41, 66]. По разнице между ХПК и БПКполн определяют в сточных водах и воде содержание трудноокисляемых органических веществ и рассчитывают необходимую конструкцию сооружений с более интенсивной биологической очисткой. Описан метод непрерывного автоматического определения органических веществ в воде и сточных водах; одновременно определялись также БПКэ и ХПК сточных вод [108, 115].[ . ]
Расплывающиеся на воздухе кристаллы с запахом аммиака; М 105,14; т. пл. 28 °С; т. кип. 268 °С; хорошо растворим в воде; БПК.5 0,1; ХПК 1,06.[ . ]
В состав очистных сооружгний поселка Лоза Загорского района входят два высоконагружаемых биофильтра диаметром 15 м, высотой 3,5 м, загруженных щебнем крупностью 40—60 мм. Сточная вода распределяется в биофильтре с помощью реактивного оросителя. Воздух подается двумя вентиляторами ЭВР-4. Гидравлическая нагрузка составляет около 10 м3/(м2-сутки), количество подаваемого воздуха — 12 м3 на 1 м3 воды. На очистные сооружения поступают производственные сточные воды в количестве 1000 м3/сутки и бытовые сточные воды жилого поселка в количестве 500 м3/сутки. БПК.5 поступающих сточных вод составляет примерно 80—130 мг/л, а БПК5 очищенных сточных вод — 4— 16 мг/л.[ . ]
Работа преаэраторов оценивается в комплексе с первичными отстойниками по степени задержания взвешенных веществ и снижению БПК.5. Эффект работы преаэраторов зависит от концентрации сточной воды, количества подаваемого активного ила и конструкции первичного отстойника. Эффект от преаэрации повышается с увеличением концентрации сточных вод.[ . ]
Сточные воды заводов безалкогольных напитков характеризуются нейтральной активной реакцией (pH =7), они содержат 200 мг/л взвешенных веществ; БПК.5 этих стоков составляет 400 мг/л.[ . ]
По оси абсцисс отложены пятисуточные БПК ( 5). лежащие в пределах 1—1200 мг/л. По линии ординат отложены пол ные БПКо от 2,5 до 2000 мг/л. Прямыми, имеющими подъема слева направо, ¡показаны константы скорости ¡потребления кисло рода в пределах от 0,01 до 0,4.[ . ]
Пусть известно, что промежуток времени между протеканием воды от пункта А до ¡пункта Б равен ¿=14,1 суток, константа скорости (потребления кислорода К1 =0,04 и начальная БПК в точке А равна 5,0 мг/л. Восстанавливаем в точке ¿=14,1 перпендикуляр до встречи с кривой, для которой АТ, =0,04. Из точки пересечения этих двух линий ¡проводим горизонталь до встречи с наклонной, для которой БПК=5,0 мг/л. Из точки пересечения этих двух линий опускаем перпендикуляр на верхнюю горизонталь, которая даст БПК=1,33 мгЦл.[ . ]
Перегрузка первичных отстойников и сокращение времени отстаивания до 1 ч приводит к тому, что в отстойнике задерживается всего 25—30% взвешенных веществ и около 10—15% БПК.5. Следовательно, основная доля по .переработке загрязнений падает на аэротенки, нагрузка ¡на активный ил увеличивается до 460— 500 мг/г ила. Такой активный ил обычно вспухает, особенно в летний период, иловой индекс повышается до 200—300 мл/г. В условиях повышения илового индекса приходится снижать дозу ила в аэротенках, так как не справляются с работой вторичные отстойники, снижение дозы ила увеличивает и без того высокую нагрузку на ил. Приходится увеличивать расход воздуха (до 80— 100 м3 на кг БПКб). Одновременно увеличивается прирост активного ила (он достигает 15—20 т на 100 тыс. м3 сточных вод), что приводит к нарушению работы илоуплотнителей и всей цепочки сооружений по обработке осадка.[ . ]
Кроме основных элементов состава клетки (С, N. О, Н) для ее построения необходимы в незначительном количестве и другие компоненты. Так, потребность клетки в марганце составляет 10-10-5 мг на 1 мг снятой БПК.5, меди— 14,6 -10—5, цинке— 16-10-5, молибдене — 43-10 5, селене — 14-10 10, магнии — 30-Ю-4, кобальте — 13-10 5, кальции 62-10-4, натрии — 5-10-5, калии — 45-10— , железе —12-10-3, карбонат-ионе — 27-. 10-4. Содержание указанных элементов в природных водах, из которых затем образуются сточные, обычно достаточно, чтобы полностью удовлетворить требованиям бактериального метаболизма. Часто не хватает азота и фосфора и их добавляют искусственно в виде суперфосфата, ортофосфорной кислоты, аммофоса, сульфата, нитрата или хлорида аммония, мочевины и т. п.[ . ]
Мей (May, 1954) в статье «Очистка сточных вод нефтеперерабатывающих заводов на опытных биофильтрах» пишет, что очистке подвергались сточные воды, содержащие 42—8Ш мг/л нефтепродуктов с БПК 50—650 мг/л при отсутствии сульфидов. Установка включала коагуляторы, первичные отстойники, биофильтры, вторичные отстойники. В качестве коагулянта использовался сернокислый алюминий (35—40 мг/л) и активированная Si02 (5—6 мг/л). В результате коагуляции БПК снижалось на 33%, содержание нефтепродуктов —■ на 9—86%. Нагрузка на биофильтры по БПК.5 менялась от 148 до 444 г в сутки на 1 м3 загрузки биофильтров. В результате фильтрования БПК5 снижалось до 15— 20 мг/л. После биофильтров рекомендуется сточные воды накоплять в прудах в течение 60 суток, а перед выпуском в водоем пропускать их через микропроцеживатели.[ . ]
Подсчитать, как изменится нагрузка Н на ил, если изменить процент регенерации с 25 на 50% при продолжительности аэрации £ = 6,8 ч, дозе ила в собственно аэротенке ал= 1,4 г/л, в регенераторе яр = 5,6 г/л, зольности ила 3.1 = 28%- БПК.5 воды, поступающей в аэротенк, равна 120 мг/л.[ . ]
Реагенты (сернокислый алюминий и известь) дозируются в сточную воду перед аэрируемыми песколовками в количестве, обеспечивающем снижение концентрации фосфора при отстаивании до 1—2 мг/л. Одновременно в процессе отстаивания снижается БПК.5 на 60—65 % и концентрация взвешенных веществ на 80—90 %. При такой высокой степени извлечения загрязнений на стадии механической очистки продолжительность аэрации может быть значительно сокращена.[ . ]
Опыты по очистке сточных вод предприятий вискозного штапеля хлорированным сернокислым железом производил Моттл [8; 9]. Результаты опытов показали, что по сравнению с обычным отстаиванием пр.и использовании этого способа очистки окисляемость снижается на 31,7%, а БПК.5 — на 39,9%. Оптимальная доза реагента— 100—400 мг/л pH — 6,65—11,8; продолжительность отстаивания — 2 часа.[ . ]
Существенным источником жировых отходов служат мясокомбинаты. Их сточные воды по степени загрязнения в 2-10 раз превышают коммунальные и содержат большое количество белков, жиров, протеинов, спиртов, жирных кислот, что предопределяет значительные величины ХПК и БПК. Так, например, Московский мясокомбинат имеет стоки следующего состава, мг/л: жиры до 2300, белки до 2000, взвешенные вещества до 3000, БПК.5 до 1500, ХПК до 8800 (по кислороду).[ . ]
В настоящее время за рубежом находят все более широкое распространение предельно допустимые концентрации вредных химических веществ в воде водоемов и другие стандарты качества воды. В Англии установлены следующие контрольные показатели для качества воды источников бытового водопользования: БПК.5 меньше 4 мг/л, ХПК менее 25 мг/л. Для источников рыбохозяйственного значения эти показатели выше: БПКб от 10 до 4 мг/л, ХПК от 40 до 25 мг/л. В Англии установлены так называемые рабочие нормативы для сточных вод на основе расчетов, обеспечивающих требуемое качество воды в водоеме (1951).[ . ]
Дефицчт воды во многих районах стимулирует применение очищенных городских сточных вод для водоснабжения промышленных предприятий. Для доведения качества очищенных сточных вод до нормы, требуемой при использовании их в промышленном водоснабжении, необходимо производить их доочистку на фильтрах и обеззараживание. Рекомендуется применение скорых песчаных фильтров, позволяющих снизить содержание взвешенных веществ и БПК.5 до 5 мг/л, а также хлорирование (дозы хлора 5—10 мг/л). Доочищенные сточные воды не должны вызывать повышенного биологического обрастания [76]. Опыт использования очищенных городских сточных вод для водоснабжения промышленных предприятий подтверждает перспективность этогб мероприятия.[ . ]
Качество применяемых коагулянтов, т. е. содержание активных веществ в хлорном железе и гашеной извести, определяют не реже раза в неделю и в каждой новой порции перед ее использованием. Степень коагуляции осадка проверяют не реже раза в неделю, обязательно при использовании новой партии коагулянтов и при пуске сооружений в работу после остановки. Не реже раза в декаду анализируют фильтрат (пробы среднесуточные), определяют pH, взвешенные вещества, БПК.5 и плотный остаток.[ . ]
На кафедре канализации МИИГС (С. В. Яковлевым) вместе с сотрудниками Щукинской очистной станции (П. И. Галаниным и А. Н. Дубовой) исследовалась работа биокоагулятора, в который подавалась’биопленка из вторичных отстойников после биофильтров.[ . ]
В водохранилищах водораздельного бьефа, вследствие отстойного эффекта, в среднем на 10% снижается цветность вода; большинство же показателей качества воды сохраняется на том же уровне, что и в Иваньковском водохранилище. Ниже плотины, на участке длиной 80 км, канал не принимает сточных вод. Водотоки, пересекающие трассу канала, пропущены под ним дюкерами или отведены в другие бассейны. Далее на участке длиной 20 км расположены водохранилища водораздельного бьефа — Икшинское и Песшвское, которые имеют небольшие водосборы и пренебрежимо малые источники загрязнений. Качество воды в этих водохранилищах определяется качеством исходной воды Иваньковского водохранилища и внутриводными процессами. Пяловское и Клязьминское водохранилища имеют относительно большие водосборы и получают большие объемы загрязнений. Особое место занимает Учинское водохранилище, имеющее наименьшую водосборную площадь и наибольший объем при большой глубине. По данным Союзгипроводхоза [3] вода по каналу до Пестова (90 км) проходит в течение 4 сут, по Пестовскому и Икшинскому водохранилищам 10 сут. Коэффициенты самоочищения при температуре воды 19°С характеризуются так: БПК-5 — 0,0072; нефтепродукты — 0,0044; цветность — 0,014.[ . ]
источник
Вода незагрязненных водоемов в зависимости от температуры (от 30ºС до 0 ºС) содержит 8-14 мг/л кислорода в насыщенном состоянии при атмосферном давлении. Поступающие в водоем вместе со сточными водами бактерии и некоторые химические вещества потребляют для своего окисления растворенный в воде кислород, понижая тем самым содержание его в воде.
При очень низком содержании кислорода жизнедеятельность в водоеме затухает, интенсивность процессов самоочищения снижается, а иногда и почти прекращается. Процесс окисления поступающих в водоем вместе со сточными водами веществ может быть разделен на три стадии, характеризующиеся определенной последовательностью расходования кислорода.
Вначале идет процесс химического окисления легко и трудно окисляющихся соединений, затем биохимическое окисление органических веществ, и, наконец, нитрификация азотсодержащих веществ с образованием солей азотной кислоты.
Если первая стадия (чисто химическое потребление кислорода) не длительна, то вторая (биохимическое окисление), в зависимости от температуры сточной воды и концентрации органических веществ — длится несколько суток. Процесс нитрификации может происходить более продолжительное время (до 40 – 50 суток).
Практическое значение имеет вторая фаза окисления сточных вод, протекающая при участии микроорганизмов в присутствии растворенного в воде свободного кислорода, в результате которой сточная вода приобретает способность не загнивать.
Под влиянием микроорганизмов органическое вещество сточных вод постепенно минерализуется, требуя для своего окисления все меньше кислорода (происходит распад органического вещества).
БПК сточных вод при этом постепенно уменьшается до момента полной минерализации, когда кислород уже не расходуется.
Биохимическое потребление кислорода (БПК) определяется количеством кислорода в мг/л, которое требуется для окисления находящихся в воде органических веществ, что устанавливается по разности в содержании кислорода в момент взятия пробы и спустя определенное время, например 5 суток (БПК ).
При относительно сильном загрязнении воды открытых водоемов может оказаться, что спустя 5 суток в ней совсем не окажется кислорода. Поэтому анализ начинают с того, что исследуемую воду предварительно взбалтывают в продолжении 1 мин в присутствии воздуха для насыщения ее кислородом. Потом определяют растворенный кислород в одной части ее пробы сразу же после взбалтывания, а в другой – спустя 5 суток выстаивания в темном месте при t = 18 – 20ºС.
Полное окисление происходит где-то за 20 суток, но для практических целей обычно определяют БПК через 5 суток и только для более полной качественной характеристики сточной воды в ней определяют БПК и БПК .
Растворенный в воде кислород находят по методу Винклера. Принцип данного метода основан на том, что гидроокись двухвалентного марганца MnO (белый осадок) поглощает свободный кислород, образуя двуокись марганца MnO (бурый осадок).
Осадок растворяют в соляной кислоте. При этом выделяется йод в количестве, эквивалентном содержанию в воде растворенного кислорода. Выделившийся йод оттитровывается раствором гипосульфита (тиосульфата натрия) в присутствии крахмала:
2MnCl + O + 4NaOH = 2MnO + 4NaCl + 2H O;
MnO + 2KI + 4HCl = MnCl + I + 2KCl + 2H O;
I + 2Na S O = Na S O + 2NaI
Цель анализа – провести оценку качества сточной воды по результатам ее анализов на БПК.
Принцип метода анализа основан на определении убыли растворенного в воде кислорода за определенное время (5 или 20 суток).
— раствор хлористого марганца: 50 г MnCl растворяют в 100 см 3 дистиллированной воды;
— смесь едкого натрия и йодистого калия: 32 г х.ч. гидроокиси натрия растворяют в 100 см 3 воды и затем прибавляют 2 г йодистого калия.
Раствор, подкисленный соляной или серной кислотами, не должен давать синей окраски с крахмалом;
— 0,02 н. раствор тиосульфата натрия (титр устанавливают по бихромату калия);
— склянка с притертой пробкой вместимостью 250 см 3 ;
Ход определения
Две одинаковые склянки с притертыми пробками вместимостью 250 см 3 заполняют испытуемой водой и закрывают пробками так, чтобы под ними не было ни одного пузырька воздуха.
В одной пробе содержание кислорода определяют сразу, в другой — через 5 суток. Причем пробу хранят в темноте при комнатной температуре.
В склянку сразу после взятия анализируемой на содержание кислорода пробы, сразу после взятия пробы, вводят пипеткой 1 см 3 раствора хлористого марганца и 3 – 4 см 3 щелочного раствора йодистого калия.
При этом пипетку опускают до дна склянки и постепенно поднимают по мере вытекания из нее реактива. Затем склянку тут же осторожно закрывают пробкой. При этом часть жидкости, эквивалентная объему введенных растворов реактивов, вытесняется. Содержимое склянки перемешивают, переворачивая ее не менее 15 раз. После 10 – минутного отстаивания, когда жидкость над осадком просветлеет, образовавшийся осадок гидроокиси марганца растворяют добавлением 1 см 3 концентрированной серной кислоты. Для полного растворения осадка склянку встряхивают. Затем из нее отбирают в коническую колбу адекватную часть жидкости, равную точно 200 см 3 раствора, и титруют выделившийся йод 0,02 н. раствором тиосульфата натрия. К концу титрования, когда раствор приобретает бледно – желтый цвет, в него добавляют 0,5%-ный раствор крахмала и продолжают титрование до его обесцвечивания.
Формула для определения содержания кислорода в воде (в мг на 1л) имеет вид
,
где О — концентрация кислорода в воде, мг/ дм 3 ;
А — количество 0,02 н. раствора тиосульфата натрия, затраченного на титрование, см 3 ;
К – поправочный коэффициент тиосульфата натрия;
V — объем воды, взятый из склянки для титрования, см 3 .
Содержание кислорода в другой склянке, хранившейся в течение 5 суток (или другое время), устанавливают подобным же способом.
Формула для расчета БПК имеет вид
,
где Х – искомое БПК , мг/ дм 3 О ;
А — содержание растворенного кислорода в воде до инкубации, мг/ дм 3 ;
А — содержание растворенного кислорода в воде после инкубации, мг/ дм 3 .
источник