Определение жесткости воды в современном мире – это обязательное условие для обеспечения работоспособности всей техники, работающей с ней. Тем не менее нельзя сказать, что такая жидкость действительно вредна для человека. Всего должно быть в меру, ведь излишне мягкая вода наносит не меньше ущерба здоровью, чем жесткая.
Начинать всегда следует с самых азов, чтобы было полное понимание проблемы. В нашем случае, прежде чем приступать к определению жесткости воды, сначала нужно понять, что она собой представляет. По результатам экспертизы, проведенной в 2011 на кафедре химии и экологии Новгородского университета им. Ярослава Мудрого, для природной натуральной воды жесткость является абсолютно нормальным явлением. Вплоть до момента появления современной техники этот вопрос вообще мало кого интересовал, тысячелетиями люди спокойно употребляли ее в том виде, в котором она есть. Придают воде жесткость растворенные в ней соли магния и кальция. Само понятие жесткости возникло по результатам ощущения людей, так как когда насыщенная этими солями и другими элементами вода вступает во взаимодействие с мылом, пена практически не образуется, затрудняя стирку или мытье.
Прежде чем понять, какую воду пить, следует учитывать тот факт, что жесткость не является однородной величиной. Есть как минимум две основные разновидности:
Зависят эти виды от типа растворенных солей, которые в любой жесткой воде присутствуют всегда вместе, составляя общую жесткость. Тем не менее разделять их можно и нужно. Временная жесткость напрямую зависит от наличия бикарбонатных и гидрокарбонатных анионов. Главная их особенность – разложение во время кипячения. В результате распада получается непосредственно сама вода, углекислый газ и карбонат кальция, который уже практически не растворяется. Получается, что от временной жесткости можно без особых проблем избавиться при помощи простого поднятия температуры воды до +100 градусов. В качестве примера можно привести любой чайник. После продолжительного использования можно обнаружить внутри осадок, который и является результатом описанного выше процесса распада. Все же, что не разлагается подобным образом, относится к постоянной жесткости, избавиться от которой без специальной обработки практически невозможно.
Это необходимо для того, чтобы понимать, какую воду пить можно без опаски, а также для того, чтобы любая техника, взаимодействующая с водой, не вышла из строя. Для человека излишне жесткая вода вредна. Но даже если этот параметр будет находиться на приемлемом для нашего организма уровне, все равно оборудование это не устроит. Аквариумы, кофейные, стиральные и посудомоечные машины, чайники, мультиварки и множество других вариантов техники требует воду строго определенной жесткости. Обычно справиться с этим помогают фильтры типа «Гейзер-3», однако зачастую такая мера может даже считаться излишней. Прежде чем тратить на них деньги, рекомендуется сначала провести тест на жесткость воды, ведь вполне возможно, что этот показатель и так на нормальном уровне.
Как уже было сказано выше, в первую очередь ущерб человеку наносит не какой-то определенный тип воды, а полное отсутствие баланса в организме.
- Плохое растворение пищевых продуктов (связано с катионами Ca 2 + и Mg 2 +).
- Кофе, чай и любые другие подобные напитки завариваются очень плохо.
- При длительном употреблении возможно расслабление желудка.
- Жесткая вода может стать причиной образования камней в почках.
- Насыщает организм требуемыми ему элементами.
- Улучшает состояние зубов, уменьшает вероятность возникновения кариеса.
- Жесткая вода является причиной поломки большинства видов техники.
- Выводит шлаки, но попутно вымывает полезные элементы (калий, магний и кальций). В результате кости становятся более хрупкими. Также не лучшим образом воздействует на сердечно-сосудистую систему.
- Негативно воздействует на гипофиз-адреналиновую систему.
- Оказывает плохое влияние на водно-солевой баланс организма.
Таким образом, определение жесткости воды должно производится не с целью избавиться от нее, а для того, чтобы свести негативное воздействие к минимуму и привести употребление такой жидкости к требуемому организмом балансу.
Согласно ГОСТу, питьевая вода должна проверяться на жесткость строго в лаборатории, посредством титриметрического анализа. Для этого сначала необходимо взять пробы, объем которых должен быть не менее 400 кубических сантиметров (0,4 литра). В качестве емкости, в которой будет производиться хранение, может использоваться любая тара, если она изготовлена из стекла или полимерного материала. Очень важно провести анализ не позднее чем через 24 часа после отбора пробы. В особых случаях, когда необходимо увеличить этот срок, производится подкисление жидкости посредством добавления соляной кислоты. В таком состоянии она может храниться уже около 1 месяца.
Среди всех методов определения жесткости воды данный вариант заслуженно считается самым достоверным и комплексным. В его основе лежит процесс образования соединений трилона вместе со щелочноземельными элементами ионов. Минимальный показатель жесткости, который поддается определению при помощи этого способа, – 0,1 о Ж (нормой считается 7-10 о Ж). В качестве пробы может быть использована обычная вода из-под крана. Лучшим выходом в ситуации с подозрением на повышенную жесткость является сразу же посетить соответствующую лабораторию, так как никакие домашние методы не смогут выдать точные данные. Но о них — ниже.
Полностью описывать весь процесс нет никакого смысла, так как воспроизвести его самостоятельно, без нужных навыков и химических элементов и оборудования невозможно. Тем не менее можно выделить несколько основных принципов реакции, которые сохраняются в любой ситуации и присущи абсолютно всем вариантам:
- Всегда должен быть способ, позволяющий зафиксировать эквивалентность реакции, которая и является основой для определения жесткости.
- Анализ проводится очень быстро.
- Должно выполняться требование стехиометричности процесса. Проще говоря, это значит, что в процессе проведения реакции не должны образовываться никакие побочные продукты.
- С момента начала реакции ее невозможно повернуть вспять или остановить.
Для определения жесткости воды в домашних условиях можно использовать специальные приспособления, купить которые не составит особого труда (они не запрещены и общедоступны). Выглядят они как стандартные тестовые полоски. Для использования достаточно погрузить одну из них в воду, требующую проверки, на указанный в инструкции период времени. В результате изделие изменит свой цвет. При использовании таких полосок для определения жесткости воды главной проблемой является определить, каков именно показатель жесткости. Чтобы это сделать, нужно сравнивать цвет на полосе и примеры с описанием на упаковке. К сожалению, далеко не всегда можно сразу же понять, что именно показывает приспособление, и даже в более четкой ситуации точность данных оставляет желать лучшего. В целом такие тест-полоски подходят только для общего понимания того, насколько жесткая или мягкая вода.
Проверить воду из-под крана на жесткость также можно при помощи подручных средств. Правда, это скорее занимательный опыт для детей, чем действительно вариант тестирования показаний жидкости.
- Банку емкостью 1 литр (или любую другую подобную емкость).
- Стакан в форме цилиндра.
- Любые весы (удобнее всего использовать электронные).
- Линейку.
- Мыло хозяйственное (72% или 60%).
- Дистиллированную воду.
Для проверки необходимо взять 1 грамм мыла, измельчить его и поместить в стакан. После этого следует подогреть дистиллированную воду, но не доводить до кипения. Ее следует налить в тот стакан, в котором уже лежит мыло. В итоге оно обязано растворится в воде. Следующий шаг – налить еще больше воды. После этого следует налить в банку обычной воды из-под крана и медленно вылить мыльную жидкость из стакана и перемешать (медленно). Если образуется пена, то это — показатель жесткости. К сожалению, более или менее четко сказать, каков именно ее уровень, при помощи такого метода практически невозможно.
Еще один вариант определения жесткости питьевой воды – воспользоваться специальным прибором – TDS-метром. В принципе, он предназначен для определения электропроводимости воды, на что влияют как непосредственно соли (создающие жесткость), так и множество других элементов, что не дает нужного уровня точности. Более того, показания прибора обычный человек, не умеющий их считывать, не поймет и скорее всего запутается. Попробуем упростить задачу. Подавляющее большинство таких устройств в качестве единиц измерения используется некие ppm. У нас же применяются другие варианты, основанные на эквиваленте миллиграмма на литр жидкости. В среднем, 1 наша единица (мг-экв/л) равняется 50,05 зарубежным ppm. По правилам, концентрация солей (т.е. жесткости) должна быть не более 350 ppm или же 7 мг-экв/л. На эти цифры и стоит ориентироваться. Если же прибор будет отечественным, все значительно облегчается. Хуже всего, когда подобное приспособление произведено где-то в Китае или другой подобной стране, где используются собственные единицы измерения. Тогда придется самостоятельно искать их эквивалент и переводить в привычные нам показания.
Из других приборов, способных определять жесткость воды, отдельно следует отметить уникальное устройство АКМС-1. Это достаточно большой стационарный агрегат, сходный по размерам с фильтрами «Гейзер-3». Просто так в домашних условиях с его помощью проверять жидкость не представляется возможным. Именно поэтому такие приспособления используются в первую очередь на производстве, где жесткость воды может повлиять на работу дорогостоящей техники или нанести другой подобный вред. В отличие от всех остальных аналогов, АКМС-1 действительно быстро и точно показывает текущий уровень жесткости, позволяя оператору своевременно реагировать. При помощи этого приспособления можно как пускать воду к рабочим агрегатам напрямую, если она не представляет для них угрозы, так и предварительно ее фильтровать. Это, конечно же, выльется в дополнительные затраты, но зато поможет сэкономить на ремонте техники, который обойдется значительно дороже.
Учитывая все указанное выше и требования ГОСТ, вода питьевая должна регулярно проверяться на уровень жесткости. Тем не менее принимать радикальные меры по ее умягчению не стоит, так как вредны оба состояния – слишком жесткая и слишком мягкая. Только в той ситуации, когда показатели действительно выше или ниже, стоит предпринимать какие-то действия. К слову, если с жесткостью регулярно борются, то про слишком мягкую воду практически не слышно, а ведь на это также нужно обращать не меньше внимания.
источник
Метод определения общей жесткости воды основан на том, что ионы кальция и магния связываются трилоном Б в комплексные соединения. О конце реакции судят по изменению цвета индикатора хромогена черного от розово-малинового до синевато-серого. Появление синевато-серого окрашивания свидетельствует об отсутствии ионов Са 2+ и Mg 2+ в растворе, т. е. о полном связывании их с трилоном Б.
В коническую колбу вместимостью 250 мл отмеривают 100 мл исследуемой воды, добавляют 5 мл аммиачного буферного раствора, индикатор хромоген (сухую смесь) и медленно титруют 0,1 н раствором трилона Б до перехода окраски в серовато-синюю.
Общую жесткость воды Жо, ммоль экв/л, вычисляют по формуле
где V1 – объем 0,1 н раствора трилона Б, израсходованный на титрование пробы, мл; К – коэффициент нормальности раствора трилона Б (К = Nфакт / 0,1); N1 – нормальность раствора трилона Б; V2 – объем исследуемой пробы воды, мл.
Определение карбонатной жесткости воды
Оттитровывают 100 мл воды 0,1 н раствором HCl в присутствии метилового оранжевого до перехода окраски от желтой к розовой. Карбонатную жесткость Жк, ммоль экв/л, вычисляют по формуле
где V3 – объем HCl, который пошел на титрование, мл; N2 – нормальность HCl, моль/л; V2 – объем воды, который взят для анализа, мл.
Некарбонатная жесткость определяется как разница между общей и карбонатной жесткостью
Определение количества диоксида углерода
В колбу поместите 200 мл исследуемой воды, добавьте 2 капли раствора фенолфталеина и взболтайте. Если вода окрасилась в интенсивный розовый цвет, это значит, что в ней нет растворенного диоксида углерода. Отсутствие окраски или очень слабая окраска свидетельствуют о присутствии растворенного диоксида углерода. В этом случае пробу титруют 0,1 н раствором NaOH до появления интенсивной окраски. Концентрацию диоксида углерода определяют по формуле
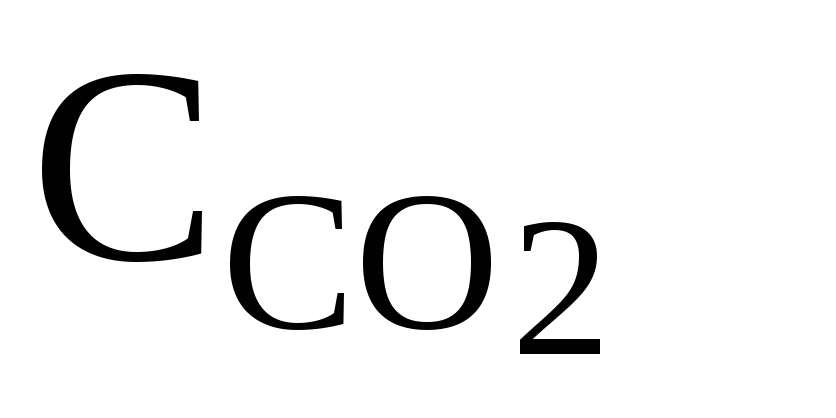
где N – нормальность NаОН, моль/л; V4 – его объем, мл.
Определение концентрации кальция и магния
К 100 мл воды добавляют 3 мл 10%-ного КОН до рН = 10–12, вносят примерно 0,2 г сухого индикатора мурексида, смешанного с сульфатом калия, и титруют трилоном Б до перехода окраски из розовой в фиолетовую.
Концентрацию кальция СК, ммоль экв/л, рассчитывают по формуле
где V5 – объем трилона Б, пошедший на титрование, мл.
Концентрацию магния См, ммоль экв/л, рассчитывают по формуле
После проведения полного обессоливания воды необходимо убедится в отсутствии в ней как катионов (Mg 2+ , Ca 2+ ), так и анионов (SO4 2– , NO3 – , Cl – ). Анализ на содержание указанных анионов в воде до ее обессоливания и после проводится качественно.
SO4 2– – раствор хлорида бария дает белый осадок сульфата бария;
Cl – – при добавлении раствора нитрата серебра образуется белый осадок хлорида серебра;
NO3 – – при добавлении раствора дифениламина в серной кислоте появляется характерное для ионов NO3 – синее окрашивание.
Определение содержания взвешенных частиц (мутность воды)
Мутность воды определяется фотоколориметрическим методом при длине волны 440 нм. Оптическую плотность измеряют в кюветах с толщиной поглощающего слоя 3 мм. Количество взвешенных частиц в воде находят по калибровочной кривой.
Регистрирующим прибором в фотоколориметре служит микроамперметр типа М907, оцифрованный в микроамперах и имеющий шкалу 0–100 делений, соответствующих шкале коэффициентов пропускания – и оптической плотности – D. При измерении со светофильтром 440 нм, отмеченным на лицевой панели колориметра черным цветом, ручку «Чувствительность» устанавливают в одно из положений 1, 2 или 3. Рабочие поверхности кювет перед каждым измерением необходимо тщательно протирать спирто-эфирной смесью, жидкость в кюветы наливать до метки на боковой поверхности кюветы. При установке кювет в кюветодержатель нельзя касаться пальцами участков поверхности кювет ниже уровня жидкости в них.
Колориметр включают в сеть за 15 мин до начала измерений. Во время прогрева кюветное отделение должно быть открыто (при этом шторка перед фотоприемником перекрывает световой пучок). В световой пучок помещают кювету со стандартным раствором, по отношению к которому производят измерения, и крышку кюветного отделения закрывают. Ручками «Чувствительность» и «Установка 100» устанавливают отсчет 100 по шкале колориметра. Затем поворотом ручки кювету со стандартным раствором заменяют кюветой с исследуемым раствором. После этого производят отсчет по шкале колориметра, соответствующий коэффициенту пропускания исследуемого раствора в процентах, или по шкале D в единицах оптической плотности. Измерения проводят 3–5 раз и окончательное значение измеряемой величины определяют как среднее арифметическое полученных значений.
источник
Прежде чем устанавливать требования к оборудованию, надо определить параметры типовых задач. В этом обзоре речь идет о большой концентрации в исходной жидкости солей. Но надо точнее установить опасный уровень.
Жесткость 7 мг-экв/литр ощущается на вкус. Наверное, по этой причине установлены нормы отечественных стандартов. Но их нельзя применять одинаково по отношению ко всем пользователям. Правильные рекомендации способен дать опытный врач после медицинского обследования. Но можно отметить, что при гипертонии и почечных заболеваниях лучше исключить употребление воды с большим содержанием минералов. В США применят разные нормы в различных штатах. Однако уровень от 4 мг-экв/литр определен, как «повышенная жесткость».
Следует отметить, что выше шла речь о возможном негативном влиянии на организм человека. Но техника подвергается опасности при концентрации солей от 0,1 мг. Профильные специалисты рекомендуют снижать ее до минимально возможных значений. В области контакта с нагревательными элементами стиральных машин теплообменников котлов отопления процесс образовании накипи отличается высокой интенсивностью. После определения необходимых параметров на выходе, следует внимательно изучить состав исходной жидкости. Здесь сделать правильные выводы не просто. В проточной воде (река, ручей) жесткость не велика.
Однако открытые водоемы ничем не защищены от загрязненной окружающей среды. Сюда попадают отходы производства и сельскохозяйственные удобрения, аллергены и опасные для жизни химические соединения. Пользуясь такими источниками придется устанавливать фильтр для умягчения воды, а также многоступенчатые системы предварительной очистки, что значительно увеличит общую стоимость проекта. Стоит помнить о возможном существенном увеличении жесткости (в несколько раз) при сильных ливнях, в периоды весенних паводков и зимних оттепелей.
В муниципальных системах водоснабжения применяют действующие нормы. Как отмечено выше, они определяют чрезмерно большую допустимую концентрацию солей жесткости. Также надо отметить плохое состояние отечественных инженерных сетей, что повышает вероятность попадания в жидкость опасных и вредных примесей в ходе транспортировки.
На фото электромагнитный фильтр (умягчитель воды) АкваЩит
По этим причинам многие пользователи, владельцы загородных земельных участков, предпочитают подключение к собственным (коллективным) артезианским скважинам. На большой глубине состав примесей отличается стабильностью. Здесь нет органических составляющих, которые очень трудно удалять в процессе очистки. Но именно тут достаточно часто присутствуют горные породы, насыщенные кальциевыми и магниевыми солями. По этой причине фильтры для очистки жесткой воды Гейзер, Аквафор или Барьер включают в состав комплекта оборудования.
Чтобы уточнить содержание примесей, во всех случаях можно применить химический и бактериологический анализ. В торговой сети предлагают специализированные экспресс-тесты. Но в профильной лаборатории проще получить более точные результаты по широкому перечню проверяемых параметров. При изучении различных комплектов оборудования необходимо учитывать не только приведенные факты, но и условия реальной эксплуатации.
Явным преимуществом этой технологии является ее целевое назначение. Фильтр Гейзер и Барьер был создан специально для решения задач по снижению жесткости из скважины. Потому можно рассчитывать на хорошие потребительские характеристики. Из конкретных преимуществ следует отметить следующие позиции:
- Установки данной категории выпускают в широком ассортименте. Не сложно подобрать комплект для небольшой городской квартиры или крупного многоэтажного дома.
- При правильном определении параметров, одним набором можно обеспечить защиту всего объекта недвижимости в целом.
- Регулярные рабочие операции выполняются под управлением автоматики.
- В некоторых современных моделях фильтров для воды из скважины электроника контролирует важные параметры, отключает технику при появлении опасных режимов, предотвращает аварийные ситуации.
- Допустима оперативная настройка с учетом изменения жесткости, расхода.
- Основная загрузка при правильной эксплуатации сохраняет свои полезные свойства более 8 лет.
- Расходные регенерационные материалы стоят недорого.
Для объективности анализа ниже приведены детали, которые способны вызвать затруднения и дополнительные расходы:
- Компактные аппараты лучшего фильтра для жесткой воды «кабинетного» типа недостаточно производительны даже для маленькой семьи.
- Для размещения крупных комплектов необходим соответствующий свободный объем. Как правило, используют отдельные помещения, чтобы изолировать шумы в ходе регенерационных процессов.
- В такой технической комнате в частном доме надо поддерживать определенный производителем режим температуры и влажности. Сюда надо подвести электропитание, водопровод, канализацию.
- Чтобы предотвратить преждевременный выход из строя стиральной машины, приходится устанавливать систему предварительной очистки от механических и других вредных примесей. Для этого хорошо было бы прочитать отзывы на форумах, чтобы составить свой рейтинг фильтров.
- Монтаж и наладка отличаются сложностью, т.к. ставятся на трубу. Исключить ошибки можно, обратившись к профильным специалистам.
- Дополнительную настройку в ходе эксплуатации надо делать самому (с помощью опытного мастера). Современный уровень развития технологий не позволяет автоматизировать соответствующие процессы без чрезмерных затрат.
- Вода на выходе из скважины из-за солей натрия приобретает насыщенный горький привкус.
- Лучший фильтр для жесткой воды под мойку способен снижать жесткость до уровня 0,1-0,5 мг-экв/литр. Допустима максимальная концентрация солей на входе от 12 до 16 мг-экв/литр (в зависимости от состава набора, марки ионообменной засыпки). При этом, какой лучше выбрать и купить, проточный фильтр или под мойку решать только вам.
Надо отдельно отметить общую сложность конструкции. Здесь есть электронные и поплавковые датчики, движущиеся узлы, электромеханические клапаны. Все это повышает вероятность поломок, снижает общий уровень надежности. Чтобы сохранить подачу воды при ремонте, опытные специалисты рекомендуют монтаж обходного трубопровода с запорной арматурой. По сравнению с другими вариантами такой комплект отличается высокой стоимостью.
Этот магистральный фильтр под мойку для жесткой воды обеспечивает высокий уровень очистки. Мембраны не пропускают крупные молекулярные соединения. Такую технологию можно было бы назвать идеальным решением. Но правда ли она лучше и ее стоить выбрать? Но надо учитывать следующие негативные факторы:
- Аппараты обратного осмоса способны выполнять свои функции длительное время, если исходная жесткость не более 5-6 мг-экв/литр.
- Производительность стандартных бытовых моделей фильтров под мойку для жесткой воды ограничена десятками литров воды в сутки. Такого объема недостаточно для удовлетворения технических, санитарных и гигиенических потребностей в квартиру.
- Чтобы увеличить мощность, применят несколько мембран параллельно. Соответствующие конструкци получаются слишком дорогими. Их приходится оснащать насосным оборудованием, дополнительными системами контроля.
Для уменьшения концентрации вредных солей, перед лучшим фильтром под мойку для жесткой воды устанавливают картриджи с катионитами. Но такие изделия отличаются небольшой эффективностью, непродолжительным сроком службы. Поэтому для вас вопрос какой лучше выбрать может быть сложным и не всегда оправданным. При частых заменах следует рассчитывать на существенные траты.
Вместо картриджей со смолами в частном доме применяют стационарные установки, рассмотренные выше. Они обеспечивают общую защиту объекта от накипи, снижают уровень жесткости. Для подготовки питьевой воды используют фильтр обратного осмоса Аквафор.
Вместо задержания и удаления солей жесткости можно изменить вредные свойства. Главной проблемой является образование накипи, которая быстро способна вывести из строя качественную стиральную машину, иное дорогое оборудование. Данная технология решает задачу с применением особых химических соединений, полифосфатов.
Соответствующие средства выпускают в форме крупных кристаллов. Их засыпают в небольшую емкость, которая устанавливается на трубу в частном доме или квартире в разрез подающей трубы перед техникой (стиральной машиной, бойлером, котлом и т.д.). Растворенные полифосфаты образуют пленку на микроскопических частицах солей жесткости, чем блокируют процесс образования накипи.
Такой способ сохраняет эффективность при небольшом расстоянии до объекта защиты (десятки сантиметров). Зная какой лучше выбрать и какой фильтр лучше купить, можно случайно купить контрафактную продукцию. Его применяют при исходной жесткости из скважины до 10-12 мг-экв/литр. Полифосфаты активизируют рост водорослей. Их надо устранить из воды для питья. При попадании на кожные покровы и слизистые оболочки они могут провоцировать аллергические реакции, раздражение тканей.
Этот проточный фильтр для очистки жесткой воды стоит недорого. Они вполне пригодны для решения локальных задач. Необходимо только обеспечить тщательный контроль и своевременное пополнение засыпки. Даже однократный рабочий цикл без соответствующей защиты сделает поверхность ТЭНа шероховатой, что ускорит нарастание на нем пористого слоя из карбонатов.
Данная технология подобна рассмотренному выше «химическому» способу. Однако она не загрязняет воду примесями. Следующие преимущества и особенности конструкции также заслуживают упоминания:
- Способность выполнять свои функции полноценно при обработке воды с жесткостью до 21 мг-экв/литр.
- Большая дальность действия – до 2 км по длине трубопровода от места монтажа магистрального фильтра для очень жесткой воды.
- Автоматизированная настройка работы.
- Компактность и небольшой вес.
- Отсутствие сложных механических узлов и движущихся частей.
- Размещение компонентов установки вне потока жидкости.
Единственным недостатком устройств этого класса является необходимость постоянного подключения к электросети. Самым экономным пользователям следует изучить возможности новых моделей проточных фильтров. При сохранении высокой эффективности они потребляют от 5 до 20 Вт за час.
Необходимо помнить, что такое оборудование не выполняет функции классического фильтра для очень жесткой воды из скважины. Дополнительную обработку жидкости применяют по мере необходимости. Для задержания вредных примесей применяют проточные наборы из картриджей, установки обратного осмоса.
источник
Как выполняется контроль жёсткости воды. Понятие жёсткости, от чего она зависит. Анализ воды на жёсткость дома. Лабораторные методы контроля общей и временной жёсткости жидкости. Приборы для выполнения анализа. Методы борьбы с повышенной жёсткостью в быту. Контроль жёсткость воды или анализ воды на жёсткость нужен для определения концентрации солей в жидкости. Этот анализ можно проводить в лабораторных условиях и дома.
Жёсткость воды – термин, говорящий о процентном соотношении солевых частиц магния и калия в жидкости. Она подразделяется на две разновидности:
- Временная (такая жидкость называется карбонатная);
- Общая жёсткость (данная вода относится к некарбонатной).
Первый тип жёсткости характеризуется присутствием гидрокарбонатных солевых частиц магния и калия. Если такую воду закипятить, то элементы распадутся на карбонаты и гидроксиды и выпадут в осадок. Именно этот белый налёт часто покрывает наши чайники изнутри и собирается на других нагревательных элементах.
Для жидкости с общей жёсткостью характерно наличие других химических элементов (различных нитратов, хлоридов и тп.п). Обычно жёсткость питьевой воды связана с особенностями вашего региона, составом грунтов. Чем больше известковых пород находится в почве, тем выше жёсткость воды. Но важно не только понимать суть понятия, но и знать, как проверить жёсткость воды. Выполнить это легко как в быту, так и на заводе.
Для проверки жёсткости водопроводной воды дома можно использовать следующие способы:
- Постарайтесь обильно вспенить мыльный брусок или порошок для стирки. Если у вас образуется мало пены, то ваша вода имеет повышенную жёсткость. Это возникает по той причине, что солевые частицы калия и магния не позволяют мылу пениться. При обильной пышной пене от любого моющего средства можно утверждать, что вода нежёсткая. Но этот метод не позволят точно определить степень жёсткости.
- На вкус также можно отличить жёсткую воду от мягкой. Она более горькая. Но не все могут точно уловить горьковатый привкус солей магния и калия.
- Белый осадок в чайниках, накипь на нагревательных элементах других бытовых приборов – признак жёсткой воды. Осадок возникает из-за распада солей и выпадения их на дно. Данная особенность жёсткой воды очень вредит бытовым приборам и отопительному трубопроводу.
- От жёсткости воды зависит скорость заваривания чайного напитка. При мягкой воде на эту процедуру уйдёт от 3 до 6 мин., в жёсткой воде чай будет завариваться от 8 до 12 мин. Кстати, на вкус оба напитка будут существенно отличаться.
- Благодаря нехитрому компактному измерительному прибору можно очень легко определить жёсткость любой жидкости. Он называется TDS-метр. Агрегат измерят электропроводность жидкости. Чем выше показатель, тем больше уровень солесодержания жидкости. Обычно его ещё называют солемер. Чаще такой анализ воды на жёсткость делают владельцы аквариумов и цветоводы.
- Проверить жёсткость воды в быту можно, используя тест-полоски, продающейся в аптеках медтехники.
Для этого анализа можно использовать колориметрическую методику и принцип титрования. Процедура анализа выполняется так: порция воды смешивается с метилоранжем (индикатором), ёмкость устанавливается на светлом фоне. Во вторую тару с водой добавляют соляную кислоту, пока не получится красно-оранжевый цвет воды.
Временную жёсткость жидкости находят в процессе расчёта требуемого количества соляной кислоты по формуле: Нвр = NHCl * VHCL* 1000/ V1, где N-насыщенность раствора, V-его количество, V1-количество пробы.
Этот анализ проводят в лаборатории. Для него используют комплексонометрическую методику. Она базируется на принципе возникновения соединений ионов, подвергающихся анализу, с природными реагентами. Сначала воду в пробирке разводят раствором индикатора на спирту (чёрного этиохрома «Т»). Также для этих целей может использоваться сухая смесь кальциевых и натриевых хлоридов. В итоге полученная смесь окрашивается в насыщенный рубиновый цвет. Затем в пробирку капается вещество, называемое Трилон.
Расчёт общей жёсткости производится по уравнению: Жо=Nx*Vx*1000/V1, где N-насыщенность вещества Трилон, V-его количество, V1-количество пробы.
Как мы уже говорили выше, прибор контроля жёсткости воды называется солемер или TDS-метр. Точность проверки составляет 2%. Основной принцип работы данного агрегата построен на зависимости электропроводности жидкости от общего числа примесей солей магния и калия. То есть чем больше данных солей в воде, тем больше будут показания прибора, а следовательно, тем выше жёсткость воды.
На некоторых предприятиях и заводах наблюдается прямая зависимость между жёсткостью используемой воды и исправностью работы оборудования. Поэтому для обеспечения бесперебойной работы технологического оборудования требуется осуществлять постоянный автоматический контроль жёсткости воды.
Для этих целей используется специальное оборудование, например, анализатор «АКМС-1». Этот прибор непрерывно контролирует содержание солевых частиц кальция и магния в жидкости, поступающей в технологическое оборудование. То есть он подсчитывает общую жёсткость в пределах 0,005-25,0 мг-экв/л.
Как понять, что ваша водопроводная вода жёсткая, мы писали выше. Теперь перечислим ряд мер, позволяющих снизить жёсткость воды в домашних условиях:
- Самый простой способ – кипячение воды.
- Фильтрация воды через системы обратного осмоса (специальные мембраны).
- Использование смягчающих солей.
- Применение фильтрующих картриджей.
- Магнитное фильтрующее устройство.
- Использование ионообменной смолы в комплексе с солевым раствором.
Хотите провести контроль жёсткости воды? Заказать такую услугу вы можете у наших специалистов, для этого вам достаточно связаться с нами по указанным телефонам.
источник
Чтобы выразить жесткость воды в цифрах, указывают концентрацию в ней ионов кальция и магния. Международная система единиц рекомендует измерять жесткость в молях на кубический метр, но на практике применяют более удобные единицы.
В России для измерения жесткости используются градусы жесткости и миллиграмм-эквиваленты на литр (мг-экв/л).
Чтобы выразить жесткость воды в цифрах, указывают концентрацию в ней ионов кальция и магния. Международная система единиц рекомендует измерять жесткость в молях на кубический метр, но на практике применяют более удобные единицы.
В России для измерения жесткости используются градусы жесткости и миллиграмм-эквиваленты на литр (мг-экв/л).
По действующему ГОСТу 31865-2012 единицей измерения жесткости воды является градус — °Ж. 1°Ж = 1 мг-экв/л. Для сравнения 1°Ж (Россия) = 2,8 dH (Германия).
По величине данного показателя вода делится на 3 категории:
По действующему ГОСТу 31865-2012 единицей измерения жесткости воды является градус — °Ж. 1°Ж = 1 мг-экв/л. Для сравнения 1°Ж (Россия) = 2,8 dH (Германия).
По величине данного показателя вода делится на 3 категории:
По санитарным правилам и нормам ( СанПиН 2.1.4.1074–01 ) жесткость питьевой воды из централизованного источника водоснабжения не должна превышать 7 мг-экв/л (в отдельных случаях 10 мг-экв/л).
На практике даже «средняя» жесткость вызывает заметный дискомфорт. Уже 4–5 °Ж дадут о себе знать: оставят накипь в чайнике и плёнку на самом чае, известковый налет на мойке и белые разводы на посуде, «забьют» аэратор водопроводного крана и лейку душа.
По санитарным правилам и нормам ( СанПиН 2.1.4.1074–01 ) жесткость питьевой воды из централизованного источника водоснабжения не должна превышать 7 мг-экв/л (в отдельных случаях 10 мг-экв/л).
На практике даже «средняя» жесткость вызывает заметный дискомфорт. Уже 4–5 °Ж дадут о себе знать: оставят накипь в чайнике и плёнку на самом чае, известковый налет на мойке и белые разводы на посуде, «забьют» аэратор водопроводного крана и лейку душа.
Вариант «Точно»:
Самый точный метод определить жесткость воды — сдать ее на анализ в лабораторию. Например, в Санэпидемстанцию. СЭС проверит не только концентрацию солей жесткости, но и зафиксирует нитраты, пестициды, уровень содержания железа, сероводород, органические примеси и другие вещества, которые часто встречаются в грунтовых водах. Если вы подбираете систему водоочистки для коттеджа, вам обязательно нужно сделать анализ воды.
Вариант «Точно»:
Самый точный метод определить жесткость воды — сдать ее на анализ в лабораторию. Например, в Санэпидемстанцию. СЭС проверит не только концентрацию солей жесткости, но и зафиксирует нитраты, пестициды, уровень содержания железа, сероводород, органические примеси и другие вещества, которые часто встречаются в грунтовых водах. Если вы подбираете систему водоочистки для коттеджа, вам обязательно нужно сделать анализ воды.
Вариант «Быстро»:
Использовать тест-полоски для определения жесткости воды. Они продаются в зоомагазине или в магазине с кофе-машинами, иногда — в фирменных магазинах бытовой техники. Такой тест покажет примерную жесткость. На бумагу нанесен реагент, который при контакте с водой меняет окрас. Полоска опускается на время в воду, и интенсивность ее окраса будет меняться в зависимости от концентрации вещества в воде.
Основные недостатки такого метода: низкая точность и то, что интерпретировать результат теста бывает сложно. Придется сначала на глаз определить интенсивность окраса, сравнив с «палитрой» возможных результатов. А затем указанные на палитре численные значения жесткости переводить из европейских градусов в российские. Качественные тест-полоски обычно зарубежного производства.
источник
МУНИЦИПАЛЬНЫЙ ЭТАП ВСЕРОССИЙСКОГО ДЕТСКОГО КОНКУРСА НАУЧНО-ИССЛЕДОВАТЕЛЬСКИХ И ТВОРЧЕСКИХ РАБОТ
Устранение жесткости воды с помощью бытовых фильтров
7 класса МБОУ «СОШ №12 с УИОП»
г. Старый Оскол, Белгородской области
учитель физики, учитель биологии
г. Старый Оскол, Белгородской области
Брызгунова Ирина Николаевна
Сотникова Валентина Анатольевна
школа № 12 с углубленным изучением
отдельных предметов», г.Старый Оскол
Основными проблемами экологии, которые связаны с гидросферой планеты, являются условия обеспечения населения водой, ее качество и возможности ее повышения. До недавних пор эти проблемы не стояли так остро, в связи с относительной чистотой природных источников водоснабжения и их достаточным количеством. Но в последние годы ситуация резко изменилась. Значительная концентрация городского населения, резкое увеличение промышленных, сельскохозяйственных, транспортных, энергетических и других антропогенных выбросов привели к нарушению качества воды, появлению в источниках водоснабжения отличных от естественной природной среды химических, радиоактивных и биологических агентов.
Все это ставит проблему эффективного водообеспечения качественной водой населения на первое место среди остальных проблем.
Показатели качества воды подразделяются на:
физические (температура, цветность, запах, вкус и др.);
химические (жесткость, щелочность, активная реакция, окисляемость, сухой остаток и др.);
биологические и бактериологические (общее количество бактерий, коли-индекс и др.).
Но наиболее важным качеством питьевой воды является её жесткость. Воду называют жёсткой, если в ней содержится большое количество растворенных солей кальция и магния.
Так как проблема жесткости воды очень значима в наши дни, мы решили посветить наш проект именно этому вопросу — жёсткость воды и способы её устранения с помощью бытовых фильтров.
Поступающая в потребление жесткая вода, не прошедшая через фильтр смягчения, обладает горьковатым вкусом и оказывает негативное воздействие на организм человека. Кроме того, соли жесткости откладываются на поверхности сантехники, накапливаются в виде накипи на нагревательных элементах бытовых приборов, в системах отопления и водоснабжения жилищ.
В этом и проявляется актуальность выбранной нами темы, ведь именно бытовые фильтры необходимы для снижения содержания солей жесткости (кальция, магния) в домашних условиях.
Так проблема жесткости значима в наши дни, мы поставили перед собой цель удостовериться в том, что бытовые фильтры способны участвовать в смягчении питьевой воды.
Для достижения поставленной цели нам необходимо решить ряд конкретных задач :
изучить и проанализировать литературу по данной теме;
провести опыты, доказывающие, что бытовые фильтры способны смягчать воду;
сделать соответствующие выводы (удостоверить в том, что производители бытовых фильтров указывают верную информацию о своем продукте).
Объекты исследования стали:
вода после фильтра БАРЬЕР «Классик»;
вода после фильтра БАРЬЕР «Жесткость».
Вода (оксид водорода) — бинарное неорганическое соединение, химическая формула Н 2 O. Молекула воды состоит из двух атомов водорода и одного — кислорода, которые соединены между собой ковалентной связью.
При нормальных условиях представляет собой прозрачную жидкость, не имеет цвета (в малом объёме), запаха и вкуса. В твёрдом состоянии называется льдом (кристаллы льда могут образовывать снег или иней), а в газообразном — водяным паром.
Около 71 % поверхности Земли покрыто водой (океаны, моря, озёра, реки, льды) — 361,13 млн км. На Земле примерно 96,5 % воды приходится на океаны, 1,7 % мировых запасов составляют грунтовые воды, ещё 1,7 % — ледники и ледяные шапки Антарктиды и Гренландии, небольшая часть находится в реках, озёрах и болотах, и 0,001 % в облаках (образуются из взвешенных в воздухе частиц льда и жидкой воды).
Бо́льшая часть земной воды — солёная, непригодная для сельского хозяйства и питья. Доля пресной составляет около 2,5 %, причём 98,8 % этой воды находится в ледниках и грунтовых водах. Менее 0,3 % всей пресной воды содержится в реках, озёрах и атмосфере, и ещё меньшее количество (0,003 %) находится в живых организмах.
Является хорошим сильнополярным растворителем. В природных условиях всегда содержит растворённые вещества ( соли , газы).
Вода – это универсальный растворитель . Если этой уникальной жидкости предоставить достаточно времени, она растворит любое твердое вещество. На это не способно ни одно вещество в природе. Именно из-за данного свойства химически чистая вода (не содержащая примесей в принципе) – лишь теория, пока не доступная практике.
Вода – участница химических реакций . Например, благодаря ней в организме животных расщепляются белки, углеводы, жиры, и выделяется энергия, которая дает нам всем возможность жить. При фотосинтезе благодаря активному участию воды выделяется кислород, который необходим всем существам на земле.
Вода – это терморегуляция . Как бы это ни было удивительно, именно вода отвечает за поддержание постоянной температуры тела. Благодаря ней тепло равномерно распределяется по организму, температура не изменяется постоянно в зависимости от условий окружающей среды.
Вода – это уникальный транспорт . Благодаря удивительной жидкости растения и животные могут успешно насыщаться питательными веществами. Вода является одним из основных компонентов лимфы и крови, играет невероятно важную роль в работе выделительной системы. С помощью этой безликой жидкости к верхушкам растений поступают минеральные соли.
Вода – это упругость клеток и организмов . Как всем известно, воду в жидком состоянии практически нельзя сжать. Благодаря этому она часто выступает скелетом клетки и, как следствие, поддерживает форму органов. Вот, к примеру, самый обычный лист вашего комнатного растения. Он поддерживает постоянную форму исключительно благодаря удивительным возможностям воды.
Методы очистки воды — способы отделения воды от нежелательных примесей и элементов.
Существуют несколько методов очистки и все они входят в три группы методов:
физико-химические ( Физико-химическая очистка применяется для очистки сточных вод от грубо- и мелкодисперсионных частиц, коллоидных примесей, растворенных соединений. Высокопроизводительный, но в то же время дорогой способ очистки.)
биологические ( Биологические методы применяются для очистки от растворенных органических соединений. Метод основан на способности микроорганизмов разлагать растворенные органические соединения.)
Наиболее дешевая — механическая очистка — применяется для выделения взвесей.
Основные методы: процеживание, отстаивание и фильтрование. Применяются, как предварительные этапы.
Фильтрование — процесс разделения неоднородных систем при помощи пористых перегородок, пропускающих дисперсионную среду и задерживающих дисперсную твёрдую фазу.
Фильтр для воды — устройство для очистки воды от механических, нерастворимых частиц, примесей, хлора и его производных, а также от вирусов, бактерий, тяжелых металлов.
Бытовые фильтры, используемые для получения питьевой воды условно можно разделить на 3 категории — простейшие бытовые фильтры, средней степени очистки и бытовые фильтры высшей степени очистки. К лучшей (высшей) степени очистки относится очистка обратноосмотическими бытовыми фильтрами — наиболее качественная и передовая технология на сегодняшний день. К простейшим относятся кувшины и насадки.
Из-за важности воды, «как источника жизни», её нередко подразделяют на типы по различным принципам.
Мягкая вода и жёсткая вода — по содержанию катионов кальция и магния. Вода с большим содержанием солей называется жёсткой , с малым содержанием — мягкой.
Жесткость — это совокупность физико-химических свойств воды, которые зависят от содержания в ней так называемых «солей жесткости», т. е. растворенных солей щелочноземельных металлов – в основном, кальция и магния.
Различают два типа жесткости: временная (карбонатная), обусловленная присутствием гидрокарбонатных анионов, и постоянная (некарбонатная), обусловленная присутствием сульфатных, нитратных и хлоридных анионов. Общая величина жесткости определяется как сумма карбонатной и некарбонатной жесткости.
Принята следующая классификация воды:
● средней жесткости – 3,0-6,0 мг-экв/л;
● мягкая – 3,0 мг-экв/л и менее.
Для определения качества требующей умягчения воды и последующего подбора фильтров умягчителей берется в расчет показатель общей жесткости.
Причинами повышенной жесткости воды, требующей умягчения с помощью специального фильтра, обычно являются растворение и выветривание горных пород, попадающих в подземные воды. Это могут быть залежи известняков, гипса или доломитов.
Поступающая в коттедж жесткая вода, не прошедшая через фильтр смягчения, обладает горьковатым вкусом и оказывает негативное воздействие на организм человека. Кроме того, соли жесткости откладываются на поверхности сантехники, накапливаются в виде накипи на нагревательных элементах бытовых приборов, в системах отопления и водоснабжения коттеджа и т.д. Фильтры для умягчения воды необходимы для снижения содержания солей жесткости (кальция, магния) в домашних условиях. Монтаж системы умягчения воды в коттедже требует изначальных капитальных вложений средств, однако эти затраты несравнимы с ценой замены вышедшей из строя бытовой техники или стоимостью устранения неисправностей оборудования, установленного в коттедже.
КАК ВЛИЯЕТ ЖЁСТКОСТЬ НА КАЧЕСТВО ВОДЫ
С точки зрения применения воды для питьевых нужд, ее приемлемость по степени жесткости может существенно варьироваться в зависимости от местных условий. Порог вкуса для иона кальция лежит (в пересчете на мг-эквивалент) в диапазоне 2-6 мг-экв/л, в зависимости от соответствующего аниона, а порог вкуса для магния и того ниже. В некоторых случаях для потребителей приемлема вода с жесткостью выше 10 мг-экв/л. Высокая жесткость ухудшает органолептические свойства воды, придавая ей горьковатый вкус и оказывая отрицательное действие на органы пищеварения.
Всемирная Организация Здравоохранения не предлагает какой-либо рекомендуемой величины жесткости по показаниям влияния на здоровье. В материалах ВОЗ говорится о том, что хотя ряд исследований и выявил статистически обратную зависимость между жесткостью питьевой воды и сердечно-сосудистыми заболеваниями, имеющиеся данные не достаточны для вывода о причинном характере этой связи. Аналогичным образом, однозначно не доказано , что мягкая вода оказывает отрицательный эффект на баланс минеральных веществ в организме человека.
Вместе с тем, в зависимости от рН и щелочности, вода с жесткостью выше 4 мг-экв/л может вызвать в распределительной системе водопровода отложение шлаков и накипи (карбоната кальция), особенно при нагревании. Именно поэтому нормами Котлонадзора вводятся очень жесткие требования к величине жесткости воды, используемой для питания котлов (0.05-0.1 мг-экв/л).
Кроме того, при взаимодействии солей жесткости с моющими веществами (мыло, стиральные порошки, шампуни) происходит образование «мыльных шлаков» в виде пены. Это приводит не только к значительному перерасходу моющих средств. Такая пена после высыхания остается в виде налета на сантехнике, белье, человеческой коже, на волосах (неприятное чувство «жестких» волос хорошо известное многим). Главным отрицательным воздействием этих шлаков на человека является то, что они разрушают естественную жировую пленку, которой всегда покрыта нормальная кожа и забивают ее поры.
Признаком такого негативного воздействия является характерный «скрип» чисто вымытой кожи или волос. Оказывается, что вызывающее у некоторых раздражение чувство «мылкости» после пользования мягкой водой является признаком того, что защитная жировая пленка на коже цела и невредима. Именно она и скользит. В противном случае, приходится тратиться на лосьоны, умягчающие и увлажняющие кремы и прочие хитрости для восстановление той защиты кожи, которой нас и так снабдила природа.
Устранение жесткости воды
Чтобы избежать нежелательных последствий влияния солей жесткости на здоровье человека и функционирование бытовых приборов, применяются технологии устранения жесткости воды. На данный момент учеными разработано несколько способов, позволяющих справиться с данной проблемой:
реагентное умягчение( Ca(HCO 3 ) 2 + Ca(OH) 2 → 2CaCO 3 ↓ + 2H 2 O)
источник
Са2+ + Na2MgТр.→ Mg2+ + Na2СаТр.
и ионы кальция будут заменены в анализируемой воде ионами магния в эквивалентном отношении.
Устойчивость комплекса существенно зависит от рН раствора. Поэтому комплексонометрическое титрование ведут в заданном интервале рН, используя различные буферные растворы.
Методом комплексонометрии можно определить катионы магния, кальция, цинка, алюминия, бария, свинца и многие другие – более 40 различных катионов. Этот метод широко применяется для определения жесткости воды.
1.6. Методика определения жесткости воды комплексонометрическим
Метод основан на образовании при рН=10±0,2 прочного бесцветного комплексного соединения трилона Б с ионами кальция и магния. В эквивалентной точке титрования все ионы кальция и магния связываются в комплексное соединение трилоном Б, в результате чего происходит изменение окраски индикатора от красной до голубой.
Чувствительность метода составляет 0,5 мг – экв/л при титровании 0,1н
Отбор проб является важной частью анализа, необходимым условием правильности получаемых результатов.
Главные принципы, которые требуется соблюдать при отборе проб воды, состоят в следующем:
1. Проба воды, взятая для анализа, должна отражать условия и место ее отбора. При отборе поверхностных вод необходимо изучить окружающую местность и брать пробы воды выше и ниже спуска сточных вод. Пробы из трубопроводов при наличии штуцера отбирают так, чтобы скорость вытекания воды из трубопровода совпадала со скоростью отбора. Соответственно цели анализа отбирают разовые и смешанные (средние) пробы за определенный период, сливая разовые, взятые из одного и того же места, через равные промежутки времени. Иногда средние пробы
отбирают одновременно из разных мест исследуемого объекта и сливают вместе. Окончательный объем средней пробы должен быть пропорционален расходу воды и определяется из условия заданного перечня определений.
2.Объем пробы должен быть достаточным и соответствовать применяемой методике анализа. Для неполного анализа, при котором определяют только несколько компонентов, достаточно отобрать 1 л воды. Для более подробного анализа следует брать 2 л воды.
3. Пробы воды отбирают в стеклянные или полиэтиленовые бутыли с хорошо подобранной пробкой, а при наличии крупных примесей – в жестяные бидоны или банки с широким горлом. Посуду, используемую для отбора проб, необходимо вымыть хромовой смесью и тщательно промыть водопроводной, а затем дистиллированной водой. Перед отбором пробы посуду ополаскивают несколько раз исследуемой водой.
4. Отбор пробы, условия транспортирования и сроки хранения определяются из условий отсутствия изменений в содержании определяемых компонентов или в свойствах воды. Необходимо учесть, что ни консервация, ни фиксация не обеспечивают постоянного состава пробы на продолжительное время.
Целью этих операций является сохранение содержания соответствующего
компонента без изменения на время, необходимое для доставки и обработки пробы воды. К анализу следует приступать в кратчайший срок после отбора пробы.
1.6.3. Реактивы и оборудование
· трилон Б (фиксанал 0,1н) по ТУ 6-09-2540-87;
· серно – кислый магний MgSO4 (фиксанал 0,1н) ТУ 6-09-2540-87;
· аммиачный буферный раствор;
· индикатор эриохром черный Т или кислотный хром темно – синий ч.д.а. ТУ 6-09-3870-87Е;
· сернистый натрий 9 – водный ч.д.а., Na2S ГОСТ 2053-77.
· Трилон Б 0,05н: раствор готовят из 0,1н трилона Б, приготовленного из фиксанала, разбавлением его в 20 раз. Для этого 50 мл трилона Б 0,1н переносят в мерную колбу на 100 мл и доводят до метки обессоленной воды. При отсутствии фиксанала берут навеску 18,613 г. трилона Б и растворяют в мерной колбе на 1000 мл. Устанавливают титр трилона Б по фиксаналу 0,1н MgSO4. Пипеткой отбирают 10 мл 0,1н MgSO4 в коническую колбу, добавляют 90 мл обессоленной воды, 5 мл аммиачно – буферного раствора, 5 – 7 капель индикатора кислотного хром темно – синего (эриохром черного, хромогена) и титруют раствором трилона Б до голубого цвета. Должно пойти 20 мл трилона Б
· Аммиачный буферный раствор: 20 г NH4Cl растворить в 500 мл воды, добавить 80 мл концентрированного аммиака NH4OH и довести объем до 1000 мл.
· Индикаторы кислотный хром темно – синий или эриохром черный Т: 0,5 г индикатора растворяют в 20 мл аммиачно – буферного раствора и доводят объем до 100 мл этиловым спиртом.
Отобрав определенный объем анализируемой воды (обычно 100мл) в коническую колбу, вводят в нее 5 мл аммиачной буферной смеси, несколько капель
индикатора и титруют окрашенную в розовый или фиолетово – розовый цвет жидкость раствором трилона Б. Титрование ведут медленно, по каплям, так как образование трилонатных комплексов происходит не мгновенно.
ибавление титранта, т.е. раствора трилона Б, ведут до наиболее четкого изменения цвета. Здесь необходима, как говорят, «ститровка» всего коллектива данной лаборатории. Дело в том, что резкое «от одной капли» изменение окраски титруемой жидкости происходит только при работе с 0,1н и 0,01н растворами трилона Б. Применение более разбавленных растворов создает не резкое, а постепенное изменение окраски; на это требуется, например, от трех до пяти капель 0,002н раствора трилона Б. Вследствии этого необходимо выработать по возможности единое мнение о той окраски, при которой следует считать титрование законченным. Для этого в ряд конических колб вливают по 100 мл дистиллированной обессоленной воды, добавляют в каждую колбу по 2 мл раствора сернокислого магния (MgSO4) конц.
1 мг-экв/л и по 5 мл аммиачной буферной смеси. Затем в первую колбу вводят 0,95 мл 0,002н раствора трилона Б, т.е. с явным недостатком, а в каждую следующую на одну каплю больше, чем в предыдущую. Например, 0,95; 0,98; 1,01; 1,04; 1,07; 1,10 мл (если объем капли 0,03мл). Жидкость в последней колбе будет явно перетитрована, т.к. 1 мл 0,002н раствора трилона Б содержит 2 мкг – экв вещества, т.е. такое же количество, что и 2 мл магнезиального раствора. Составив все колбы в ряд, решают, где возникает наиболее четко визуально – определенная разница окрасок. До этого изменение цвета в дальнейшем и ведут титрование. Следует лишь иметь ввиду, что переход окраски отмечается несколько различно в зависимости от освещения. Наиболее четко этот переход заметен при естественном дневном освещении, менее отчетливо при обычном электрическом и хуже всего при лампах «дневного света». Из индикаторов четче всего переход окраски при работе с эриохром черным ЕТ00, но этот индикатор, к сожалению, и наименее чувствителен.
Так как в анализируемой воде могут присутствовать, кроме кальция и магния, также и другие катионы, взаимодействующие с Трилоном Б, например железо,
цинк, медь, марганец, то принимают меры против их влияния на результаты титрования. Влияние меди и цинка устраняют добавлением к воде нескольких капель 10% — го раствора сульфида натрия. Образующиеся сернистые медь и цинк столь малорастворимы, что уже не дают трилонаты. Влияние железа может быть предотвращено окислением его до трехвалентного, которое выпадает в щелочной воде в осадок, также очень малорастворимый. Иногда предпочитают закомплексовывать железо лимонной или винной кислотами, добавленными с большим избытком. Марганец в щелочной среде окисляется до марганцовистой кислоты. Жидкость при этом приобретает серый цвет, мешающий титрованию. Введением гидроксиламина или гидрозина сохраняют марганец в двухвалентном состоянии. При этом он оттитровывается вместе с кальцием и магнием, несколько завышая, следовательно, величину жесткости. В водах электростанций марганца
обычно так мало, что этим завышением пренебрегают.
Следует заметить, что иногда в водах (чаще всего в котловых) оказываются
вещества, образуют с индикаторами прочные, окрашенные в красный цвет, соединения. Они лишь очень медленно, иногда в течение часа, разлагаются трилоном Б, причем для этого необходим обычно значительный его избыток. При титровании вод, содержащих такие вещества, розовая окраска или оттенок не устраняются даже после добавления значительных избытков трилона Б. Проба остается неоттитрованной, однако по истечении некоторого времени, иногда 10 – 20 минут, иногда 1 часа, розовый оттенок исчезает и жидкость приобретает явно сильно «перетитрованный» вид. Специальные опыты показывают, что такие прочные соединения с индикаторами, медленно разрушающиеся лишь избытками трилона Б, образуют катионы металлов, расположенных в правой нижней части таблицы Д.И. Менделеева, а также, по – видимому, некоторые органические амины. Устранить мешающее влияние этих агентов иногда удается выпариванием порции воды досуха, прокаливанием сухого остатка при 700 – 8000С и последующим растворением кальциевых и магниевых соединений слабой соляной кислотой. Можно также применить для определения жесткости таких вод олеатный способ.
1.6.5. Обработка результатов
Жесткость анализируемой воды вычисляют по формулам:


где а – расход трилона Б, пошедшее на титрование, см3
N – нормальность раствора трилона Б
К – поправочный коэффициент к номинальной нормальности
1.7. Экспериментальные данные
Проведя анализ, получили показания жесткости исходной воды, которые представлены в таблице 1.2
Vсредний, см3 Трилон Б 0,05н
6,60 + 6,57 + 6,74 + 6,59 + 6,45 + 6,51 + 6,52 + 6,41 + 6,59 + 6,57


Выполнив расчеты по формулам, получили жесткость воды 3,275 мг-экв/л, что соответствует предъявляемым требования к качеству исходной воды.
Полная себестоимость промышленной продукции — это выраженные в денежной форме затраты предприятия на ее производство и реализацию. Планирование и учет себестоимости продукции ведут по элементам затрат и калькуляционным статьям расходов.
Элементы затрат: материальные затраты (МЗ), трудовые затраты (ТЗ), амортизация, прочие затраты.
Статьи калькуляции: сырье и материалы, топливо и энергия на технологические цели, основная и дополнительная зарплата, отчисления в различные фонды, общепроизводственные расходы (ОПР), общехозяйственные расходы (ОХР), коммерческие расходы (КР), прочие расходы.
Калькуляция себестоимости промышленной продукции состоит из трех частей:
2. накладные расходы (ОПР, ОХР и КР)
3. плановые накопления (прибыль и торговые надбавки)
В состав ОПР входят: расходы на содержание и эксплуатацию оборудования (амортизация производственного оборудования и транспорта, расход энергии на приведение в действие оборудования, ремонт оборудования, расходы по внутризаводскому перемещению грузов, износ инструментов) и цеховые расходы (зарплата цехового персонала, амортизация, содержание и ремонт основных фондов, расходы на ОТ и ТБ, недостачи и потери от порчи и простоев).
В состав ОХР входят: расходы по содержанию аппарата управления (зарплата руководителей, амортизация и содержание непроизводственных зданий и сооружении и легковых автомобилей, расходы на содержание вычислительных
центров, почтово-телеграфные расходы) и прочие общехозяйственные расходы (зарплата служащих, расходы на подготовку кадров и другие).
Коммерческие расходы включают расходы на анализ рынка, рекламу и прочие.
Калькуляция себестоимости промышленной продукции
Основная заработная плата производственных рабочих (Зосн)
Дополнительная заработная плата производственных рабочих (Здоп)
Отчисления во внебюджетные фонды (Овбф)
Итого трудовые затраты (ТЗ)
Общепроизводственные расходы (ОПР)
Общехозяйственные расходы (ОХР)
Итого производственная себестоимость (С/Спр)
Итого полная себестоимость (С/Сполн)
Рыночная цена продукции (Црын)
Расчет статей калькуляции.
1. Определяем трудовые затраты:
ТЗ = Зосн + Здоп + Овбф = 450 + 45 + 126 = 621
Здоп = 10% от Зосн = 450 ∙ 0,1 = 45
Овбф ≈ 28% от Зосн = 450 ∙ 0,28 = 126
2. Определяем общехозяйственные расходы: ОХР = Зосн · Кохр = 450 ∙ 1,3 = 585
3. Определяем производственную себестоимость: С/Спр = ПЗ + ОПР + ОХР = 711 + 135 + 585 = 1431
4. Определяем коммерческие расходы:
КР = С/Спр · Ккр = 1431 ∙ 0,02 = 28,6
5. Определяем полную себестоимость:
С/Сполн = С/Спр + КР = 1431 + 28,62 = 1459,6
П = С/Сполн · 0,3 = 1459,6 ∙ 0,3 = 437,9
7. Определяем оптовую цену:
Цопт = С/Сполн + П = 1459,6 + 437,9 = 1897,5
8.Определяем налог на добавленную стоимость: НДС = Цопт · 0,18 = 1897,5 ∙ 0,18 = 341,5
9. Определяем отпускную цену:
Цотп = Цопт + НДС = 1897,5 + 341,5 = 2239
10. Определяем торговую надбавку:
ТН = Цотп · 0,25 = 2239 ∙ 0,25 = 559,75
11. Определяем рыночную цену:
Црын = Цотп + ТН = 2239 + 559,75 = 2798,75
3. ОХРАНА ТРУДА И ТЕХНИКА БЕЗОПАСОСТИ
Лабораторные, складские и вспомогательные помещения снабжаются средствами пожаротушения в соответствии с разработанными на предприятии нормами.
К первичным огнетушащим средствам относятся различные огнетушители, асбестовое полотно, а также водопроводная вода. В условиях лаборатории, при чрезвычайном обилии различных горючих веществ с различными свойствами, особенно важно правильное и своевременное применение первичных средств тушения огня. Успешная борьба с возгораниями не возможна без четкого знания возможностей и областей применения каждого из имеющихся в лаборатории огнетушащих средств.
В химической лаборатории рекомендуется использовать углекислотные, порошковые, пенные и воздушно-пенные огнетушители.
Углекислотный огнетушитель должен быть в каждом лабораторном помещении, независимо от наличия других средств огнетушения.
Лабораторные помещения должны быть оснащены средствами индивидуальной защиты (СИЗ): защитными очками, резиновыми перчатками, фартуком, аптечкой для оказания первой помощи; на рабочих местах надлежит иметь достаточное количество нейтрализующих средств (3% содовый и 2% кислотный растворы).
Подавляющая часть работ в химической лаборатории связана с использованием стеклянной посуды, аппаратов и приборов. Поэтому технике безопасности при работе со стеклом необходимо уделять самое серьезное внимание:
· нельзя нагревать не термостойкие стаканы и колбы на открытом огне или непосредственно электроплитке, а также резко охлаждать нагретые сосуды;
В данной работе представлено описание использования воды в промышленности, основные показатели качества воды и ее свойства, такие как щелочность, жесткость, прозрачность, реакция воды и другие.
Подробно рассмотрены способы водоподготовки.
Изложены возможные методы определения жесткости воды, подробно рассмотрен комплексонометрический метод.
Представлены методика анализа, правила отбора проб воды для анализа, правила приготовления реактивов и выполнения анализа. Также представлена таблица экспериментальных данных, из которой следует, что жесткость воды составляет 3,275 мг-экв/л, что соответствует предъявляемым требования к качеству исходной воды.
Дан экономический расчет статей калькуляции.
Дана техника безопасности при работе в химических лабораториях. Описаны правила работы со стеклом, средства пожаротушения, а также средства личной защиты и спецодежда сотрудников химических лабораторий.
1. Алексеев В.Н. Количественный анализ. – М.: Химия, 1972
2. Васильев В.П.Аналитическая химия. Кн. 1: Титриметрические и гравиметрические методы анализа. – М.: Дрофа, 2005.
3.Временное методическое руководство по анализу технологических и сточных вод предприятий черной металлургии. – М.: Металлургия, 1981.
4.Глинка Н.Л. Общая химия. – М.: Химия, 1980.
5.Гурвич С.М., Кострикин Ю.М. Оператор водоподготовки. – М.: Энергия, 1967.
6. Инструкция о порядке проведения химического анализа воды и пара в Паросиловом цехе ОАО «ММК» ЭИ-ПСЦ-3-44-2008
7.Кострикин Ю.М. Инструкция. – М.: 1967.
8. Крешков А.П., Ярославцева А.А. Курс аналитической химии. Количественный анализ. – М.: Химия, 1982.
9. Посыпайко В.И., Васина Н.А. Аналитическая химия и технический анализ. – М.: Высшая школа, 1979.
10.Сороко В.Е., Вечная С.В., Попова Н.Н. Основы химической технологии. – СПб.: 1986.
· стеклянная посуда не предназначена для работы на повышенном давлении;
· нельзя допускать нагревание жидкостей в закрытых колбах или приборах, не имеющих сообщения с атмосферой;
· категорически запрещается использовать посуду, имеющую трещины или отбитые края;
· осколки разбитой посуды убирают только с помощью щетки и совка, но ни в коем случае не руками;
· стеклянные приборы и посуду больших размеров можно переносить только двумя руками. Поднимать крупные бутыли за горло запрещается.
Транспортировка до рабочего места химических реактивов (до 2 – х литров) должна осуществляться в специальных металлических контейнерах (ведрах).
Бутылки, реактивные склянки и колбы с химическими реактивами должны иметь надпись этикетку, бирку с названием. Хранить на рабочих местах вещества неизвестного происхождения запрещено!
При разведении концентрированных реактивов их приливают тонкой струей в воду при одновременном перемешивании раствора. Приливать воду к концентрированным кислотам и щелочам запрещено!
Нейтрализовать разрешается лишь разбавленные кислоты разбавленными щелочами и наоборот. При смешивании, нейтрализации или разбавлении растворов, сопровождающихся выделением тепла, необходимо пользоваться термостойкой посудой.
Нельзя засасывать концентрированные кислоты и щелочи ртом в пипетку, необходимо пользоваться резиновыми грушами.
Дозировка кислот, щелочей и других химических реактивов производится с помощью мензурок, цилиндров и другой мерной посуды в реактивную склянку.
Все работы должны проводиться в СИЗ: резиновых перчатках, очках, фартуке и спецодежде (халате).
После каждого пользования концентрированными реактивами необходимо тщательно мыть руки.При разливе концентрированных химических веществ,
После проведения полного обессоливания воды необходимо убедится в отсутствии в ней как катионов (Mg 2+ , Ca 2+ ), так и анионов (SO4 2– , NO3 – , Cl – ). Анализ на содержание указанных анионов в воде до ее обессоливания и после проводится качественно.
SO4 2– – раствор хлорида бария дает белый осадок сульфата бария;
Cl – – при добавлении раствора нитрата серебра образуется белый осадок хлорида серебра;
NO3 – – при добавлении раствора дифениламина в серной кислоте появляется характерное для ионов NO3 – синее окрашивание.
Определение содержания взвешенных частиц (мутность воды)
Мутность воды определяется фотоколориметрическим методом при длине волны 440 нм. Оптическую плотность измеряют в кюветах с толщиной поглощающего слоя 3 мм. Количество взвешенных частиц в воде находят по калибровочной кривой.
Регистрирующим прибором в фотоколориметре служит микроамперметр типа М907, оцифрованный в микроамперах и имеющий шкалу 0–100 делений, соответствующих шкале коэффициентов пропускания – и оптической плотности – D. При измерении со светофильтром 440 нм, отмеченным на лицевой панели колориметра черным цветом, ручку «Чувствительность» устанавливают в одно из положений 1, 2 или 3. Рабочие поверхности кювет перед каждым измерением необходимо тщательно протирать спирто-эфирной смесью, жидкость в кюветы наливать до метки на боковой поверхности кюветы. При установке кювет в кюветодержатель нельзя касаться пальцами участков поверхности кювет ниже уровня жидкости в них.
Колориметр включают в сеть за 15 мин до начала измерений. Во время прогрева кюветное отделение должно быть открыто (при этом шторка перед фотоприемником перекрывает световой пучок). В световой пучок помещают кювету со стандартным раствором, по отношению к которому производят измерения, и крышку кюветного отделения закрывают. Ручками «Чувствительность» и «Установка 100» устанавливают отсчет 100 по шкале колориметра. Затем поворотом ручки кювету со стандартным раствором заменяют кюветой с исследуемым раствором. После этого производят отсчет по шкале колориметра, соответствующий коэффициенту пропускания исследуемого раствора в процентах, или по шкале D в единицах оптической плотности. Измерения проводят 3–5 раз и окончательное значение измеряемой величины определяют как среднее арифметическое полученных значений.
Для определения общей жесткости воды в лабораторных условиях используют комплексонометрический метод, основанный на образовании сложных соединений анализируемых ионов с органическими реагентами (комплексонами) (1). Перед началом работы пробу разбавляют спиртовым раствором индикатора эриохрома черного Т или сухой смесью хлорида натрия и кальция. К окрашенному в вино-красный цвет раствору добавляется по каплям Трилон Б. Величину общей жесткости вычисляют по формуле:
Жо=Nx*Vx*1000/V1
(N-нормальность раствора Трилона Б, V-объем раствора Трилона Б, V1-объем пробы).
Для справки: Титрование (титриметирческий анализ) – метод количественного расчета содержания вещества, реагирующего с реактивом известной концентрации.
При помощи титрования и колориметрического метода можно узнать не только величину общей, но и временной жесткости. Для этого исследуемые пробы соединяют с индикатором (метилоранж), после чего эталонный образец переставляют на белый фон, а вторую пробирку титруют раствором соляной кислоты до появления оранжево-красного оттенка. Рассчитывая необходимое количество «солянки», определяют временную жесткость воды.
Нвр = NHCl * VHCL* 1000/ V1
(N-нормальность раствора соляной кислоты, V-объем раствора соляной кислоты, V1-объем пробы)
Уравнение реакции:
Титрование – один из самых распространенных и простых методов определения концентрации ионов кальция и магния. К минусам традиционных методик следует отнести невысокую точность.
О том, как проверить жесткость воды с минимальными погрешностями, знает обслуживающий персонал высокоточных приборов. Ярким примером одного из самых надежных инструментов определения концентрации ионов кальция и магния является АКМС-1. По результатам сравнения разности электродных потенциалов с эталонными значениями, прибор автоматически выводит результаты анализа на дисплей.
Метод атомной спектрометрии основывается на резонансном поглощении света атомами исследуемых химических элементов. К преимуществам подобного метода относится высокая точность. Недостатком атомной спектрометрии считают высокую стоимость требуемых приборов.
Для определения жесткости воды можно воспользоваться приборами и инструментами, используемыми в аквариумистике. С точностью до 2% снимают показания TDS-метры.
Принцип действия подобного прибора основан на прямой зависимости электропроводности и количества растворенных солей кальция и магния.
На заводах и предприятиях, а также в лабораторных условиях очистных сооружений наиболее точными считаются результаты нескольких опытов, различающихся методикой вычисления концентрации «целевых» компонентов или частиц загрязнителя.
Выделяют три вида жёсткости:
- временная (карбонатная), обусловленная содержанием гидрокарбонатов кальция и магния – солей слабой угольной кислоты. При кипячении соли распадаются, в результате образуется нерастворимый осадок из карбоната кальция (СаСО3) и гидроокиси магния (Мg(OH)2;
- постоянная (некарбонатная), от которой невозможно избавиться кипячением. В воде находят соли двухвалентных металлов (кальция, магния, бария и стронция), образованных сильными кислотами: соляной (HCl), серной (H2 SO4), азотной (HNO3). Соли бария и стронция для расчета степени жёсткости воды не учитывают, поскольку их количества незначительны;
- общая – определяется как суммарная концентрация ионов кальция и магния в воде.
В России воду классифицируют в зависимости от величины показателя общей жёсткости:
- до 2°Ж – мягкая;
- от 2 до 10°Ж – средней жёсткости;
- более 10°Ж – жёсткая.

Слишком жёсткая или слишком мягкая вода может нанести непоправимый вред как бытовым приборам, так и здоровью людей. Мягкая вода вымывает из организма кальций, из-за чего разрушаются кости и зубы. В такой воде активно коррозируют металлические поверхности. Чтобы этого избежать, используют ингибитор коррозии.
- создает слишком большую солевую нагрузку для мочеполовой системы. Возможно появление мочекаменной болезни, ухудшение состояния волос и кожи;
неблагоприятно действует на теплотехнические и сантехнические системы, приносит немалый вред бытовой технике; - приходится тратить больше тепла на нагрев воды: слой накипи (осадок из солей жесткости), появившийся на ТЭНах, обладает низкой теплопроводностью. Из-за недостаточного отвода тепла нагревательные элементы часто сгорают;
- увеличивается расход моющих средств из-за того, что поверхностно-активные вещества (ПАВ), входящие в состав, дают с солями кальция и магния нерастворимые соединения и не образуют достаточного для удаления загрязнений количества пены;
- стенки трубопроводов быстро зарастают известковыми отложениями, поэтому в водопроводной системе снижается напор, трубы приходится менять.
Следите за показателями жёсткости воды, поступающей из водопровода или местного источника. Если пользоваться доступными средствами смягчения воды, водопроводная система, нагреватели, стиральная и посудомоечная машины прослужат намного дольше.
Прежде чем покупать дорогие устройства и реагенты, выясните, какие соли и в каком количестве присутствуют в водопроводной воде. Показатель общей жёсткости меняется в зависимости от количества осадков, таяния снега и других явлений, влияющих на концентрацию солей. Чтобы правильно выбрать умягчители, сначала сделайте анализ на определение жёсткости воды.
Для бытовых целей: умывания, стирки и уборки, – достаточно выяснить показатель жесткости воды один раз и в случае необходимости использовать подходящие средства. Для приготовления пищи, если водопроводная слишком вода жёсткая, целесообразно использовать бутилированную воду хорошего качества, которую периодически проверять портативным и несложным в обращении прибором для определения общей и карбонатной жёсткости.
Предположить, что вода содержит большое количество солей щелочноземельных металлов, можно по следующим признакам:
- плохо пенится мыло и стиральный порошок;
- на поверхности нагревательных приборов образуется известковый налет;
- вода имеет горьковатый вкус и дольше обычного заваривается чай;
- при кипячении на поверхности воды образуется характерная пленка;
- плохо развариваются мясные продукты.
1. Полоски жесткости воды. Продаются в аптечных магазинах «Медтехника», показывают результат измерения с точностью 1-2°Ж.
Инструкция: опустить полоску жесткости в стакан с водой, подождать, пока индикатор, которым она пропитана, изменит цвет, затем сравнить с эталонной шкалой.
2. Экспресс-тесты для аквариумов. Этот способ основан на методе титрования.

Инструкция: в пробирку налить 5 мл воды и по каплям добавить реагент, содержащий индикатор. Число капель реагента, необходимых для того, чтобы раствор из жёлтого стал синим, равно количеству градусов жёсткости, каких именно – указано в инструкции к тесту.
3. Специальные приборы. Самый простой и точный метод определения жёсткости воды – титрование. Основан на реакции индикаторов, их способности менять цвет при достижении той или иной концентрации в строго определенном количестве воды, содержащей соли. В лабораториях результаты титрования обрабатывают с помощью фотоколориметра.
Существуют приборы, принцип действия которых заключается в измерении электропроводности воды. Уровень проводимости прямо пропорционально зависит от концентрации солей кальция и магния, растворённых в воде. В продаже есть приборы типа TDS-метр (total dissolved solids, или «солемер») и EC-метр (кондуктометр).

TDS-метр выдаёт результат в ppm. Устройство показывает общее содержание солей и удельную электропроводность воды. EC-метр дополнительно показывает и удельное сопротивление раствора в мкСм/см (микро Сименс). Результат TDS = k * EC, где коэффициент k в пределах 0,55–0,80 (среднее значение 0,67).

С помощью таких приборов удобно следить и поддерживать требуемое качество воды в аквариумах или для полива растений, чувствительных к повышенной жёсткости.
Жёсткость воды – термин, говорящий о процентном соотношении солевых частиц магния и калия в жидкости. Она подразделяется на две разновидности:
- Временная (такая жидкость называется карбонатная);
- Общая жёсткость (данная вода относится к некарбонатной).
Первый тип жёсткости характеризуется присутствием гидрокарбонатных солевых частиц магния и калия. Если такую воду закипятить, то элементы распадутся на карбонаты и гидроксиды и выпадут в осадок. Именно этот белый налёт часто покрывает наши чайники изнутри и собирается на других нагревательных элементах.
Для жидкости с общей жёсткостью характерно наличие других химических элементов (различных нитратов, хлоридов и тп.п). Обычно жёсткость питьевой воды связана с особенностями вашего региона, составом грунтов. Чем больше известковых пород находится в почве, тем выше жёсткость воды. Но важно не только понимать суть понятия, но и знать, как проверить жёсткость воды. Выполнить это легко как в быту, так и на заводе.
Для проверки жёсткости водопроводной воды дома можно использовать следующие способы:
- Постарайтесь обильно вспенить мыльный брусок или порошок для стирки. Если у вас образуется мало пены, то ваша вода имеет повышенную жёсткость. Это возникает по той причине, что солевые частицы калия и магния не позволяют мылу пениться. При обильной пышной пене от любого моющего средства можно утверждать, что вода нежёсткая. Но этот метод не позволят точно определить степень жёсткости.
- На вкус также можно отличить жёсткую воду от мягкой. Она более горькая. Но не все могут точно уловить горьковатый привкус солей магния и калия.
- Белый осадок в чайниках, накипь на нагревательных элементах других бытовых приборов – признак жёсткой воды. Осадок возникает из-за распада солей и выпадения их на дно. Данная особенность жёсткой воды очень вредит бытовым приборам и отопительному трубопроводу.
- От жёсткости воды зависит скорость заваривания чайного напитка. При мягкой воде на эту процедуру уйдёт от 3 до 6 мин., в жёсткой воде чай будет завариваться от 8 до 12 мин. Кстати, на вкус оба напитка будут существенно отличаться.
- Благодаря нехитрому компактному измерительному прибору можно очень легко определить жёсткость любой жидкости. Он называется TDS-метр. Агрегат измерят электропроводность жидкости. Чем выше показатель, тем больше уровень солесодержания жидкости. Обычно его ещё называют солемер. Чаще такой анализ воды на жёсткость делают владельцы аквариумов и цветоводы.
- Проверить жёсткость воды в быту можно, используя тест-полоски, продающейся в аптеках медтехники.
Для этого анализа можно использовать колориметрическую методику и принцип титрования. Процедура анализа выполняется так: порция воды смешивается с метилоранжем (индикатором), ёмкость устанавливается на светлом фоне. Во вторую тару с водой добавляют соляную кислоту, пока не получится красно-оранжевый цвет воды.
Временную жёсткость жидкости находят в процессе расчёта требуемого количества соляной кислоты по формуле: Нвр = NHCl * VHCL* 1000/ V1, где N-насыщенность раствора, V-его количество, V1-количество пробы.
Этот анализ проводят в лаборатории. Для него используют комплексонометрическую методику. Она базируется на принципе возникновения соединений ионов, подвергающихся анализу, с природными реагентами. Сначала воду в пробирке разводят раствором индикатора на спирту (чёрного этиохрома «Т»). Также для этих целей может использоваться сухая смесь кальциевых и натриевых хлоридов. В итоге полученная смесь окрашивается в насыщенный рубиновый цвет. Затем в пробирку капается вещество, называемое Трилон.
Расчёт общей жёсткости производится по уравнению: Жо=Nx*Vx*1000/V1, где N-насыщенность вещества Трилон, V-его количество, V1-количество пробы.
Как мы уже говорили выше, прибор контроля жёсткости воды называется солемер или TDS-метр. Точность проверки составляет 2%. Основной принцип работы данного агрегата построен на зависимости электропроводности жидкости от общего числа примесей солей магния и калия. То есть чем больше данных солей в воде, тем больше будут показания прибора, а следовательно, тем выше жёсткость воды.
На некоторых предприятиях и заводах наблюдается прямая зависимость между жёсткостью используемой воды и исправностью работы оборудования. Поэтому для обеспечения бесперебойной работы технологического оборудования требуется осуществлять постоянный автоматический контроль жёсткости воды.
Для этих целей используется специальное оборудование, например, анализатор «АКМС-1». Этот прибор непрерывно контролирует содержание солевых частиц кальция и магния в жидкости, поступающей в технологическое оборудование. То есть он подсчитывает общую жёсткость в пределах 0,005-25,0 мг-экв/л.
Как понять, что ваша водопроводная вода жёсткая, мы писали выше. Теперь перечислим ряд мер, позволяющих снизить жёсткость воды в домашних условиях:
- Самый простой способ – кипячение воды.
- Фильтрация воды через системы обратного осмоса (специальные мембраны).
- Использование смягчающих солей.
- Применение фильтрующих картриджей.
- Магнитное фильтрующее устройство.
- Использование ионообменной смолы в комплексе с солевым раствором.
Хотите провести контроль жёсткости воды? Заказать такую услугу вы можете у наших специалистов, для этого вам достаточно связаться с нами по указанным телефонам.
Самый простой способ узнать, можно пить воду или нет – это оценить её органолептические свойства, простыми словами, осуществить экспресс-анализ воды на запах, вкус и цвет. По сути, такие действия человек выполняет практически всегда, прежде чем что-то съесть или выпить. Причём делает он это подсознательно, не задумываясь.
Проверка воды выполняется следующим образом: если у неё приемлемый цвет, то нужно понюхать, при допустимом запахе нужно попробовать и оценить вкус. Решение о пригодности к употреблению принимается по совокупности параметров.
Важно! На вкус воду рекомендуется пробовать после ее кипячения в течение 10 минут.
Естественно, точность органолептического анализа невысокая и полагаться исключительно на него не стоит. Такая мера эффективна в том случае, когда под рукой отсутствуют прочие средства, а органы чувств постоянно при вас.
Экспресс-анализ воды этим методом позволяет однозначно выявить проблемный состав. Но если какой-либо показатель окажется подозрительным — это повод сдать жидкость на лабораторную проверку.
В отличие от вкусовых качеств, неприятный запах является более точным показателем имеющейся проблемы. Самыми распространёнными причинами его возникновения являются:
- попадание продуктов нефтепереработки или химикатов в воду;
- происходящие в воде химические реакции, в первую очередь окисление;
- активная жизнедеятельность микробов и бактерий в воде.
Чтобы справиться с двумя первыми причинами, необходимо провести механическую и сорбционную очистку, только в отдельных случаях потребуется более тщательная фильтрация. К примеру, обратноосмотическая система.
Если в воде активно развиваются микроэлементы, необходимо обезвредить их путём обеззараживания. Можно применить хлорирование или обрабатывание ультрафиолетом.
Кроме того, причинами неприятного запаха воды могут служить такие обстоятельства, как повышенная жёсткость или температурный режим окружающей среды. Для понижения жёсткости можно воспользоваться умягчителями.
Хорошо справляются с задачей полифосфатные фильтры. Важно! Нельзя применять их для очистки питьевой воды, только для жидкости, использующейся в технических целях.
Абсолютная прозрачность – признак идеальной воды. Экспресс-анализ по цветовым характеристикам можно провести следующими способами:
- Наберите воду в просвечивающий стакан либо колбу и рассмотрите содержимое на фоне белоснежного листка бумаги. Если жидкость имеет тёмный оттенок — в ней, скорее всего, содержится огромное количество активно разлагающихся органических элементов.
- Налейте в прозрачный сосуд воду и попытайтесь прочесть через него какой-нибудь текст, написанный на белой бумаге. Бокал должен быть абсолютно гладким, иначе символы будут искажаться. Воды в стакане должно быть на уровне 20 см, не меньше. Если все напечатанные знаки отчётливо видны, то жидкость в достаточной степени прозрачна, в ином случае стоит задуматься о её качестве.
Мутность воды свидетельствует о большой численности мелкодисперсной взвеси либо других растворённых составляющих. К ним относятся как органические, так и неорганические сочетания. Не нужно забывать, что такая вода представляет собой идеальную среду для распространения различного рода микроорганизмов.
Чтобы осуществить экспресс-анализ питьевой воды на наличие механических соединений, достаточно наполнить ею ёмкость и дать отстояться. Если образовался осадок, это означает что жидкость необходимо пропустить сквозь фильтр тонкой механической очистки.
Для определения жёсткости достаточно что-нибудь намылить. Вода с высоким уровнем жёсткости трудно намыливается и практически не образовывает пены. А вот показатель Ph рекомендуется проверять экспресс-анализом (тестом) воды с помощью особых индикаторов, таких как лакмусовая бумага.
Такие наборы чаще всего используются для проведения проверки в домашних условиях. Тестовые полоски бывают разными, в зависимости от того, на какое количество компонентов рассчитано исследование. В продаже представлены в широком ассортименте виды наборов для экспресс-анализа воды:
- Тестовые системы вида ИТ. Исследование проводится с использованием индикаторных трубочек. Степень скопления активного вещества оказывает влияние на окрашивание тестера. Этот способ отличается высоким уровнем достоверности, простоты и хорошей чувствительностью.
- Тестовые наборы вида РС. Проверка осуществляется при помощи готовых составов либо смесей реагентов. Цвет раствора указывает на концентрацию того или иного вещества в воде. Такие наборы отлично подходят для колориметрического и спектрофотометрического анализа.
- Наборы тестеров вида ИП. В процессе проверки участвуют индикаторные пигменты. В зависимости от концентрации составляющих цвет пигмента изменяется. Экспресс-анализ воды таким набором проводить достаточно просто, а результат получается точным и быстрым.
- Специальные наборы для определения качественных показателей воды. С их помощью можно проводить анализ концентрации конкретного вещества: хлора, циановой кислоты и прочих.
Приборы экспресс-анализа воды очень компактны по размеру и просты в применении, понять процесс проверки сможет каждый. Большая их часть пригодна для использования в домашних условиях. В комплекте к каждому набору идёт инструкция по применению, где подробно описан процесс исследования. Приемлемая стоимость таких тестеров является преимуществом для простого человека.
Чтобы получить максимально точный результат, крайне важно предотвратить попадание в образец чужеродных элементов извне. К примеру, плохо очищенная ёмкость для набора воды на пробу может отрицательно повлиять и исказить результаты проверки. Итак, при отборе воды необходимо придерживаться следующих правил:
- Наливать жидкость для исследования нужно в чистую ёмкость либо специальный пакетик. Лучшим вариантом является приобретение стерильной тары из пластика в аптеке.
- Прежде чем набирать воду, следует протереть кран или вентиль медицинским спиртом, а также обработать им руки либо надеть стерильные перчатки.
- Перед набором воды для тестирования её необходимо спустить в течение 5–10 минут при полном напоре, в зависимости от вида источника.
- В зависимости от предполагаемого количества исследований набрать одну или несколько ёмкостей объёмом от 0,5–1,0 литра.
- Теперь можно приступать к тестированию реагентами, порошками, трубочками, лакмусовыми бумажками и прочими подручными средствами.
Важно! Если вы собираетесь использовать несколько тестеров, то для каждого из них следует приготовить отдельную ёмкость. То же правило распространяется на лакмусовые бумажки и прочие тесты.
Не забывайте, что своевременно проведённый анализ воды способен предотвратить многие заболевания организма.
Экология потребления. Наука и техника: Рассказ пойдёт о том, что загрязняет воду, как её чистят и почему я спокойно пью из родника, содержащего много нитратов.
Последние пять лет я занимаюсь химическим анализом воды и нахожусь в контакте с инженерами по водоподготовке. К нам приходят самые разные люди: для одних система очистки воды — очень дорогое, но жизненно необходимое приобретение, другие просто начитались страшилок в Интернете и хотят «живую воду». Но для нас, как и для врачей, все наши заказчики одинаковы. У них есть вода — скважинная, поступающая из городского или поселкового водопровода, колодезная, речная — и её необходимо очистить до установленных норм. О том, что загрязняет воду, как её чистят и почему я спокойно пью из родника, содержащего много нитратов, пойдёт этот рассказ. Но никакие названия фирм, географические привязки и другая индивидуализирующая информация указываться не будут — я просто хочу поделиться пятью годами своих наблюдений за процессом, потому что много владельцев коттеджей могли бы меньше нервничать, если бы озаботились водоочисткой ещё на этапе заливки фундамента.
Но для начала давайте определимся со структурой процесса и терминологией, чтобы общаться на одном языке. Строго говоря, без анализа воды ни одна нормальная организация, занимающаяся водоочисткой, даже на порог вас не пустит. Всё начинается с анализа воды.
Как правильно отобрать воду на анализ?
Тщательность, с которой вы выполните отбор пробы воды, в конечном счёте может существенно повлиять на цену установки. Вот общие рекомендации.
- Возьмите чистую пластиковую бутылку объёмом 1.5 л. Ни в коем случае не используйте бутылки, в которых ранее находились содержащие органические вещества жидкости (квас, пиво, кефирчик, уайт-спирит) или высокоминерализованные воды. Подойдут бутылки из-под питьевой воды. Идеальный вариант — купить новую бутылку там, где торгуют напитками на розлив.
- Если у вас скважина — пролейте её до постоянного состава. Рекомендации, как это сделать, должны предоставить ваши скваженщики. Некоторые наши заказчики рассказывали, что их скважина работала на излив по две-три недели.
- Откройте ближайший к скважине кран до любых существующих фильтров, баков и других устройств, могущих оказывать влияние на состав воды, и пролейте несколько минут, чтобы обновить воду в трубах.
- На два раза ополосните бутылку отбираемой водой, после чего налейте воду под самое горлышко, навинтите крышку, слегка сожмите бутылку с боков, чтобы вода потекла через край, и завинтите крышку до конца. Цель: набрать воду без воздушного пузыря.
- Доставьте воду в лабораторию в тот же день. Если нет такой возможности — храните воду в холодильнике не более двух суток.
Далее по анализу инженерами подбирается и рассчитывается система водоочистки, и если вас устраивает коммерческое предложение и вы его оплачиваете — к вам выезжают монтажники с оборудованием. Монтажникам от вас потребуются вход, выход и дренаж — откуда брать воду, куда её подавать и куда сливать. Особое внимание следует уделить именно канализации. Если у вас яма и вы её откачиваете — позаботьтесь о том, чтобы она могла одномоментно принять на себя 2-3 кубометра воды без последствий. Почему? Фильтры пропускают через себя грязную воду, грязь оседает на фильтрующем материале. Со временем ёмкость фильтрующего материала исчерпывается и он нуждается в обратной промывке — током воды снизу вверх вся грязь с него смывается в канализацию. На одну промывку может уходить от ста литров до полутора кубометров воды, в зависимости от типа фильтра и уровня загрязнения. И всё это количество сольётся в дренаж минут за 20 для кабинетных фильтров и где-то за час для засыпных колонного типа.
Примечание. Здесь и далее я буду приводить значения в масштабах частного домовладения.
Между прочим, если в Вашем септике применяется биологическая очистка, дренажная вода может убить её. Также монтажники потребуют с вас электрическую розетку поблизости (фильтры оснащены контроллерами — электронными управляющими мозгами, которые сами знают, когда пора начинать промывку). И ещё учтите, что эксплуатироваться любые фильтры должны при температуре не ниже +5 °C, а места занимают — в зависимости от модели — до двух квадратных метров по площади и до двух метров в высоту (хотя самый маленький фильтр со всей обвязкой может поместиться в кубический метр). Да, не забудьте про давление воды на входе! Если оно меньше 2-3 атмосфер — без повысительного насоса не обойтись. Для сравнения, системы горводоканалов обычно подают в квартиры воду под давлением около 4 атмосфер.
На входе перед фильтрами ставят грубую очистку — сетчатые фильтры, механику до 20 мкм — чтобы защитить более дорогое оборудование от проскоков песка, ржавчины и других крупных частиц. На выходе после установки рекомендуется монтировать финишную доочистку (обычно уголь — удаляет запахи, хлор и мелкие частицы). В самой дорогой комплектации ещё могут присутствовать ультрафиолетовая лампа для обеззараживания на выходе и защита от протечек на полу, но всё это опции. А вот если Ваша вода содержит много железа, то инженер может спроектировать водоочистку с применением баков, которые занимают значительное пространство.
А много железа — это сколько?
Вот теперь можно поговорить о вещах, более близких к моей профессии. И начнём мы с единиц измерения. В России и за рубежом, как ни парадоксально, применяются совершенно разные единицы измерения, хотя химия одна и та же. У нас приняты мг/л и мг-экв/л, у них — ppm.
мг/л (читается: миллиграмм на литр) — это масса исследуемых частиц, содержащаяся в одном литре раствора (а не растворителя!). Если мы исследуем ионный состав воды, то под массой частиц будет подразумеваться масса атомов одного вида. Например, 10 мг/л железа означает, что в 1 литре раствора у вас содержится 10 мг атомарного железа — того самого, у которого молярная масса, согласно таблице Менделеева, 56 г/моль. И не важно, в какой форме это железо — двухвалентный ион или трёхвалентный. Просто некая абстракция — железо, как оно есть в таблице Менделеева. А если мы измеряем содержание какой-то соли, то под массой частиц будет подразумеваться масса молекулы этой соли. Например, 10 мг хлорида натрия NaCl в 1 литре раствора.
мг-экв/л (читается: миллиграмм-эквивалент на литр) — с этого момента начинается особая чёрная магия. Иеремия Рихтер, немецкий химик, открыл закон эквивалентов (и попутно портал в ад) в 1792 году. Закон гласит: вещества реагируют в количествах, пропорциональных их эквивалентам, или m1Э2 = m2Э1. Попробуйте найти химика, который приходит в восторг, считая эквиваленты! Мне такие маньяки пока не встречались, хотя я занимаюсь химией уже 14 лет. Начнём издалека. Возьмём обычную реакцию между мелом и соляной кислотой:
Улетевший углекислый газ и воду отбросим, как несущественное, и выделим в этой реакции самое важное:
Ca 2+ + 2Cl — = CaCl2 (в ионной форме)
Теперь возьмём каждый из ионов и заставим его вступить в гипотетическую реакцию гидрирования с катионом водорода, невзирая на знак заряда (да, мы, химики, любим всякие извращения; а на самом деле — масса катиона водорода принята за единицу, и теперь нам нужно найти количество других ионов, эквивалентное этой единице).
1/2Ca 2+ + H + = CaH (фактор эквивалентности = 0.5, а эквивалент водорода — частица 1/2Ca 2+ )
Cl — + H + = ClH (фактор эквивалентности = 1, а эквивалент водорода — частица Cl — )
Итак, с одним катионом водорода может (условно) прореагировать либо один анион хлора, либо половинка катиона кальция. Численное выражение доли вещества, эквивалентной одному катиону водорода, называется фактором эквивалентности. Теперь мы можем сделать простой вывод:
1/2Ca 2+ = Cl — (1 эквивалент кальция = 1 эквиваленту хлора)
Представим, что мы титруем щёлочность соляной кислотой (об этих страшных словах — позже). С соляной кислотой могут реагировать самые разные соли (гидрокарбонаты, карбонаты, гидроксиды…) самых разных ионов (кальция, магния, натрия…). Как нам всё это выразить в одной единице измерения? Мы не имеем права использовать здесь уже знакомую нам единицу измерения мг/л, потому что просто непонятно — миллиграмм чего? Кальция? Магния? Их смеси? В каком соотношении? Зато с эквивалентами эта проблема снимается сама собой:
Cl — = 1/2Ca 2+ = 1/2Mg 2+ = Na + = 1/3Al 3+ и т.д.
Нам не важно, какой именно вид катиона или аниона мы оттитровали, но мы знаем, что одному эквиваленту потраченной соляной кислоты всегда будет соответствовать один эквивалент неведомой штуки, которая с этой кислотой способна прореагировать. Хорошо, с эквивалентом более-менее разобрались. А что же такое миллиграмм-эквивалент? Это масса одного эквивалента в миллиграммах. Грубо — считается по таблице Менделеева как молярная масса, умноженная на фактор эквивалентности. Для приведённого выше отношения это будет выглядеть так:
35.45 мг Cl — = 20.04 мг Ca 2+ = 12.15 мг Mg 2+ = 22.99 мг Na + = 8.99 мг Al 3+
Заметьте, молярная масса, например, кальция равна 40.08 г/моль, но с 1 граммом водорода может прореагировать только половинка кальция — 20.04 грамма. Вот эта цифра — 20.04 — и будет грамм-эквивалентом кальция. Или миллиграмм-эквивалентом. Или микрограмм-эквивалентом. Эта единица удобна тем, что если мы когда-нибудь выясним, какое именно соединение прореагировало в той реакции с соляной кислотой, мы всегда сможем умножить количество миллиграмм-эквивалентов на массу одного эквивалента — и перевести таким образом миллиграмм-эквиваленты в обычные миллиграммы для конкретного соединения. Итак, мг-экв/л — это количество миллиграмм-эквивалентов вещества в одном литре раствора.
ppm (читается: пи-пи-эм, parts per million) — число частиц на миллион. Показывает, сколько исследуемых растворённых частиц находится в одном миллионе частиц раствора (не растворителя!). Единица измерения применяется на Западе почти повсеместно. Соответствует нашему мг/л (потому что миллиграмм — это, вроде как, тоже миллионная часть от литра, при условии, что плотность раствора равна 1.00, но при таком разбавлении изменением плотности всё равно можно пренебречь).
мкСм/см (читается: микросименс на сантиметр) — единица измерения удельной электропроводности воды. Берут два электрода, погружают в воду. На один подают известное количество тока, на втором измеряют, сколько дошло. Поскольку в водном растворе носителями заряда являются ионы, то по количеству перенесённых с одного электрода на другой электрончиков можно сделать вывод об общей доле ионов в растворе. Сименс — единица, обратная сопротивлению (1 См = 1 Ом -1 ). Измерение удельной электропроводности иногда может дать достаточно точное представление об общем солесодержании воды. Если вода относительно чистая, то условно можно считать, что 1 мкСм/см ≈ 0.5 мг/л солей. И вот мы вплотную подошли к сущности анализа воды.
Тут надо отвлечься и уточнить, что видов анализов воды — масса. Навскидку, есть химический и микробиологический. А ещё органолептический, радиометрический, несть им числа. Я занимаюсь непосредственно химическим анализом воды, о нём и поговорим. В России документ, регламентирующий качество воды для хозяйственно-бытовых нужд, называется «СанПиН 2.1.4.1074-01». И контролируемых параметров там — тьма тьмущая. Здесь уместно отметить, что такого понятия, как «техническая вода», ни в одном официальном документе не существует. Более того, то, что обычно в простонародье подразумевают под технической водой — это как раз вода, которую можно пить, но нельзя использовать в той самой технике. Подчас на производство или в паровой котёл нужно подавать полностью обессоленную (деионизованную) воду.
Смотреть в лаборатории все параметры, подразумеваемые СанПиНом — сумасшествие. Во-первых, на анализ одной пробы уйдёт тогда неделя (тогда как анализ по 12 показателям делается за 2 часа). А во-вторых, существующие фильтрующие материалы всё равно очищают воду только от конечного числа загрязнителей. И, конечно, большая часть указанных в СанПиНе загрязнителей практически не встречается в обычных природных водах или встречается в таком количестве, что заведомо проходит по нормам. Пойдём по порядку со всеми комментариями (по какому именно порядку — я ещё не решил).
Железо. Есть практически во всех подземных водах, а вот в поверхностных — реках, озёрах — обнаружить его можно нечасто. Бывает в двух формах: растворимое, или двухвалентное Fe 2+ и окисленное, или трёхвалентное Fe 3+ . Соли двухвалентного железа прекрасно растворяются в воде (железный купорос FeSO4 ∙ 7H2O многие садоводы найдут в профильных магазинах), однако кислородом воздуха очень быстро окисляются и переходят в соединения трёхвалентного железа. А вот соединения трёхвалентного железа в воде не растворимы — ржавчину все видели, а ржавчина это смесь Fe2O3 ∙ nH2O и Fe(OH)3.
FeCl3 прекрасно в воде растворяется, после чего гидролизуется до оксихлорида и выпадает в осадок. То же самое касается других растворимых соединений трёхвалентного железа — они подвержены гидролизу в водном растворе с образованием нерастворимых продуктов.
Поэтому в поверхностных источниках железа мало: оно если и было изначально, то быстро окислилось при контакте с атмосферой и ушло в ил. Помимо атмосферы, естественным врагом двухвалентного железа являются железобактерии, которые живут за счёт энергии, выделяемой при окислении ими двухвалентного железа. Зато у него есть верный союзник в виде сероводорода. В подземных водах часто содержится сероводород в большом количестве, а он является сильным восстановителем и не даёт железу окисляться даже при контакте с атмосферой. Вообще, зависимость формы железа в растворе от окислительно-восстановительного потенциала и водородного показателя наглядно отображена в диаграммах Пурбе. Железо является одним из микроэлементов и необходимо организму человека (суточная потребность — 10 мг ), и усваивается, в том числе, из воды. Конечно, содержание железа сказывается на органолептических свойствах воды (если его больше 1-2 мг/л), а избыточное его поступление в организм может спровоцировать разные отклонения в здоровье. Ну, это всегда так. Всё есть лекарство и всё есть яд, всё дело в дозе, сказал Парацельс.
ПДК железа общего в воде хозяйственно-бытового назначения составляет 0.3 мг/л. В городском водопроводе с труб при ржавлении летит примерно 0.10…0.15 мг/л (там, где я живу). Удаляют железо просто: сначала окисляют, чтобы наверняка (напомню, окисленное железо в воде не растворимо), затем полученные частички коагулируют (укрупняют), и всю эту конструкцию ловят механическим способом — на слое загрузки. Существуют разные каталитические загрузки, на поверхности которых все указанные процессы и происходят. Представляют они собой песок, покрытый слоем оксида марганца — того самого катализатора окисления железа — и нуждаются в периодической реагентной промывке раствором перманганата калия (нет, соединения марганца не смываются с загрузки и не попадают в очищенную воду — ну, если, конечно, вы не захотите смешать каталитический материал с лимонной кислотой). Есть и безреагентные загрузки, но перед ними требуется предварительное окисление железа, а уж каким способом — атмосферным воздухом, озоном или хлором — решит инженер. Если в Вашей воде железа до 5 мг/л — считайте, что Вам крупно повезло: установка будет подешевле. Если железа 10 мг/л — уже дорого. А вот 30 мг/л и выше — можете распрощаться с планируемой поездкой в тёплые страны. Такая установка может стоить несколько сотен тысяч рублей. Вообще, основная стоимость большинства полупромышленных систем фильтрации как раз зависит от концентрации железа. Чем его больше — тем дороже. Поэтому так важно тщательно пролить воду перед отбором пробы — застоявшаяся в металлических трубах вода может набрать железа, и инженер предложит вам по анализу такую установку, на которую у Илона Маска денег не хватит. Но и это ещё не всё. Отдельно стоит упомянуть про так называемое органическое железо — комплексные органические соединения, содержащие в составе молекулы атом железа (как правило, гуматы — комплексы гуминовых кислот). Выбить железо из таких комплексов нелегко, и оно не окисляется на воздухе. Удаление из воды органического железа может быть затруднительным.
Марганец. От марганца на сантехнике появляется серый налёт, поэтому нормируют его жёстко. Организму человека этот микроэлемент тоже необходим (суточная потребность 2 мг [1] ). Из воды легко усваивается. Ещё содержится в свёкле и половине овощей вообще. Валентностей у марганца целых семь, подробно рассматривать не имеет смысла. Двухвалентный марганец хорошо растворим, трёх- и четырёхвалентный обычно подвергается гидролизу и выпадает в виде нерастворимых гидроксидов. В отличие от железа, марганец в поверхностных водах встречается чаще. Особенно если это колодцы, и в подземной воде, питающей их, содержится какой-нибудь двухвалентный ион марганца. Дело в том, что марганец так вот запросто атмосферным воздухом не окисляется. Может захватываться осаждающимся железом и удаляться совместно с ним. Загрузки все те же самые, ибо принцип тот же: окисление, укрупнение и механическая фильтрация. ПДК 0.1 мг/л.
Жёсткость. Жёсткость замыкает тройку параметров, на которые нацелены почти все полупромышленные системы очистки воды. Да-да, есть фильтры-обезжелезиватели (удаляют железо, марганец и некоторые другие тяжёлые металлы) и фильтры-умягчители (удаляют жёсткость). Безусловно, есть другие типы фильтров, которые работают, например, по окисляемости, но в конечном итоге для промышленных нужд вам предложат обратный осмос с предочисткой, тогда вода на выходе будет как по ГОСТу для лабораторий: 3…5 мкСм/см. Но мы отвлеклись. В школе вам рассказывали, что жёсткость — это совокупность ионов кальция и магния. Именно они выпадают в виде накипи при кипячении воды. На самом деле, такое определение не совсем корректно. Да, значительную долю жёсткости составляют ионы кальция и магния, но вообще жёсткость — это сумма всех щелочноземельных ионов, а также некоторых двухвалентных ионов тяжёлых металлов. Цинк, барий, кадмий, даже двухвалентное железо — это всё жёсткость. Другое дело, что химик в лаборатории будет маскировать ионы двухвалентного железа при измерении жёсткости. Зато кадмий вполне себе на величине жёсткости отразится. Но поспешу вас успокоить: ионов кальция в составе жёсткости большинство — как правило, процентов 80, и ещё процентов 15 магния. Нормируют жёсткость исключительно для снижения количества накипи в чайниках, а особо рьяно — в отраслевых стандартах для всяких котельных, где жёсткости в воде быть не должно вообще. Иногда вы можете услышать, что использовать в хозяйстве нужно исключительно мягкую воду, а жёсткая, якобы, вредна. Жёсткая вода увеличивает затраты на мыло, уменьшает срок жизни стиральной машинки… Вас могут начать убеждать, аргументируя тем, что кальций из воды всё равно не усваивается, и организм получает его из молока и сыра. Это некорректно.
источник

