Если вам скажут, что проточная вода может не содержать железа, не верьте. Металл попадает в колодцы и скважины из растворенных горных пород (их частицы содержатся в грунте), из сточных вод сельскохозяйственных и промышленных предприятий, накапливается при прохождении жидкости через центральную систему водоснабжения (состояние труб зачастую оставляет желать лучшего). В такой ситуации анализ воды на железо становится насущной необходимостью.
При этом ВОЗ до сих пор не установила рекомендованных норм: по мнению ученых, железо не окажет негативного влияния на здоровье человека, даже если злоупотреблять «насыщенной» водой. Допустимый порог (0,3 мг/л) был обозначен СанПином на основании вкусовых, а не медицинских показателей.
Это интересно: в организме взрослого человека содержится около 5 граммов железа, которое входит в состав гемоглобина, миоглобина и различных ферментов. Без этого элемента невозможен нормальный процесс кроветворения. Часть железа «складирована» в печени и селезенке – этот резерв используется в случае истощения организма.
В воде содержится одно или несколько соединений железа:
- Двухвалентное (растворенное);
- Трехвалентное (в состоянии взвеси);
- Органическое (соединенное с другими веществами);
- Бактериальное (продукт жизнедеятельности некоторых микроорганизмов);
- Коллоидное (с микроскопическими частицами).
Наличие «добавок» не всегда видно невооруженным глазом, зачастую выявить проблему может только экспресс-анализ воды на железо.
Определить наличие примеси можно самостоятельно. Первый тревожный звоночек – появление ярко выраженного металлического привкуса (при сильном превышении нормы этот вкус ощущается даже в кофе или чае). На стенках посуды и поверхности сантехники проступает желтоватый или рыжий налет, который сложно оттереть без абразивных средств. Белое белье после стирки приобретает грязноватый оттенок, а цветное быстро теряет яркость красок. При этом внешний вид воды может вовсе не вызывать подозрений.
Важно! Если вы обустроили скважину или колодец на участке, сделать анализ воды на железо нужно через 2-3 недели после начала ее эксплуатации. Впоследствии процедуру можно проводить раз в 2 года (либо при изменении цвета или вкуса воды).
Первичный анализ воды на железо в домашних условиях можно провести несколькими способами:
- Смешать 25 мл воды и по 1 мл сульфосалициловой кислоты, аммиака и нашатырного спирта. Если через 15-20 минут раствор окрасится в ярко-желтый цвет, в нем есть примесь железа.
- Смешать слабый раствор марганцовки с пробой воды. Тревожный «звоночек» – изменение цвета на желтовато-бурый оттенок.
- Использовать экспресс-анализ воды на железо («набор аквариумиста»). Смешайте реагент с пробами жидкости по инструкции и определите степень загрязнения по интенсивности цвета.
- Трехвалентное железо можно выявить простой процедурой – отстаиванием воды. Железо вступает в реакцию с кислородом и выпадает в виде красновато-бурого осадка.
Более подробный анализ воды на железо (общее либо двухвалентное) можно сделать в аккредитованных лабораториях. В идеале эту процедуру нужно проводить на месте – при транспортировке может начаться процесс окисления, что исказит результаты. Если такой возможности нет, нужно провести забор проб по всем правилам:
- Используйте чистую пластиковую или стеклянную посуду объемом не менее 1,5 литра (можно взять бутылку от негазированной минералки).
- Наполняйте емкость до самого верха и тщательно закручивайте пробку, чтобы перекрыть доступ воздуха.
- Доставьте образцы в течение 2 часов. Этот срок критичен при выявлении ионов железа – именно они влияют на образование накипи.
Анализ на общее железо выявляет остаток металла в воде (то, что остается после реакции элемента с кислородом). Именно этот осадок отвечает за ржавые потеки на сантехнике и желтоватый налет на посуде.
В воде из скважин и колодцев чаще всего выявляется двухвалентное (растворенное) железо. Избавиться от него можно с помощью довольно сложной системы фильтров. На входе устанавливают ионообменные картриджи, в которых происходит процесс окисления металла и образование твердого осадка. Получившийся «песок» собирается в фильтре (картриджи нужно периодически менять). Более дорогая и эффективная система – фильтры с обратным осмосом – под высоким давлением прогоняет загрязненную воду через специальные мембраны, а все загрязнения и отходы утилизирует в канализацию.
От трехвалентного железа можно избавиться с помощью аэратора – открытого резервуара, в котором отстаивается вода. Для ускорения процесса окисления жидкость насыщают кислородом при помощи компрессора. Простым аналогом системы может стать обычное ведро: наберите воду, а через сутки аккуратно слейте примерно две трети.
Для бытовой очистки воды можно использовать активированный уголь. Заверните таблетки в вату и пропустите жидкость сквозь импровизированный фильтр.
Важно! Не забывайте, что домашние процедуры очистки могут носить лишь временный характер. Чтобы не подвергать здоровье риску, своевременно проводите анализ воды на железо и используйте профессиональные системы фильтрации.
источник
Чтобы отправить ответ, вы должны войти или зарегистрироваться
- Иван
- Baccho Testis
- Неактивен
- Откуда: Queenstown
- С нами с: 2014-01-20
- Сообщений: 21 808
Определение железа в воде важный этап в процессе домашнего винокурения. Определить содержание железа в воде можно несколькими способами, например, можно использовать сульфосалициловую кислоту с аммиаком, также можно воспользоваться набором для аквариумистов, но самый универсальный и простой способ — марганцовка.
Например, при использовании сульфосалициловой кислоты вряд ли получится определить содержание двухвалентного железа и наличие железобактерий. При использовании набора аквариумиста получится определить наличие только двухвалентного железа. А при помощи перманганата калия можно определить наличие двухвалентного, трехвалентного железа и железобактерии.
Двухвалентное железо
FeO — оксид железа(II) сложное неорганическое соединение двухвалентного железа и кислорода в воде отстоявшейся воде может выпадать в виде черного осадка.
Трехвалентное железо
Fe2O3 — оксид железа(III) амфотерный оксид с большим преобладанием основных свойств. Красно-коричневого цвета.
Железобактерии
Бактерии, способные окислять двухвалентное железо (Fe2+) до трёхвалентного (Fe3+) и использовать освобождающуюся при этом энергию на усвоение углерода из углекислого газа или карбонатов.
Если у вас есть унитаз и вы не обрабатываете его бачок года по два-три, загляните в него и проведите руками по стенкам. Если почувствовали «слизь» — это колонии железобактерий. Это говорит о том, что в вашей воде достаточно высокое содержание железа и дальнейшие действия можно пропустить. Делайте нормальную фильтрационную систему и очищайте воду. Если у вас уже стоит фильтр типа обратного осмоса, скорее всего у вас нет железа в воде.
Как определить содержание железа в воде?
Нужно подготовить слабый раствор перманганата калия, его можно купить в аптеке уже в разведенном виде, но потребуется немного дистиллированной воды чтобы развести посильней, необходимо сделать слабый раствор.
Потребуется пара любых небольших емкостей одного цвета. На фотографиях ниже несколько, так как проводился эксперимент.
1 — контрольная емкость с дистиллированной водой.
2 — вода из скважины в саду, глубина 20 метров, 200 метров от берега Волги
3 — вода из городского крана горячего водоснабжения
4 — вода из городского крана холодного водоснабжения
5 — вода из бачка унитаза, где на стенках есть небольшие отложения трехвалентного железа (взято из середины бачка, стенки не подвергались механическому воздействию)
1 Контрольная емкость, это будет «эталон».. не путать с этанолом!
В каждую емкость заливается ровное количество слабого раствора перманганата калия (в моем случае 1 кубик из шприца).
В контрольную емкость доливается 1 кубик дистиллированной воды, во все последующие доливается ровно по 1 кубику испытуемой воды.
Для ускорения процесса окисления все емкости были поставлены на водяную баню, просто в миску с кипятком и стояли там до остывания до комнатной температуры.
К сожалению, моя камера не может передать точные цветовые оттенки (в живую все наглядней), но если у вас хороший монитор, вы увидите изменения в трех пузырьках 3,4,5 Цвет изменился ближе к желтовато-бурому. Это говорит о том, что в воде есть железо и такая вода не подойдет чтобы разводить спирт и делать на ней зерновые заторы.
Для более понятного восприятия, сделал с фотографию на ручной настройке камеры и на копии просто подкрутил цветовой уровень по всей фотографии, так лучше видно отличие.
Даже совсем небольшое содержание железа можно определить таким простым способом. Дело в том, что перманганат калия является достаточно сильным окислителем, чтобы окислить содержащееся в воде железо до его трехвалентного состояния, что и вызывает изменение цвета раствора до появления бурого или желто-бурого (зависит от количества железа)
Вот такая картина вырисовывается на следующий день, даже в дистиллированной воде (канистра из магазина) произошла реакция окисления, это говорит о том, что в ней тоже было достаточно для видимой реакции ионов железа. А вот в воде из скважины самая наименьшая реакция, хотя и появился небольшой осадок, по всей вероятности это какие-то коллоидные частицы, возможно просто микроскопические частицы силикатов из глины, так как почва глинистая.
источник
Цель работы: оптическим методом анализа, используя ФЭК, определить концентрацию Fe 2+ , Fe 3+ , общее содержание железа в исследуемой пробе воды и контрольном растворе.
В природных водах железо может находиться в растворенном, коллоидном и взвешенном состоянии, может входить в состав минеральных и органических соединений. В подземных водах преобладают соединения двухвалентного железа Fe(HCO3)2, FeSO4, образующиеся при растворении железосодержащих пород. Эта форма содержания железа устойчива в присутствии растворенного CO2 и в отсутствии кислорода. При выходе подземных вод на поверхность наблюдается окисление Fe 2+ в Fe 3+ , сопровождающееся образованием трудно растворимого Fe(OH)3 : 4Fe 2+ + 3 O2 + 6 H2O = 4 Fe(OH)3
Гидроксид железа (III) может содержаться в поверхностных водах в виде коллоидного раствора, но под влиянием растворенных электролитов он коагулирует. Поэтому содержание железа в поверхностных водах незначительно(сотые или десятые доли мг/л). Воды северных районов (болотистые) содержат органическую форму железа – гуматы, обусловливающие их цветность.
Содержание железа в питьевой воде не должно превышать 0,3 мг/л, т.к. при большей концентрации появляется неприятный (железистый) привкус и бурый оттенок. Нежелательно железо во многих производственных водах. Так, при содержании железа в охлаждающей воде наблюдается массовое развитие железобактерий, вызывающих обрастание и закупорку труб. Вода, используемая для питания паровых котлов, не должна содержать железа более 100 мкг/л. Концентрация железа выше 1 мг/л губительны для рыб.
Выбирая метод обезжелезивания, следует предварительно определить форму содержания железа.
Концентрацию железа в воде определяют колориметрическим методом.
Качественное определение железа.
Растворы солей железа (II) окрашены в бледно – зеленый цвет.
Рассмотренная реакция наиболее характерна для Fe 2+
Растворы солей железа (III) имеют желтую окраску.
1. Роданид аммония NH4SCN или калия KSCN дает с ионами Fe 3+
кроваво – красное окрашивание роданидов железа.
Fe 3+ + 3 SCN — = Fe(SCN)3 или [Fe(SCN)6] 3-
Интенсивность окраски пропорциональна концентрации ионов Fe 3+ . Состав продуктов реакции зависит от концентрации роданида.
Это одна из важнейших и наиболее чувствительных реакций на Fe 3+ . Роданидным методом можно определить 0,05 – 2,00 мг Fe 3+ в 1 л воды. Предел обнаружения 0,05 мг/л.
Однако она не всегда надежна, так как ряд веществ, в частности ионы F — , образуют более прочные комплексы, которые мешают появлению окраски. (Кнест.[Fe(SCN)6] 3- = 5,9 ∙ 10 — 4 , Кнест .[FeF4] — = 4,8 ∙ 10 — 16 )
Качественные определения с приближенной количественной оценкой.
Ход работы: В пробирку наливают 10 мл исследуемой воды, 2 капли концентрированной HCl, несколько кристаллов персульфата аммония (NH4)2S2O8 и 0,2 мл 50%-ного NH4SCN. После внесения каждого реактива содержимое пробирки перемешивают. Приближенную массовую концентрацию общего содержания железа в воде определяют в соответствии с таблицей №1.
Окрашивание при рассмотрении сбоку
Окрашивание при рассмотрении сверху вниз
Едва заметное желтовато – розовое
Очень слабое желтовато – розовое
Очень слабое желтовато – розовое
Слабое желтовато – розовое
Слабое желтовато – розовое
Светло желтовато – розовое
Светло – желтовато – розовое
Сильное желтовато – розовое
Светло – желтовато – красное
Результаты опытов записать в виде таблицы:
источник
Ржавые потеки на раковине, унитазе или пластиковом трубопроводе свидетельствуют о том, что в воде присутствует железо, которое, окисляясь на воздухе, оставляет после себя следы соответствующего цвета.
Железо присутствует в природной воде изначально и человек употребляет его с водой. Плохо это или хорошо, когда «хорошо» переходит в «плохо», как определить этот предел количественно – ответы на эти и другие вопросы вы узнаете из этой статьи.
Врачи давно обратили внимание на то обстоятельство, что причиной усталости и плохого настроения, как правило, является дефицит железа в организме.
Дефицит этого важного для здоровья микроэлемента наблюдается у людей обоих полов в разные периоды жизни. Поэтому если вы замечаете, что у вас часто меняется настроение, и для этого нет видимых причин, то необходимо начать прием железосодержащих продуктов или препаратов.
Помимо того, что железо влияет на трудоспособность и настроение человека, оно имеет ряд других преимуществ:
- Железо является наиважнейшим элементом, участвующим в процессе формирования гемоглобина. Учитывая, что ежедневно происходит потеря большого количества железа в виде пота, мочи и кровотечений (например, менструальные выделения или порезы во время бритья), становится понятным, что это сказывается на качестве и количестве крови. Кроме того, железо участвует в транспортировки кислорода в клетки организма, что важно для правильного функционирования органов.
- Если в организме чувствуется недостаток железа, то мышцы становятся слабыми и дряблыми. Для спортсменов железо является важной составляющей эффективной тренировки. Железо помогает мышцам восстановиться в кратчайшие сроки.
- Мозг, так же как и мышцы, зависит от количества получаемого организмом железа. Если его недостаточно, то кровь не получает необходимого количества кислорода, от чего в первую очередь страдают мозговые клетки. Если же кислорода достаточно, то улучшается память, появляется стремление к новым знаниям. Врачи убеждены, что дефицит железа может повлиять на психическое здоровье человека.
- Крепкий иммунитет напрямую зависит от железа. Частые заболевания простудой и гриппом, сопровождающиеся упадком сил и вялостью, свидетельствуют о том, что организму не хватает этого микроэлемента. Чем ниже уровень железа, тем чаще приходится бороться за свое здоровье.
- Модницы давно поняли, что невозможно считаться красивой без ухоженных волос, чистой кожи и крепких ногтей. И если кератин временно делает волосы блестящими, то кожа и ногти будут выглядеть тусклыми и безжизненными без необходимого для их красоты железа.
- Железо помогает тем, кто хочет избавиться от лишнего веса либо желает держать его под контролем. Если его недостаточно, то организм не будет тратить энергию на сжигание жира, и ни диеты, ни тренировки не приведут к нужному результату.
Поэтому важно вовремя выявить этот избыток и устранить его. Как это сделать самостоятельно — читайте далее.
При высоком содержании в воде серной и соляной кислоты на вымытой посуде остаются зеленые или бурые пятна. Также о неудовлетворительном качестве воды говорит ее запах: рыбный, землистый или древесный. Это значит, что в своем составе она содержит органические соединения.
Если на серебряной посуде и на раковине остаются темноватые пятна, то вода из вашего крана содержит сероводород.
Возникновение пены при наливании воды в алюминиевую посуду говорит об избыточной концентрации щелочных соединений в ней.
Довольно часто встречающийся признак загрязненной воды – ее металлический привкус, показывающий высокое содержание в ней железа. А вода с красноватым и бурым оттенком свидетельствует о том, что ваш водопровод ржавый и старый, поэтому в трубах происходит окисление воды железом.
Мутная и грязная вода означает, что в ней содержится большое количество воздуха или метана.
Во многих городах существуют СЭС или мобильные лаборатории, изучающие качество воды, имеющие возможность проводить экспресс анализ воды на железо. Вы можете связаться с такой лабораторией и заказать анализ воды в вашем доме. Вам будет дан полный и точный ответ по этому вопросу.
В аккредитованных лабораториях проводится анализ воды на железо по ГОСТ 4011, который регламентирует порядок определения в воде двухвалентного железа (которое окисляется до ржавчины F2O3) и на общее железо.
Анализ воды на железо из скважины лучше всего производить непосредственно на месте, так как хранение и транспортировка образцов для анализа может привести к окислению железа при доступе воздуха и к выпадению окисла в осадок.
Если необходимо выполнить анализ воды на железо в лаборатории, отбираются пробы. Для проведения анализа потребуется не менее полутора литров воды, которые должны быть отобраны в чистую стеклянную или пластиковую тару. Очень важно, чтобы тара была чистой и не содержала остатков (даже запаха) жидкостей, которые в ней хранились. Хорошей посудой для отбора проб для анализа будет пластиковая бутылка от негазированной минеральной воды. Образец доставляется в лабораторию в течении двух часов.
Наиболее существенным в практическом значении является анализ воды на железо-ионы, потому что именно они влияют на образование накипи на посуде и нагревательных ТЭНах. И потеки ржавчины на сантехнике, в большей степени, зависят от активного железа, которое окисляется в воздушной среде.
Польза железа в воде для организма неоспорима, поэтому полностью избавляться от него с помощью фильтрации так же не стоит. Идеально очищенную с помощью обратного осмоса воду для этого специально минерализуют. Остаток железа в воде определяет анализ воды на общее железо.
Смягчать воду для бытовых нужд, безусловно, нужно (борьба с накипью, солями тяжелых металлов и азотными соединениями), но к содержанию в воде железа следует относиться бережно. Выдержать паритет в этом вопросе поможет своевременный и качественный анализ воды на железо, произведенный аккредитованной лабораторией.
источник
ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ
Лабораторная работа № 2.
ВОДОПОДГОТОВКА.
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ РАСТВОРЕННОГО ЖЕЛЕЗА В ВОДЕ.
Цель работы: определить содержание железа в сточной или природной воде фотоколориметрическим методом.
Общие сведения.
Железо (Ferrum) – принадлежит к 8 группе химических элементов периодической системы Д.И. Менделеева, атомная масса 55,847, атомный номер 26, плотность 7,874 г/см 3 , серебристо – белый блестящий пластичный металл, температура плавления 1535 o С. Железо достаточно распространено в земле (4 место) находится на 2 месте после алюминия; процентное содержание 4,65 %.
Главными источниками попадания соединений железа в поверхностные воды являются процессы химического выветривания горных пород, сопровождающиеся их механическим разрушением и растворением. В процессе взаимодействия с содержащимися в природных водах минеральными и органическими веществами образуется сложный комплекс соединений железа, находящихся в воде в растворенном, коллоидном и взвешенном состоянии. Значительные количества железа поступают с подземным стоком и со сточными водами предприятий металлургической, металлообрабатывающей, текстильной, лакокрасочной промышленности и с сельскохозяйственными стоками. В питьевой воде железо может содержаться также из-за плохого состояния водопроводов и применения коагулянтов на основе солей железа.
Содержание железа в поверхностных водах суши составляет десятые доли миллиграмма, вблизи болот – единицы миллиграммов. Наибольшие концентрации железа (до нескольких десятков и сотен миллиграммов в 1 дм 3 ) наблюдается в подземных водах с низкими значениями pH. Являясь биологически активным элементом, железо в определенной степени влияет на интенсивность развития фитопланктона и качественный состав микрофлоры в водоеме. Концентрация железа подвержена сезонным колебаниям. Обычно в водоемах с высокой биологической продуктивностью в период летней и зимней стагнации заметно увеличение концентрации ионов железа в придонных слоях воды. Предельно допустимая концентрация общего железа в воде водоемов 0.5 мг/л.
Содержание железа в воде выше 1-2 мг Fe 3+ в 1 дм 3 значительно ухудшает органолептические свойства, придавая ей неприятный вяжущий вкус, и делает воду малопригодной для использования в технических целях. По органолептическим показателям воды содержание железа в питьевой воде не должно превышать 0.3 мг/л (а по нормам ЕС даже 0.2 мг/л). Лишь в отдельных случаях при использовании подземных вод без установок по обезжелезиванию по согласованию с органами санитарно-эпидемиологической службы содержание железа в воде, поступающей в водопроводную сеть, допускается до 1 мг/л.
В поверхностных пресных водах железо содержится в очень не больших количествах, и, как правило, в трехвалентной форме. Повышенное содержание железа наблюдается в болотистых водах, до нескольких миллиграммов на литр, в таких водах повышенное содержание гумусовых веществ, которые соединены с трехвалентным железом. При высоких значениях pH железо в воде находится в коллоидной форме оксида железа Fe(OH)3. В подземных водах с низкими значениями pHи при минимальном содержании растворенного кислорода железо присутствует в растворенной двухвалентной форме. Трехвалентное железо при определенных условиях также может присутствовать в воде в растворенном виде как в форме неорганических солей (например, сульфатов), так и в составе растворимых органических комплексов.
При содержании в воде железа в концентрациях выше 0.3 мг/л вода после непродолжительного контакта с воздухом окисляется кислородом и становится желтовато – бурого цвета. Такая вода вызывает появление ржавых подтеков на сантехнике, отложения в котельном и бойлерном оборудовании. При концентрациях выше 1 мг/л вода мутная окрашивается в желто-бурый цвет при не длительном контакте с воздухом. Такая вода не допустима для использования, как в питьевых, так и в технических целях.
Железо человек получает в основном с пищей, из воды – максимально 10%. Также возможно попадание железа из воздуха, при этом вероятно возникновение профессиональных заболеваний. ВОЗ не дает рекомендуемой величины потребления железа по показаниям здоровья. В больших количествах железо, как и любое другое химическое вещество, способно вызвать в организме человека нарушения и даже патологии.
Виды железа, содержащегося в воде.
Как правило, в воде встречается несколько видов железа (таблица 1).
Двухвалентное железо (Fe +2 ) –в этой форме железо находится в растворенном состоянии. Иногда при определенных значениях pH гидроксид железа Fe(OH)2, выпадает в осадок.
Трехвалентное железо (Fe +3 ) —Хлорид (FeCl3) и сульфат (Fe2(SO4)3) – в растворимой форме, гидроксид железа Fe(OH)3 – в нерастворимом виде (существуют исключения при низком уровне pH).
Органическое железо – существует в различных комплексах, растворимых или в коллоидной форме. Органическое железо трудно удалить из воды. Органическое железо бывает следующих видов:
· Растворимое органическое железо. Способно связывать и удерживать кальций и другие металлы. Некоторые органические молекулы связывают железо в сложные растворимые комплексы – хелаты. Пример, таких органических соединений: порфириновая группа гемоглобина крови (удерживает железо), хлорофилл (удерживает магний), гуминовая кислота.
· Бактериальное железо. Существуют бактерии, использующие растворенное железо для жизни, они получают энергию, преобразуя двухвалентное железо в трехвалентное.
· Коллоидное железо. Коллоиды –частицы размером менее 1 микрона, которые не растворяются в воде, но трудно фильтруются из-за малого размера. К коллоидным частицам также относятся крупные органические молекулы (танины, лигнины). Коллоидные частицы обладают высоким поверхностным зарядом, поэтому они отталкивают друг друга и не укрупняются, образуя в воде суспензии, находящиеся во взвешенном состоянии, вода становится мутной.
Таблица 1 – Виды железа, содержащиеся в воде.
| Тип железа | Вода из-под крана | Вода после отстаивания |
| Двухвалентное | Чистая | Красно-бурый осадок |
| Трехвалентное | Окрашена | Красно-бурый осадок |
| Коллоидное | Желто-бурая | Не образует осадка, Не фильтруется |
| Растворенное органическое | Желто-бурая | |
| Бактериальное | Радужная пленка, желеобразные образования в водопроводной системе. |
Процесс удаления из воды железа называется обезжелезиванием. Очистка воды от железа – одна из самых сложных задач в водоподготовке. Одного универсального экономически оправданного метода очистки, который можно было бы применить во всех случаях для любой воды, не существует. Основные методы обезжелезивания:
· Окисление (реагентное, каталитическое). В результате окисления загрязнения осаждаются (с помощью коагулянтов или без них), потом фильтруются с помощью специальных систем очистки воды.
· Мембранные методы (осмос, обратный осмос, нанофильтрация)
Поскольку железо образует устойчивые окрашенные соединения, для его определения можно использовать фотоколориметрические методы.
Фотоколориметрия. Теоретические основы метода.
Закон Бугера – Ламберта — Бера
В основе оптических методов анализа лежит эффект избирательного поглощения света определенной длины волны веществом. Если вещество облучается видимым светом, этот раздел оптических методов анализа называется фотоколориметрией.
При прохождении потока излучения через частично поглощающую среду интенсивность прошедшего потока I согласно закону Бугера – Ламберта — Бера равна
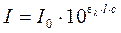
где I – интенсивность падающего потока;
ελ – молярный коэффициент поглощения при данной длине волны;
l – толщина поглощающего слоя (кюветы);
с – концентрация поглощающего вещества, моль/дм 3 .
Или в логарифмической форме:

Величину lg(I/I) в (2), характеризующую поглощающую способность вещества в растворе, называют оптической плотностью. В аналитической практике, стремясь подчеркнуть сущность процесса, лежащего в основе фотометрического определения, а именно поглощение квантов электромагнитного излучения оптического диапазона аналитической формой, эту величину называют поглощением, или светопоглощением и обозначают буквой А (absorption) либо D (density).
Закон Бугера – Ламберта — Бера: оптическая плотность раствора прямо пропорциональна концентрации вещества и толщине поглощающего слоя. Серию аналитических определений выполняют при постоянной толщине поглощающего слоя, тогда оптическая плотность линейно зависит от концентрации (рисунок 1).
Коэффициент линейной регрессии зависимости А = f(С) представляет собой молярный коэффициент поглощения ελ = tg a.
Рисунок 1. – зависимость оптической раствора плотности от концентрации.
Обратите внимание, что эта прямая линия проходит через начало координат. Для раствора поглощающего вещества при постоянных концентрациях и толщине поглощающего слоя оптическая плотность зависит от длины волны, поэтому измерения проводят при длине волны, соответствующей максимальному поглощению.
Приборами для фотоколориметрии служат фотоэлектроколориметры (ФЭК), характеризующиеся простотой оптической и электрической схем. Большинство фотометров имеет набор из 10-15 светофильтров и представляет собой прибор, в которых пучок света от источника излучения (лампа накаливания, редко ртутная лампа) проходит через светофильтр и проходит через кювету с исследуемым раствором или раствором сравнения (рисунок 2).
1 – источник света, 2 – щель, 3 – монохроматор (светофильтр),
4 – измерительная ячейка (анализируемый образец, образец сравнения),
5 – детектор, 6 – усилитель, 7 – регистрирующее устройство
(графическое, визуальное, цифровое)
Рисунок 2 – Блок-схема фотоэлектроколориметра (упрощенная)
Количественное определение вещества по светопоглощению основано на применении закона Бугера — Ламберта — Бера. Концентрацию можно определить, пользуясь методом градуировочного графика А = f(C), методом сравнения или методом добавок. Погрешности определения составляют около 5%.
Для перевода вещества в окрашенную форму используются химические реакции. Обязательное требование к реакциям, используемым в количественном анализе – они должны протекать избирательно, быстро и полностью воспроизводимо. Окраска образующейся аналитической формы должна быть устойчивой во времени и к действию света, а поглощение раствора, несущее информацию о концентрации поглощающего вещества, должно подчиняться физическим законам, связывающим поглощение и концентрацию, конкретно – закону Бугера – Ламберта – Бера.
Практическая часть.
Ион Fe 3+ с роданид-ионом в зависимости концентрации ионов железа и роданид-ионов дает ряд окрашенных в кроваво-красный цвет комплексов:
Число роданид-анионов n в комплексе железа может изменяться от 1 до 6. В данной работе берется избыток роданид-ионов, при этом образуются комплекс FeSCN6 3- .
Для построения градуировочной кривой используются стандартные растворы, отличающиеся друг от друга по концентрации не менее чем на 10 %.
Растворы готовят непосредственно перед колориметрированием, так как окраска растворов неустойчива.
По серии стандартных растворов соли железа строят градуировочную кривую, выражающую зависимость оптической плотности от концентрации. На оси ординат наносят значения оптической плотности, на оси абсцисс – концентрации. Обычно график строят по 5 – 6 точкам.
Определив плотность исследуемого раствора соли железа, по оси ординат находят точку, которая соответствует данному значению оптической плотности, проводят линию, параллельную оси абсцисс до пересечения ее с градуировочной кривой. Из точки пересечения опускают перпендикуляр на ось абсцисс. Находят Cx.
Определению иона Fe 3+ данным методом мешают некоторые восстановители (S 2- , SO3 2- , Sr 2+ ) и окислители, разрушающие роданид-ион (MnO4 — , NO3 — , H2O2), а также ионы, образующие комплексные соединения с железом (F — , Cl — , PO4 3- ).
Оборудование.
Посуда и материалы
Мерные колбы вместимостью 50 см 3 и 1000 см 3
Пипетки вместимостью 1, 5, 10, 25 см 3 .
1. Основной стандартный раствор железоаммиачных квасцов NH4Fe(SO4)2×12 H2O (додекагидрата сульфата аммония железа III) концентрации 0.1 мг Fe 3+ в 1 см 3 раствора.
2. Рабочий стандартный растворжелезоаммиачных квасцов готовят в день анализа разбавлением основного стандартного раствора в 10 раз (5 см 3 основного раствора отмерить пипеткой, поместить в мерную колбу объемом 50 см 3 и довести до метки дистиллированной водой). В 1 см 3 рабочего стандартного раствора сожержится 0.01 мг железа Fe 3+ .
3. Роданид аммония NH4SCN либо роданид калия KSCN концентрации 50 %.
4. Соляная кислота, плотность 1.12 г/см 3 .
Вопросы для защиты
Информация для лаборантов.
1. железоаммиачные квасцы NH4Fe(SO4)2×12 H2O (додекагидрат сульфата аммония железа III), концентрация 0.1 г Fe 3+ в 1 см 3 .
Навеску свежеперекристаллизованных железоаммиачных квасцов массой 0.8836 г растворяют в мерной колбе объемом 1000 см 3 , добавляют 2 см 3 концентрированной соляной кислоты и доводят до метки дистиллированной водой.
2. Роданид аммония NH4SCN либо роданид калия KSCN концентрации 50 %. Навеску соли массой 50 г растворяют в 50 см 3 дистиллированой воды.
3. Соляная кислота, плотность 1.12 г/см 3 . К 65 см 3 дистиллированной воды приливают 100 см 3 концентрированной соляной кислоты.
4. Аммоний надсернокислый.
5. Вода дистиллированная
1. 7 мерных колб объемом 50 см 3
2. пипетки на 1 (2) и 5 см 3 со шкалой
Оборудование
ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ
Лабораторная работа № 2.
ВОДОПОДГОТОВКА.
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ РАСТВОРЕННОГО ЖЕЛЕЗА В ВОДЕ.
Цель работы: определить содержание железа в сточной или природной воде фотоколориметрическим методом.
Общие сведения.
Железо (Ferrum) – принадлежит к 8 группе химических элементов периодической системы Д.И. Менделеева, атомная масса 55,847, атомный номер 26, плотность 7,874 г/см 3 , серебристо – белый блестящий пластичный металл, температура плавления 1535 o С. Железо достаточно распространено в земле (4 место) находится на 2 месте после алюминия; процентное содержание 4,65 %.
Главными источниками попадания соединений железа в поверхностные воды являются процессы химического выветривания горных пород, сопровождающиеся их механическим разрушением и растворением. В процессе взаимодействия с содержащимися в природных водах минеральными и органическими веществами образуется сложный комплекс соединений железа, находящихся в воде в растворенном, коллоидном и взвешенном состоянии. Значительные количества железа поступают с подземным стоком и со сточными водами предприятий металлургической, металлообрабатывающей, текстильной, лакокрасочной промышленности и с сельскохозяйственными стоками. В питьевой воде железо может содержаться также из-за плохого состояния водопроводов и применения коагулянтов на основе солей железа.
Содержание железа в поверхностных водах суши составляет десятые доли миллиграмма, вблизи болот – единицы миллиграммов. Наибольшие концентрации железа (до нескольких десятков и сотен миллиграммов в 1 дм 3 ) наблюдается в подземных водах с низкими значениями pH. Являясь биологически активным элементом, железо в определенной степени влияет на интенсивность развития фитопланктона и качественный состав микрофлоры в водоеме. Концентрация железа подвержена сезонным колебаниям. Обычно в водоемах с высокой биологической продуктивностью в период летней и зимней стагнации заметно увеличение концентрации ионов железа в придонных слоях воды. Предельно допустимая концентрация общего железа в воде водоемов 0.5 мг/л.
Содержание железа в воде выше 1-2 мг Fe 3+ в 1 дм 3 значительно ухудшает органолептические свойства, придавая ей неприятный вяжущий вкус, и делает воду малопригодной для использования в технических целях. По органолептическим показателям воды содержание железа в питьевой воде не должно превышать 0.3 мг/л (а по нормам ЕС даже 0.2 мг/л). Лишь в отдельных случаях при использовании подземных вод без установок по обезжелезиванию по согласованию с органами санитарно-эпидемиологической службы содержание железа в воде, поступающей в водопроводную сеть, допускается до 1 мг/л.
В поверхностных пресных водах железо содержится в очень не больших количествах, и, как правило, в трехвалентной форме. Повышенное содержание железа наблюдается в болотистых водах, до нескольких миллиграммов на литр, в таких водах повышенное содержание гумусовых веществ, которые соединены с трехвалентным железом. При высоких значениях pH железо в воде находится в коллоидной форме оксида железа Fe(OH)3. В подземных водах с низкими значениями pHи при минимальном содержании растворенного кислорода железо присутствует в растворенной двухвалентной форме. Трехвалентное железо при определенных условиях также может присутствовать в воде в растворенном виде как в форме неорганических солей (например, сульфатов), так и в составе растворимых органических комплексов.
При содержании в воде железа в концентрациях выше 0.3 мг/л вода после непродолжительного контакта с воздухом окисляется кислородом и становится желтовато – бурого цвета. Такая вода вызывает появление ржавых подтеков на сантехнике, отложения в котельном и бойлерном оборудовании. При концентрациях выше 1 мг/л вода мутная окрашивается в желто-бурый цвет при не длительном контакте с воздухом. Такая вода не допустима для использования, как в питьевых, так и в технических целях.
Железо человек получает в основном с пищей, из воды – максимально 10%. Также возможно попадание железа из воздуха, при этом вероятно возникновение профессиональных заболеваний. ВОЗ не дает рекомендуемой величины потребления железа по показаниям здоровья. В больших количествах железо, как и любое другое химическое вещество, способно вызвать в организме человека нарушения и даже патологии.
Виды железа, содержащегося в воде.
Как правило, в воде встречается несколько видов железа (таблица 1).
Двухвалентное железо (Fe +2 ) –в этой форме железо находится в растворенном состоянии. Иногда при определенных значениях pH гидроксид железа Fe(OH)2, выпадает в осадок.
Трехвалентное железо (Fe +3 ) —Хлорид (FeCl3) и сульфат (Fe2(SO4)3) – в растворимой форме, гидроксид железа Fe(OH)3 – в нерастворимом виде (существуют исключения при низком уровне pH).
Органическое железо – существует в различных комплексах, растворимых или в коллоидной форме. Органическое железо трудно удалить из воды. Органическое железо бывает следующих видов:
· Растворимое органическое железо. Способно связывать и удерживать кальций и другие металлы. Некоторые органические молекулы связывают железо в сложные растворимые комплексы – хелаты. Пример, таких органических соединений: порфириновая группа гемоглобина крови (удерживает железо), хлорофилл (удерживает магний), гуминовая кислота.
· Бактериальное железо. Существуют бактерии, использующие растворенное железо для жизни, они получают энергию, преобразуя двухвалентное железо в трехвалентное.
· Коллоидное железо. Коллоиды –частицы размером менее 1 микрона, которые не растворяются в воде, но трудно фильтруются из-за малого размера. К коллоидным частицам также относятся крупные органические молекулы (танины, лигнины). Коллоидные частицы обладают высоким поверхностным зарядом, поэтому они отталкивают друг друга и не укрупняются, образуя в воде суспензии, находящиеся во взвешенном состоянии, вода становится мутной.
Таблица 1 – Виды железа, содержащиеся в воде.
| Тип железа | Вода из-под крана | Вода после отстаивания |
| Двухвалентное | Чистая | Красно-бурый осадок |
| Трехвалентное | Окрашена | Красно-бурый осадок |
| Коллоидное | Желто-бурая | Не образует осадка, Не фильтруется |
| Растворенное органическое | Желто-бурая | |
| Бактериальное | Радужная пленка, желеобразные образования в водопроводной системе. |
Процесс удаления из воды железа называется обезжелезиванием. Очистка воды от железа – одна из самых сложных задач в водоподготовке. Одного универсального экономически оправданного метода очистки, который можно было бы применить во всех случаях для любой воды, не существует. Основные методы обезжелезивания:
· Окисление (реагентное, каталитическое). В результате окисления загрязнения осаждаются (с помощью коагулянтов или без них), потом фильтруются с помощью специальных систем очистки воды.
· Мембранные методы (осмос, обратный осмос, нанофильтрация)
Поскольку железо образует устойчивые окрашенные соединения, для его определения можно использовать фотоколориметрические методы.
Фотоколориметрия. Теоретические основы метода.
Закон Бугера – Ламберта — Бера
В основе оптических методов анализа лежит эффект избирательного поглощения света определенной длины волны веществом. Если вещество облучается видимым светом, этот раздел оптических методов анализа называется фотоколориметрией.
При прохождении потока излучения через частично поглощающую среду интенсивность прошедшего потока I согласно закону Бугера – Ламберта — Бера равна
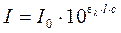
где I – интенсивность падающего потока;
ελ – молярный коэффициент поглощения при данной длине волны;
l – толщина поглощающего слоя (кюветы);
с – концентрация поглощающего вещества, моль/дм 3 .
Или в логарифмической форме:

Величину lg(I/I) в (2), характеризующую поглощающую способность вещества в растворе, называют оптической плотностью. В аналитической практике, стремясь подчеркнуть сущность процесса, лежащего в основе фотометрического определения, а именно поглощение квантов электромагнитного излучения оптического диапазона аналитической формой, эту величину называют поглощением, или светопоглощением и обозначают буквой А (absorption) либо D (density).
Закон Бугера – Ламберта — Бера: оптическая плотность раствора прямо пропорциональна концентрации вещества и толщине поглощающего слоя. Серию аналитических определений выполняют при постоянной толщине поглощающего слоя, тогда оптическая плотность линейно зависит от концентрации (рисунок 1).
Коэффициент линейной регрессии зависимости А = f(С) представляет собой молярный коэффициент поглощения ελ = tg a.
Рисунок 1. – зависимость оптической раствора плотности от концентрации.
Обратите внимание, что эта прямая линия проходит через начало координат. Для раствора поглощающего вещества при постоянных концентрациях и толщине поглощающего слоя оптическая плотность зависит от длины волны, поэтому измерения проводят при длине волны, соответствующей максимальному поглощению.
Приборами для фотоколориметрии служат фотоэлектроколориметры (ФЭК), характеризующиеся простотой оптической и электрической схем. Большинство фотометров имеет набор из 10-15 светофильтров и представляет собой прибор, в которых пучок света от источника излучения (лампа накаливания, редко ртутная лампа) проходит через светофильтр и проходит через кювету с исследуемым раствором или раствором сравнения (рисунок 2).
1 – источник света, 2 – щель, 3 – монохроматор (светофильтр),
4 – измерительная ячейка (анализируемый образец, образец сравнения),
5 – детектор, 6 – усилитель, 7 – регистрирующее устройство
(графическое, визуальное, цифровое)
Рисунок 2 – Блок-схема фотоэлектроколориметра (упрощенная)
Количественное определение вещества по светопоглощению основано на применении закона Бугера — Ламберта — Бера. Концентрацию можно определить, пользуясь методом градуировочного графика А = f(C), методом сравнения или методом добавок. Погрешности определения составляют около 5%.
Для перевода вещества в окрашенную форму используются химические реакции. Обязательное требование к реакциям, используемым в количественном анализе – они должны протекать избирательно, быстро и полностью воспроизводимо. Окраска образующейся аналитической формы должна быть устойчивой во времени и к действию света, а поглощение раствора, несущее информацию о концентрации поглощающего вещества, должно подчиняться физическим законам, связывающим поглощение и концентрацию, конкретно – закону Бугера – Ламберта – Бера.
Практическая часть.
Ион Fe 3+ с роданид-ионом в зависимости концентрации ионов железа и роданид-ионов дает ряд окрашенных в кроваво-красный цвет комплексов:
Число роданид-анионов n в комплексе железа может изменяться от 1 до 6. В данной работе берется избыток роданид-ионов, при этом образуются комплекс FeSCN6 3- .
Для построения градуировочной кривой используются стандартные растворы, отличающиеся друг от друга по концентрации не менее чем на 10 %.
Растворы готовят непосредственно перед колориметрированием, так как окраска растворов неустойчива.
По серии стандартных растворов соли железа строят градуировочную кривую, выражающую зависимость оптической плотности от концентрации. На оси ординат наносят значения оптической плотности, на оси абсцисс – концентрации. Обычно график строят по 5 – 6 точкам.
Определив плотность исследуемого раствора соли железа, по оси ординат находят точку, которая соответствует данному значению оптической плотности, проводят линию, параллельную оси абсцисс до пересечения ее с градуировочной кривой. Из точки пересечения опускают перпендикуляр на ось абсцисс. Находят Cx.
Определению иона Fe 3+ данным методом мешают некоторые восстановители (S 2- , SO3 2- , Sr 2+ ) и окислители, разрушающие роданид-ион (MnO4 — , NO3 — , H2O2), а также ионы, образующие комплексные соединения с железом (F — , Cl — , PO4 3- ).
Оборудование.
Посуда и материалы
Мерные колбы вместимостью 50 см 3 и 1000 см 3
Пипетки вместимостью 1, 5, 10, 25 см 3 .
1. Основной стандартный раствор железоаммиачных квасцов NH4Fe(SO4)2×12 H2O (додекагидрата сульфата аммония железа III) концентрации 0.1 мг Fe 3+ в 1 см 3 раствора.
2. Рабочий стандартный растворжелезоаммиачных квасцов готовят в день анализа разбавлением основного стандартного раствора в 10 раз (5 см 3 основного раствора отмерить пипеткой, поместить в мерную колбу объемом 50 см 3 и довести до метки дистиллированной водой). В 1 см 3 рабочего стандартного раствора сожержится 0.01 мг железа Fe 3+ .
3. Роданид аммония NH4SCN либо роданид калия KSCN концентрации 50 %.
4. Соляная кислота, плотность 1.12 г/см 3 .
Последнее изменение этой страницы: 2016-09-20; Нарушение авторского права страницы
источник
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
Методы измерения массовой концентрации
Methods for determination
Настоящий стандарт распространяется на питьевую воду и устанавливает колориметрические методы измерения массовой концентрации общего железа.
1.1. Пробы воды отбирают по ГОСТ 2874 и ГОСТ 24481.
1.2. Объем пробы воды для измерения массовой концентрации железа должен быть не менее 200 см 3 .
1.3. Способы консервирования, сроки и условия хранения проб воды, предназначенных для измерения массовой концентрации общего железа, — по ГОСТ 24481.
(Измененная редакция, Изм. № 2).
Метод основан на взаимодействии ионов железа в щелочной среде с сульфосалициловой кислотой с образованием окрашенного в желтый цвет комплексного соединения. Интенсивность окраски, пропорциональную массовой концентрации железа, измеряют при длине волны 400-430 нм. Диапазон измерения массовой концентрации общего железа без разбавления пробы 0,10-2,00 мг/дм 3 . В этом интервале суммарная погрешность измерения с вероятностью Р=0,95 находится в пределах 0,01-0,03 мг/дм 3 .
Фотоколориметр любого типа с фиолетовым светофильтром ( 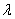
Кюветы с толщиной рабочего слоя 2-5 см.
Весы аналитические лабораторные, класс точности 1, 2 по ГОСТ 24104.
Колбы мерные 2-го класса, вместимостью 50, 100, 1000 см 3 по ГОСТ 1770.
Пипетки мерные без делений вместимостью 50 см 3 и пипетки мерные с ценой наименьшего деления 0,1-0,05 см 3 , вместимостью 1, 5 и 10 см 3 2-го класса по нормативно-техническому документу.
Колбы стеклянные лабораторные конические номинальной вместимостью 100 см 3 , типа Кн по ГОСТ 25336.
Аммоний хлористый по ГОСТ 3773.
Аммиак водный по ГОСТ 3760, 25 %-ный раствор.
Квасцы железоаммонийные по нормативно-техническому документу.
Кислота соляная по ГОСТ 3118.
Кислота сульфосалициловая по ГОСТ 4478.
Вода дистиллированная по ГОСТ 6709.
Все реактивы, используемые для анализа, должны быть квалификации химически чистые (х. ч.) или чистые для анализа (ч.д.а).
2.3.1. Приготовление основного стандартного раствора железо-аммонийных квасцов
0,8636 г железоаммонийных квасцов FeNH 4 ( SO 4 )2 × 12 H 2 O взвешивают с точностью, не превышающей 0,0002 г по шкале весов, растворяют в мерной колбе вместимостью 1 дм 3 в небольшом количестве дистиллированной воды, добавляют 2,00 см 3 соляной кислоты плотностью 1,19 г/см 3 и доводят до метки дистиллированной водой. 1 см 3 раствора содержит 0.1 мг железа.
Срок и условия хранения раствора — по ГОСТ 4212.
2.3.2. Приготовление рабочего стандартного раствора железоаммонийных квасцов
Рабочий раствор готовят в день проведения анализа разбавлением основного раствора в 20 раз. 1 см 3 раствора содержит 0,005 мг железа.
2.3.3. Приготовление раствора сульфосалициловой кислоты
20 г сульфосалициловой кислоты растворяют в мерной колбе вместимостью 100 см 3 в небольшом количестве дистиллированной воды и доводят этой водой до метки.
2.3.4. Приготовление раствора хлористого аммония молярной концентрации 2 моль/дм 3
107 г NH 4 Cl растворяют в мерной колбе вместимостью 1 дм 3 в небольшом количестве дистиллированной воды и доводят этой водой до метки.
2.3.5. Приготовление раствора аммиака (1:1)
100 см 3 25 %-ного раствора аммиака приливают к 100 см 3 дистиллированной воды и перемешивают.
При массовой концентрации общего железа не более 2,00 мг/дм 3 отбирают 50 см 3 исследуемой воды (при большей массовой концентрации железа пробу разбавляют дистиллированной водой) и помещают в коническую колбу вместимостью 100 см 3 . Если проба при отборе не консервировалась кислотой, то к 50 см 3 добавляют 0,20 см 3 соляной кислоты плотностью 1,19 г/см 3 . Пробу воды нагревают до кипения и упаривают до объема 35-40 см 3 . Раствор охлаждают до комнатной температуры, переносят в мерную колбу вместимостью 50 см 3 , ополаскивают 2-3 раза по 1 см 3 дистиллированной водой, сливая эти порции в ту же мерную колбу. Затем к полученному раствору прибавляют 1,00 см 3 хлористого аммония, 1,00 см 3 сульфосалициловой кислоты, 1,00 см 3 раствора аммиака (1:1), тщательно перемешивая после добавления каждого реактива. По индикаторной бумаге определяют значение рН раствора, которое должно быть 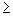
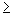
Объем раствора в мерной колбе доводят до метки дистиллированной водой, оставляют стоять 5 мин для развития окраски. Измеряют оптическую плотность окрашенных растворов, используя фиолетовый светофильтр ( 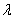
Для построения градуировочного графика в ряд мерных колб вместимостью 50 см 3 наливают 0,0; 1,0; 2,0; 5,0. 10,0; 15,0; 20,0 см 3 рабочего стандартного раствора, доводят до метки дистиллированной водой, перемешивают и анализируют, как исследуемую воду. Получают шкалу растворов, соответствующих массовым концентрациям железа 0,0; 0,1; 0,2; 0,5; 1,0; 1,5; 2,0 мг/дм 3 .
Строят градуировочный график, откладывая по оси абсцисс массовую концентрацию железа, а по оси ординат — соответствующие значения оптической плотности. Построение градуировочного графика повторяют для каждой партии реактивов и не реже одного раза в квартал.
Массовую концентрацию железа (X) в анализируемой пробе, мг/дм 3 с учетом разбавления вычисляют по формуле
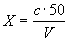
где с — концентрация железа, найденная по градуировочному графику, мг/дм 3 ;
V — объем воды, взятый для анализа, см 3 ;
50 — объем, до которого разбавлена проба, см 3 .
За окончательный результат анализа принимают среднее арифметическое результатов двух параллельных измерений, допустимое расхождение между которыми не должно превышать 25 % при массовой концентрации железа на уровне предельно допустимой. Результат округляют до двух значащих цифр.
Сходимость результатов анализа ( А) в процентах вычисляют по формуле
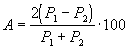
где Р1 — больший результат из двух параллельных измерений;
Р 2 — меньший результат из двух параллельных измерений.
Разд. 2. (Измененная редакция, Изм. № 2).
Метод основан на реакции ортофенантролина с ионами двухвалентного железа в области рН 3-9 с образованием комплексного соединения, окрашенного в оранжево-красный цвет. Интенсивность окраски пропорциональна концентрации железа. Восстановление железа до двухвалентного проводится в кислой среде гидроксиламином. Окраска развивается быстро при рН 3,0-3,5 в присутствии избытка фенантролина и устойчива в течение нескольких дней. Диапазон измерения массовой концентрации общего железа без разбавления пробы 0,05-2,0 мг/дм 3 . В этом интервале суммарная погрешность измерения с вероятностью Р = 0,95 находится в пределах 0,01-0,02 мг/дм 3 .
(Измененная редакция, Изм. № 2).
3.2. Аппаратура, материалы и реактивы
Фотоэлектроколориметр различных марок.
Кюветы с толщиной рабочего слоя 2-5 см.
Колбы мерные 2-го класса точности по ГОСТ 1770, вместимостью 50 и 1000 см 3 .
Пипетки мерные без делений, вместимостью 10, 25 и 50 см 3 и пипетки мерные с делениями 0,1-0,01 см 3 вместимостью 1, 2 и 5 см 3 2-го класса точности по нормативно-техническому документу.
Колбы плоскодонные по ГОСТ 25336, вместимостью 150-200 см 3 .
Аммоний уксуснокислый по ГОСТ 3117.
Гидроксиламин солянокислый по ГОСТ 5456.
Квасцы железоаммонийные по нормативно-техническому документу.
Кислота соляная по ГОСТ 3118.
Кислота уксусная по ГОСТ 61.
Вода дистиллированная по ГОСТ 6709.
Аммиак водный по ГОСТ 3760, 25 %-ный раствор.
Все реактивы, используемые для анализа, должны быть квалификации чистые для анализа (ч. д. а.).
3.3.1. Приготовление раствора ортофенантролина
0,1 г моногидрата ортофенантролина ( C 12 Н8 N 2 × H 2 O ), взвешенного с погрешностью не более 0,01 г, растворяют в 100 см 3 дистиллированной воды, подкисленной 2-3 каплями концентрированной соляной кислоты. Реактив сохраняют на холоде в темной склянке с притертой пробкой. 1 см 3 этого реактива связывает в комплекс 0,1 мг железа.
3.3.2. Приготовление 10%-ного раствора солянокислого гидроксиламина
10 г солянокислого гидроксиламина ( NH 2 OH × HCl ), взвешенного с погрешностью не более 0,1 г, растворяют в дистиллированной воде и доводят объем до 100 см 3 .
3.3.3. Приготовление буферного раствора
250 г уксуснокислого аммония ( N Н4С2Н3 O 2 ), взвешенного с погрешностью не более 0,1 г, растворяют в 150 см 3 дистиллированной воды. Добавляют 70 см 3 уксусной кислоты и доводят объем до 1 дм 3 дистиллированной водой.
(Измененная редакция, Изм. № 2).
3.3.4. Приготовление основного стандартного раствора железоаммонийных квасцов — по п. 2.3.1.
3.3.5. Приготовление рабочего стандартного раствора железоаммонийных квасцов — по п. 2.3.2.
3.3.4; 3.3.5. (Измененная редакция, Изм. № 2).
Определению мешают цианиды, нитриты, полифосфаты; хром и цинк в концентрации, превышающей в 10 раз массовую концентрацию железа; кобальт и медь в концентрации более 5 мг/дм 3 и никель в концентрации 2 мг/дм 3 . Предварительное кипячение воды с кислотой превращает полифосфаты в ортофосфаты, добавлением гидроксиламина устраняется мешающее влияние окислителей. Мешающее влияние меди уменьшается при рН 2,5-4.
При отсутствии полифосфатов исследуемую воду тщательно перемешивают и отбирают 25 см 3 (или меньший объем, содержащий не более 0,1 мг железа, разбавленный, до 25 см 3 дистиллированной водой) в мерную колбу вместимостью 50 см 3 . Если при отборе пробы вода была подкислена, то ее нейтрализуют 25 %-ным раствором аммиака до рН 4-5, контролируя потенциометрически или по индикаторной бумаге. Затем добавляют 1 см 3 солянокислого раствора гидроксиламина, 2,00 см 3 ацетатного буферного раствора и 1 см 3 раствора ортофенантролина. После прибавления каждого реактива раствор перемешивают, затем доводят объем до 50 см 3 дистиллированной водой, тщательно перемешивают и оставляют на 15-20 мин для полного развития окраски.
Окрашенный раствор фотометрируют при сине-зеленом светофильтре ( 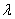
Массовую концентрацию железа находят по градуировочному графику.
В присутствии полифосфатов 25 см 3 исследуемой пробы помещают в плоскодонную колбу вместимостью 100-150 см 3 , прибавляют 1 см 3 концентрированной соляной кислоты, нагревают до кипения и упаривают до объема 15-20 см 3 . После охлаждения раствора его переносят в мерную колбу вместимостью 50 см 3 , добавляют дистиллированную воду до объема примерно 25 см 3 и доводят 25 %-ным раствором аммиака до рН 4-5, контролируя потенциометрически или по индикаторной бумаге.
Далее прибавляют реактивы и проводят анализ, как указано выше (при отсутствии полифосфатов).
Для построения градуировочного графика в мерные колбы вместимостью 50 см 3 вносят 0,0; 0,5; 1,0; 2,0; 3.0; 4,0; 5,0; 10,0; 20,0 см 3 рабочего стандартного раствора, содержащего в 1 см 3 0,005 мг железа, доводят объем дистиллированной водой приблизительно до 25 см 3 и анализируют так же, как и исследуемую воду. Получают шкалу стандартных растворов с массовой концентрацией железа 0,0; 0,05; 0,1; 0,2; 0,3; 0,4; 0,5; 1,0 и 2,0 мг/дм 3 . Фотометрируют в тех же условиях, что и пробу. Строят градуировочный график, откладывая по оси абсцисс массовую концентрацию общего железа в мг/дм 3 а на оси ординат — соответствующие значения оптической плотности.
(Измененная редакция, Изм. № 2).
3.5. Массовую концентрацию общего железа вычисляют по п. 2.5.
(Измененная редакция, Изм. № 2).
Метод основан на взаимодействии ионов двухвалентного железа с 2,2-дипиридилом в области рН 3,5-8,5 с образованием окрашенного в красный цвет комплексного соединения. Интенсивность окраски пропорциональна массовой концентрации железа. Восстановление трехвалентного железа до двухвалентного проводится гидроксиламином. Окраска развивается быстро и устойчива в течение нескольких дней. Диапазон измерения массовой концентрации общего железа без разбавления пробы 0,05-2,00 мг/дм 3 .
В этом интервале суммарная погрешность измерения с вероятностью Р=0,95 находится в пределах 0,01-0,03 мг/дм 3 .
(Измененная редакция, Изм. № 2).
4.2. Аппаратура, материалы, реактивы
Фотоэлектроколориметр любой марки.
Кюветы с толщиной оптического слоя 2-5 см.
Колбы мерные 2-го класса точности по ГОСТ 1770, вместимостью 50, 100 и 1000 см 3 .
Пипетки мерные без делений, вместимостью 25 см 3 н пипетки мерные с делениями 0,1-0,01 см 3 , вместимостью 1, 5 и 10 см 3 2-го класса точности по нормативно-техническому документу.
Аммоний уксуснокислый по ГОСТ 3117.
Гидроксиламин солянокислый по ГОСТ 5456.
2,2-дипиридил ( 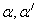
Квасцы железоаммонийные по нормативно-техническому документу.
Кислота уксусная по ГОСТ 61.
Спирт этиловый ректификованный по ГОСТ 18300, высшего сорта.
Вода дистиллированная по ГОСТ 6709.
Все реактивы, используемые для анализа, должны быть квалификации химически чистые (х. ч.) или чистые для анализа (ч. д. а.).
(Измененная редакция, Изм. № 2).
4.3.1. Приготовление основного стандартного раствора железоаммонийных квасцов — по п. 2.3.1.
4.3.2. Приготовление рабочего стандартного раствора железоаммонийных квасцов — по п. 2.3.2.
4.3.1; 4.3.2. (Измененная редакция, Изм. № 2).
4.3.3. Приготовление 10 %-ного раствора солянокислого гидроксиламина — по п. 3.3.2.
4.3.4. Приготовление ацетатного буферного раствора — по п. 3.3.3.
4.3.5. Приготовление 0,1 %-ного раствора 2,2-дипиридила.
0,1 г 2,2-дипиридила, взвешенного с погрешностью не более 0,01 г, растворяют в 5,00 см 3 этилового спирта и разбавляют в 100 см 3 дистиллированной воды.
Для определения массовой концентрации общего железа исследуемую воду тщательно перемешивают и отбирают 25 см 3 (или меньший объем, содержащий не более 0,1 мг железа) в мерную колбу вместимостью 50 см 3 . Прибавляют 1 см 3 раствора гидроксиламина солянокислого, 2,00 см 3 ацетатного буферного раствора, 1,00 см 3 раствора 2,2-дипириднла и доводят до метки дистиллированной водой. После добавления каждого реактива содержимое колбы перемешивают. Раствор оставляют на 15-20 мин для полного развития окраски. Окрашенный раствор фотометрируют, применяя зеленый светофильтр ( 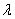
Массовую концентрацию железа находят по градуировочному графику.
Для построения градуировочного графика в мерные колбы вместимостью 50 см 3 вносят 0,0; 2,0; 5,0; 10,0; 15,0; 20,0 см 3 рабочего стандартного раствора железоаммонийных квасцов. Добавляют дистиллированной воды до объема примерно 25 см 3 . Далее растворы проводят через весь ход анализа так же, как исследуемую воду. Получают шкалу стандартных растворов с массовой концентрацией железа 0,0; 0,2; 0,5; 1,0; 1,5; 2,0 мг/дм 3 . Оптическую плотность измеряют в тех же условиях, что и пробы. Строят градуировочный график, откладывая по оси абсцисс массовую концентрацию железа в мг/дм 3 , а по оси ординат — соответствующие значения оптической плотности.
Массовую концентрацию общего железа вычисляют по п. 2.5.
4.3.5; 4.4; 4.5. (Измененная редакция, Изм. № 2).
1. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 09.10.72 № 1855
3. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
источник






