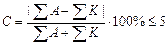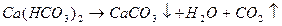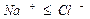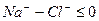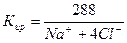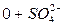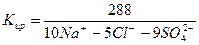Химический анализ подземных вод может служить качественным показателем использования воды для хозяйственно-питьевого водоснабжения, бальнеологических, промышленных и хозяйственных целей, а также диагностическим признаком при гидрохимических методах поисков и разведки месторождений полезных ископаемых.
Результаты химического анализа подземных вод могут быть выражены в табличной или сокращенной отчетной форме в виде формулы Курлова.
1). Табличная форма выражения химического анализа.
Количественно концентрация катионов и анионов выражается в г/дм 3 , мг/дм 3 , а эквивалентное содержание – миллимолях (ммоль) и процентах (%).
Пример расчета химического анализа воды в табличной форме приводится ниже.
| Ионы | Содержание, мг/дм 3 | Эквивалентное содержание | |
| ммоль | % | ||
| Na + Ca 2+ Mg 2+ | 88,04 22,75 15,62 | 69,9 17,6 12,5 | |
| Сумма катионов | — | 126,41 | |
| Cl — SO4 2 — HCO3 — | 98,40 17,43 3,51 | 82,5 14,5 3,0 | |
| Сумма анионов | — | 119,34 | |
| М (сухой остаток) | — | — | |
| СО2(свободный) | — | — | |
| рН водородный показатель | 5,3 | — | — |
| Т воды, градус С | — | — |
Эквивалентное (молярное) содержание определяется путем умножения каждого иона на пересчетный коэффициент, учитывающий его атомный вес и валентность и представляющий собой величины, обратные эквивалентным массам ионов (таблица 2).
| Катионы | Коэффициент | Анионы | Коэффициент |
| Na + Ca 2+ Mg 2+ | 0,0435 0,0499 0,08222 | Cl — SO4 2- HCO3 — | 0,0282 0,0208 0,0164 |
Для пересчета в %-эквивалентную форму суммы катионов и анионов в миллимолях принимаются за 100%, а затем определяется доля каждого катиона и аниона в % от соответствующей суммы катионов и анионов.
Химический анализ считается достоверным, если ошибка анализа не превышает 5%.
В нашем случае С = 2,88%. Анализ достоверен.
2) Сокращенная форма выражения химического анализа (формула М.Г. Курлова)
Формула Курлова представляет собой псевдодробь, в числителе которой в порядке убывания в %-эквивалентной форме располагаются анионы, а в знаменателе – катионы. Ионы, содержание которых менее 1%, в формулу не включаются. Проценты округляют до целых чисел.
Слева от дроби указывается содержание газов в мг/дм 3 и минерализация (М) в г/дм 3 , за которую принимается сухой остаток. Справа записывают значение (рН), температуру воды (Т) в градусах Цельсия, дебит источника в м 3 /сут и содержание микроэлементов, если такие имеются.
В нашем случае формула Курлова (таблица 1):
3) Наименование воды по химическому составу.
Наименование химического типа подземных вод должно состоять из двух частей, отражающих преобладающий анионный и катионный состав воды. Наименование химического типа воды начинается с ее анионного, а затем катионного состава в %-эквивалентной форме, превышающего 20% от суммы миллимолярной концентрации. Перечисление ионов производится в порядке возрастания концентрации – от меньшего значения к большему.
В сокращенном анализе анионы представлены хлоридами, сульфатами и гидрокарбонатами, а катионы – натрием, кальцием и магнием. В нашем случае вода хлоридно-натриевая.
4) Классификация воды по минерализации.
В зависимости от величины минерализации, за которую принимается сухой остаток, подземные воды классифицируются в соответствии с приведенной таблицей 3.
| Минерализация М, г/дм 3 | Подгруппа | Группа |
| £ 0,5 >0,5-1,0 | Весьма пресные Пресные | Пресные |
| >1,0-1,5 >1,5-3,0 >3,0-5,0 >5,0-10,0 >10,0-25,0 | Весьма слабосолоноватые Слабо солоноватые Умеренно солоноватые Солоноватые Сильно солоноватые | Солоноватые |
| >25,0-36,0 >36,0-50,0 | Слабосоленые Сильносоленые | Соленые |
| >50,0-150,0 >150,0-350,0 >350,0 | Рассолы слабые Рассолы крепкие Рассолы весьма крепкие (рапа) | Рассолы |
В нашем случае М = 6,9 г/дм 3 . Вода солоноватая.
Реакция воды обусловлена величиной концентрации водородных ионов рН, которая представляет собой обратный логарифм концентрации ионов водорода. Классификация воды по водородному показателю приведена в таблице 4.
| Водородный показатель рН при Т22 о С | Подгруппа | Группа |
| £ 3,5 >3,5-4,5 >4,5-5,5 >5,5-6,0 | Весьма кислая Кислая Умеренно кислая Слабокислая | Кислая |
| >6,0-8,0 | Нейтральная | Нейтральная |
| >8,0-8,5 >8,5-9,0 >9,0-9,5 >9,5 | Слабощелочная Умеренно щелочная Щелочная Весьма щелочная | Щелочная |
В нашем случае рН = 5,3. Вода умеренно кислая.
6) Классификация подземных вод по температуре воды.
Классификация воды по температуре приведена в таблице 5.
| Температура, Т о С | Наименование |
| 0-4 >4-20 >20-37 >37-50 >50-75 >75-100 >100-200 >200-374 | Переохлажденная Очень холодная Холодная Теплая Очень теплая Горячая Очень горячая Слабо перегретая Весьма перегретая |
Примечание: воды с температурой от 20 до 100 о С называются термальными.
В нашем случае Т15 о С. Вода холодная.
Жесткость воды имеет большое значение при использовании подземных вод для питьевого водоснабжения, промышленных и хозяйственных целей. Жесткость воды обусловливается содержанием в ней солей кальция и магния. Измеряется в миллимолях (мг-экв/дм 3 ).
Различают общую жесткость (ОЖ), устранимую или временную жесткость (УЖ) и постоянную жесткость (ПЖ).
Общая жесткость обусловлена присутствием в воде гидрокарбонатов, хлоридов и сульфатов кальция и магния и равняется сумме устранимой и постоянной жесткости.
Устранимая жесткость обусловлена присутствием в воде гидрокарбонатов кальция и магния. Такая жесткость получила название карбонатной (КЖ) и может быть устранена при кипячении
Карбонат кальция и магния выпадает в осадок, образуя накипь. При использовании такой воды для промышленных и коммунальных целей происходит отложение карбоната кальция и магния на стенках котлов и трубопроводов, что приводит к выводу их из эксплуатации.
При высоком содержании НСО3 — в воде, превышающем суммарную концентрацию кальция и магния, вся жесткость считается карбонатной.
Постоянная жесткость обусловлена наличием в воде сульфатов и хлоридов кальция и магния и равняется разности между общей и карбонатной жесткостью.
Классификация воды по общей жесткости приводится в таблице 6 (ГОСТ 6055-86).
| Содержание в ммоль | Группа жесткости |
| £ 1,5 >1,5-3,0 >3,0-6,0 >6,0-9,0 >9,0 | Очень мягкая Мягкая Умеренно жесткая Жесткая Очень жесткая |
Подземные воды, жесткость которых превышает 7 ммоль, не могут быть использованы для питьевого и промышленного водоснабжения.
В нашем случае общая жесткость составляет 38,37 ммоль, устранимая (карбонатная) – 3,50 ммоль, постоянная – 34,86 ммоль. Вода очень жесткая, непригодная для питьевого и промышленного водоснабжения.
8) Пригодность для питьевого водоснабжения.
Пригодность воды для питьевого водоснабжения нормируется ГОСТ 6055-86 «Вода питьевая». В рамках сокращенного гидрохимического анализа нормативными являются минерализация, общая жесткость, содержание Cl — и SO 2- 4 , а также величина рН с предельно допустимыми концентрациями, приведенными в таблице 7.
| Наименование показателей | ПДК | Содержание в нашем примере | Степень пригодности |
Минерализация М, мг/дм 3 Общая жесткость ОЖ, ммоль 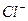 , мг/дм 3 , мг/дм 3 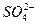 , мг/дм 3 рН , мг/дм 3 рН | 6,5-8,5 | 38,37 5,3 | Не пригодна Не пригодна Не пригодна Не пригодна Не пригодна |
В нашем случае вода по всем компонентам не пригодна для водоснабжения.
9) Пригодность для ирригационных целей.
Пригодность использования подземных вод, в том числе и шахтных, для ирригационных целей в сельском хозяйстве нормируется степенью минерализации воды и расчетным ирригационным коэффициентом. Классификация воды по минерализации, нормирующая степень пригодности для орошения сельскохозяйственных угодий, приведена в таблице 8.
| Минерализация, г/дм 3 | Степень пригодности для орошения |
| £1,7 >1,7-5,0 >5,0 | Пригодна Пригодна условно (возможно засоление) Не пригодна |
В нашем случае минерализация 6,9 г/дм 3 . Вода для орошения не пригодна.
Расчет ирригационного коэффициента выполняется в зависимости от соотношения ионов натрия, хлора и сульфатов в эквивалентной форме в миллимолях.


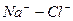
 |
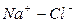

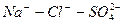
Во втором случае избыточное содержание катионов натрия может быть нейтрализовано содержащимся в воде сульфат-ионом. В третьем случае избыток натрия накапливается в почве в виде поглощенных катионов.
В первых двух случаях вода улучшению не подлежит, в третьем случае воду можно улучшить добавкой гипса. Классификация воды по ирригационному коэффициенту приведена в таблице 9.
| Ирригационный коэффициент | Характеристика воды | ||||||||||||||||||||||||||||||||||||||||||||||||||
| >18 >6-18 ³1,2-6,0 + — , Кир= 0,58. Вода очень плохая и улучшению не подлежит. 10) Агрессивность подземных вод. Подземные воды в зависимости от состава могут оказывать разрушающее действие на бетоны, цементы и металлы. Оценка агрессивности подземных вод по отношению к бетонам марки W4 и металлам производится на основании таблиц 5-7 и 26 СНиП 2.03.11-85 «Защита строительных конструкций от коррозии» (в скобках указаны номера таблиц согласно СНиП). Дата добавления: 2015-04-18 ; просмотров: 71 ; Нарушение авторских прав источник Данная работа рассчитана на 2 часа академических занятий и на 4 часа самостоятельной работы студентов с преподавателем. Целью данной работы является ознакомление студентов с данными сокращенного химического анализа подземных вод, методикой их обработки и пересчета путем использования нормативов ГОСТа, систематизация и оценка пригодности их для питьевого водоснабжения или технического использования. 2.2.1 Свойства и характеристика подземных вод. Вопросы практического использования подземных и рудничных вод могут быть решены только после полного изучения их физико-химических свойств, химического и бактериального состава. Химический состав и физические свойства подземных вод изучают для различных целей: питьевого и технически-хозяйственного водоснабжения (питания паровых котлов, охлаждения машин, тушения пожаров и т.п.), орошения полей, лечебных целей, как поисковый критерий на различные полезные ископаемые, для оценки агрессивности подземных вод по отношению к бетону, коррозирующих свойств по отношению к металлам, для установления связи водоносных горизонтов между собой и с поверхностными водами и т.п. Подземные воды представляют собой сложные естественные растворы, находящиеся в многообразных связях и взаимодействии с окружающей природной средой. Естественная физико-географическая и геологическая обстановка определяют особенности генезиса и дальнейшего преобразования подземных вод. К физическим свойствам подземных вод относятся температура, цвет, запах, прозрачность, вкус, привкус, электропроводность и радиоактивность. Определение этих свойств частично проводится непосредственно в полевых условиях при отборе проб воды, а в основном – в химических лабораториях по специальной методике. Химические свойства подземных вод определяются количеством и соотношением содержащихся в них в растворенном виде солей, присутствующих в воде в виде ионов – анионов и катионов, а также некоторых недиссоциированных соединений, газов и органических соединений. Среди ионов наибольшее практическое значение имеют следующие: катионы – водород – H + , натрий – Na + , калий – K + , магний – Mg 2+ , кальций – Ca 2+ , железо – Fe 2+ ; анионы – хлор – Cl — , сульфат – SO4 2- , гидрокарбонат – HCO3 — . Из недиссоциированных соединений наиболее часто встречаются окислы железа – Fe2O3, кремния – Si2O3, алюминия – Al2O3, а из газов – углекислый газ – CO2, кислород – O2, азот – N2, метан – CH4, сероводород – H2S. В результате выполнения данной работы студенты, изучив химический состав подземных вод, должны иметь определенные навыки по их обработке и систематизации, а также определить область практического использования. Перечень необходимых определений веществ, содержащихся в подземных водах, устанавливается в соответствии с целевым назначением анализа, что и указывается в программе работ гидрогеологических исследований. 2.2.2 Способы выражения химического состава подземных вод. В природной воде молекулы солей почти полностью диссоциированы на ионы, поэтому основной формой выражения результатов химического анализа воды является ионная форма. При этом содержание любого иона в процессе исследования выражается в граммах или миллиграммах на кубический дециметр (что равнозначно литру) воды (г/дм 3 (г/л), мг/дм 3 (мг/л)). Поэтому результаты анализов в химических лабораториях даются в ионной форме, т.е. в г/дм 3 (г/л), мг/дм 3 (мг/л). Но, делать некоторые выводы о составе и свойствах воды можно, лишь имея анализы в миллиграмм — эквивалентной и эквивалент — процентной формах. Поэтому данные химического анализа должны быть пересчитаны (табл. 3). Для этого вначале необходимо определить эквивалент каждого аниона и катиона. Дело в том, что ионы взаимодействуют между собой в строго определенных эквивалентных весовых соотношениях. Например, один эквивалент одного иона хлора Cl — может взаимодействовать только с одним эквивалентом иона натрия Na + или кальция Ca 2+ . Следовательно, эквивалент – это число, показывающее, в каком весовом соотношении данный ион вступает в соединение с другим ионом. Для пересчета анализа из ионной формы в миллиграмм – эквивалентную следует число миллиграммов каждого иона разделить на его эквивалентный вес, который представляет собой отношение атомного (или ионного) веса данного элемента к его валентности. Например, кальция Ca 2+ в воде содержится 420 мг/дм 3 . Эквивалентный вес одного иона кальция Ca 2+ равен: 40,08 : 2 = 20,04 мг/экв. Чтобы определить его миллиграмм – эквивалентное содержание надо 420 : 20,04 = 20,96 мг/экв. Также для пересчета анализов воды в миллиграмм-эквиваленты содержание ионов умножают на специальные пересчетные коэффициенты, которые представляют частное от деления единицы на эквивалентный вес. Для выше приведенного примера пересчетный коэффициент кальция Ca 2+ равен 1 : 20,04 = 0,0499. Если 420 • 0,0499 = 20,96 мг/экв – миллиграмм-эквивалентная форма. Ниже приведены пересчетные коэффициенты для некоторых ионов: гидрокарбонат HCO3 — – 0,0164 Если сумму всех катионов и анионов в миллиграмм-эквивалентной форме принять за 100%, можно получить соответствующие выражения для анионов и катионов в эквивалент-процентной форме. Количества катионов и анионов, выраженные в эквивалент-процентной форме, должны быть равны между собой, т.е. сумма всех катионов должна составлять 50% и сумма всех анионов тоже 50%, что является удобным контролем анализа. В последнее время очень часто принимают за 100% сумму миллиграмм-эквивалентов анионов и также за 100% — сумму миллиграмм-эквивалентов катионов. Расчет от этого не изменяется, но величины эквивалент-процентов становятся в два раза больше. Если результаты анализа воды выражены в миллиграмм-эквивалентной форме, то перед символом иона ставят букву r, например rCl — и т.д. При анализе могут быть неточности. Допустимая неточность анализа определяется из выражения: Таблица 3 — Исходные данные
В итоге пересчетов должна быть составлена таблица следующей формы (табл. 4): Таблица 4 — Порядок пересчета ионной формы в другие формы
При химическом анализе воды определяют величину сухого остатка после выпаривания и количества веществ, содержащихся в воде (минерализацию). Количества веществ показывают в ионной форме, при которой содержание отдельных ионов определяют в миллиграммах на 1 л воды. При выборе и оценке воды источника централизованного хозяйственно-питьевого водоснабжения пользуются государственными стандартами (ГОСТ – 2874 – 82 и др.). Сумма растворенных в воде веществ – сухой остаток – при t = 105 – 110 0 C не должна превышать 1000 мг/л. 2.2.3 Минерализация. Это экспериментально определенный сухой остаток или подсчитанная сумма минеральных веществ. Единой классификации по степени минерализации нет, их достаточно много применительно к требованиям отдельных ведомств. В таблице 5 приводится выражение общей минерализации подземных вод по В.М. Вернадскому, согласующееся с требованиями их практического использования. Таблица 5 — Классификация подземных вод по общей минерализации
2.2.4 Жесткость воды. Особое ее качество, обусловленное присутствием углекислых и сернокислых солей Ca 2+ и Mg 2+ . Жесткость поземных вод имеет большое значение при их оценке для практического использования. Жесткая вода плохо взмыливается, дает накипь в паровых котлах (что уменьшает их теплопроводность, приводит к перерасходу топлива и может вызвать аварию) и в посуде, вспенивается, в жесткой воде медленнее развариваются овощи, мясо, крупы и другие продукты. Различают общую, временную (карбонатную или устранимую) и постоянную жесткость воды. Общей называют жесткость, соответствующую пробе свежей воды. При кипячении воды растворенные в ней бикарбонаты (двууглекислые соли) переходят в углекислые и выпадают в виде осадка или накипи. Жесткость, соответствующая кипяченной воде, называется постоянной. Разность между общей и постоянной жесткостью воды называют временной жесткостью. Жесткость выражают в градусах жесткости. Существует три системы градусов жесткости: немецкая, французская, английская. За один немецкий градус жесткости принимается содержание в 1 л 10 мг CaO или 7,2 мг MgO. За один французский градус – содержание в 1 л воды 10 мг CaCO3 или 17,5 мг MgCO3. В английской системе одному градусу жесткости соответствует содержание в 1 л воды14 мг CaCO3 (точнее, в английских мерах, — 1 гран (64,79892 мг) CaCO3 на 1 галлон (4,546 л) воды). Для перевода из одной системы градусов в другую можно воспользоваться такими соотношениями: 1,0 0 жестк. нем. = 1,79 0 жестк. франц. = 1,25 0 жестк. англ. 0,56 0 жестк. нем. = 1,0 0 жестк. франц. = 0,7 0 жестк. англ. 0,8 0 жестк. нем. = 1,43 0 жестк. франц. = 1,0 0 жестк. англ. Количество солей, мг/л, из которых каждая в отдельности обусловливает 1 0 жесткости, представлены ниже: 1,0 0 жестк. нем. 10,0 7,2 17,9 8,0 19,7 17,0 25,0 21,5 1,0 0 жестк. франц. 5,6 4,0 10,0 4,4 11,0 9,5 14,0 12,0 1,0 0 жестк. англ. 8,0 5,8 14,0 6,4 15,8 13,6 20,1 17,2 В настоящее время в нашем государстве вместо жесткости в градусах введено понятие жесткости в миллиграмм-эквивалентах на литр. За единицу жесткости принимают 1 мг-экв Ca, т.е.20,04 мг Ca на 1 л воды. Вместо кальция может быть принят 1 мг-экв магния, т.е. 12,16 мг Mg на 1 л воды. Для перевода из системы градусов жесткости (немецких) в миллиграмм-эквиваленты и обратно можно воспользоваться такими соотношениями: 1 мг-экв/л соответствует 2,8 0 жест. (нем.); 0,357 мг-экв/л соответствует 1,0 0 жест. (нем.). Жесткость природных вод колеблется в пределах от нескольких до десятков и сотен мг-экв/л; в одном и том же водоисточнике жесткость неодинаковая в разные времена года. В случае необходимости использования жестких вод для тех или иных целей их приходится обрабатывать специальными способами для снижения жесткости до требуемых норм. Природные воды по общей жесткости О.А. Алекин подразделяет на пять групп (табл. 6): Таблица 6 — Классификация природных вод по общей жескости
2.2.5 Оценка воды по активной реакции. Как уже отмечалось, в воде часть молекул всегда находится в диссоциированном состоянии, в виде ионов H + и OH — . Концентрация недиссоциированной воды считается постоянной, поэтому произведение ионов водорода и ионов гидроксила при данной температуре тоже будет величиной постоянной. При температуре 22 0 C эта величина равна 10 -14 . Так как чистая вода имеет нейтральную реакцию, количества ионов водорода и ионов гидроксила должны быть равны. Следовательно, Это выражение означает, что в 1 л чистой воды при 22 0 C содержится 10 -7 грамм-молекул воды в ионизированном виде, т.е. 10 -7 грамм-ионов водорода и 10 -7 грамм-ионов гидроксила. Если [H + ] = 10 -7 , то lg[H + ] = -7 и — lg[H + ] = 7. Выражение — lg[H + ] означает pH. Следовательно, если pH 7 – щелочная. По величине активной реакции или водородного показателя pH природные воды классифицируются следующим образом (табл. 7): Таблица 7 — Классификация природных вод по активной реакции
Подземные воды в большинстве своем имеют слабощелочную реакцию. Воды сульфидных и особенно колчеданных и каменноугольных месторождений обычно кислые и часто весьма кислые. Определять концентрацию водородных ионов необходимо на месте взятия пробы; наиболее употребительный способ определения – колориметрический, основанный на свойстве индикаторов менять окраску в зависимости от концентрации водородных ионов. 2.2.6 Агрессивные свойства подземных вод. Отрицательное воздействие подземных вод на металл и бетон называется агрессивностью воды. Это свойство обусловлено присутствием в воде ионов бикарбоната, водорода, агрессивной углекислоты, сульфатов и магния. В связи с этим различают агрессивность выщелачивания, общекислотную, углекислую, сульфатную и магнезиальную. Оценку различных видов агрессивности проводят по справочнику «Нормы и технические условия. Бетон гидротехнический. Признаки и нормы агрессивности воды-среды». Наличие натриевых и калиевых солей вызывает образование накипи. Свободный ион H + вызывает разъедание стенок котлов и труб. Временная (устранимая) жесткость воды является с этой точки зрения положительным фактором, так как ионы HCO3 — связывают свободные ионы H + . Кроме ионов водорода разъедающее действие на металл оказывают ионы кислорода, углекислоты, сероводорода. Поэтому вода, применяемая для технических целей, нуждается в предварительной обработке. После обработки вода по большей части становится непригодной для питья. Агрессивность выщелачивания возникает при малом содержании в воде HCO3 — (менее 1,5 мг-экв/л). В этих условиях происходит растворение и вымывание из бетона содержащейся в нем извести. Общекислотная агрессивность обусловлена низким значением водородного показателя pH (менее 5), из-за чего усиливается растворение извести бетона. Углекислая агрессивность возникает в результате действия агрессивной углекислоты CO2. В процессе взаимодействия с водой из цемента выделяется свободная известь CaCO3, которая реагирует со свободной углекислотой CO2. Реакция идет по схеме CaCO3 + CO2 + H2O = Ca(HCO3)2. Образующийся при этом бигидрокарбонат кальция является растворимым и легко выносится из бетона. Вода для большинства марок цемента становится агрессивной, если содержание в ней свободной углекислоты больше величины, определяемой по формуле a∙Ca + b. Содержание Ca 2+ выражается в мг/л, а коэффициенты a и b определяются в зависимости от карбонатной жесткости HCO3 — (мг-экв/л) и суммарного содержания ионов Cl — + SO4 2- в мг/л по специальной таблице 14. Сульфатная агрессивность возникает при наличии в воде повышенного количества сульфата SO4 2- ; в бетоне происходит кристаллизация новых соединений, образование которых сопровождается увеличением объема, вследствие чего происходит разрушение бетона. Такими новыми соединениями являются гипс CaSO4 ∙ 2H2O и сульфоаллюминат кальция 3CaO ∙ Al2O3 ∙ 3CaSO4 ∙ 31H2O (цементная бацилла). При образовании гипса объем бетона увеличится в два раза, а при образовании цементной бациллы – в 2,5 раза. При содержании в воде SO4 2- менее 250 мг/л сульфатная агрессивность отсутствует независимо от содержания хлора Cl — . Вода становится агрессивной по отношению к обычным портландцементам, если содержание ионов SO4 2- будет больше приведенных ниже показателей с учетом содержания в воде ионов хлора Cl — (мг/л): Cl — — менее 1000 SO4 2- — 250 Магнезиальная агрессивность, подобно сульфатной, ведет к разрушению бетона при соприкосновении его с водой, содержащей повышенное количество Mg 2+ . При этом, если содержание ионов магния Mg 2+ будет меньше 1000 мг/л, вода считается магнезиально – неагрессивной независимо от содержания иона SO4 2- (мг/л). При содержании ионов магния Mg 2+ более 1000 мг/л и больше величины, определяемой по формуле К- SO4 2- , вода считается агрессивной. Величина К для обычного портланд — цемента равна 7000. 2.2.7 Классификация подземных вод по химическому составу. Единой общепринятой классификации подземных вод в зависимости от их химического состава нет, что объясняется чрезвычайно разнообразным качественным и количественным химическим составом природных вод. Наиболее удобны те классификации, которые построены на принципе деления вод по преобладающим ионам (катионам и анионам) и по соотношению между ними. Именно на этом принципе построена классификация О.А. Алекина, широко используемая в геолого–разведочной, горной промышленности, гидротехнике и коммунальном хозяйстве. В соответствии с этой классификацией все природные воды по преобладающему в них аниону делятся на три больших класса – гидрокарбонатные, хлоридные и сульфатные. Каждый класс, в свою очередь, по преобладающему катиону делится на три группы – натриевые, кальциевые и магниевые. Группы по соотношению между ионами подразделяются на четыре типа: I тип: HCO3 — > Ca 2+ + Mg 2+ — воды маломинерализованные; II тип: HCO3 — 2+ + Mg 2+ — + SO4 2- — воды умеренной минерализации; III тип: HCO3 — + SO4 2- 2+ + Mg 2+ или, что то же самое, Cl — > Na + — воды высокоминерализованные; IV тип — HCO3 — = 0 – воды кислые, имеются только в сульфатном и хлоридном классе. Для удобства сопоставления анализов воды используют различные способы сокращенного изображения состава. Наиболее часто применяются формула М.Г. Курлова, графические – прямоугольник солевого состава Н.И. Толстихина и треугольники Фере ионного состава. Формула М.Г. Курлова представляет собой псевдодробь, где в числителе располагаются по убывающей анионы с индексом, равным содержанию данного иона в экв/%, в знаменателе — в такой же последовательности катионы. Ионы, содержание которых не превышает 10 экв/%, в формулу не включаются. Количество анионов и катионов округляется до целого числа. Перед дробью даются значение минерализации (М) с индексом, равным количеству сухого остатка в г/л, а также содержание элементов и газов с индексами, равными их содержанию в мг/л. После дроби указываются температура воды в градусах (t 0 C) и активная реакция воды (pH). В наименовании состава воды рекомендуется называть первыми анионы, затем катионы, а также элементы и газы. Ионы, содержание которых в воде менее 25%, не называются. Прямоугольник солевого состава Н.И. Толстихина (рис. 13) состоит из трех вертикальных граф. Левая и правая графы делятся на 10 равных частей, каждая часть приравнивается 10%. Нумерация производится снизу вверх. В левой графе изображаются катионы, в правой – анионы в экв/%. В средней графе показывают состав и процентное содержание солей, которые образуются в результате реакции катионов и анионов. Катионы и анионы на графике располагаются снизу вверх в последовательности, определяемой относительной реактивной силой: K + , Na + , Mg 2+ , Ca 2+ , Fe 2+ , NO3 — , Cl — , Br — , I — , SO4 2- , HCO3 — , CO3 2- .
Рисунок 13 – Прямоугольник солевого состава Треугольники Фере ионного состава (рис. 14) составляются отдельно для катионов и анионов, содержание которых дается в экв/%. В произвольном масштабе вычерчиваются два равносторонних треугольника, в вершинах которых располагаются катионы и анионы. Считается, что в вершине количество каждого катиона и аниона равно 100%. Далее, каждая сторона треугольника делится на 10 равных отрезков, соответствующих 10-ти процентам. Содержание катиона или аниона откладывается в виде точек на двух прилежащих к этой вершине сторонах треугольника. Эти точки затем соединяются прямой линией, параллельной третьей стороне. В итоге в каждом треугольнике получится по три прямые линии, точка пересечения которых графически изображает химический состав воды. 2.2.8 Оценка воды для питьевого водоснабжения. Вода, используемаядля хозяйственно-питьевого водоснабжения, должна удовлетворять требованиям ГОСТ — 2874-82 «Вода питьевая, технические требования к качеству». Согласно этого стандарта ниже приведены предельно-допустимые концентрации (ПДК) для некоторых показателей (табл. 8): Таблица 8 — Нормативы ГОСТ 2874-82
При отсутствии источника с пресной водой разрешается использовать воду с сухим остатком до 1500 мг/л, при общей жесткости до 10 мг-экв/л. В каждом случае возможность использования таких вод должна быть согласована с органами санитарно-эпидемиологической службы. Питьевая вода должна быть прозрачна, бесцветна, не иметь запаха, быть приятной на вкус. Золотисто-желтая или бурая окраска воды свидетельствует о наличии в ней растворенных органических веществ. Соленый вкус обуславливается значительным количеством NaCl, а горький – присутствием MgSO4. Наличие в воде солей азотной и азотистой кислот, а также аммиака указывает на связь этой воды с участками, где происходит разложение органических веществ, следовательно, на возможность наличия болезнетворных бактерий. Кроме того, пригодность воды для питья определяется по наличию кишечной палочки Coli. Сама по себе кишечная палочка безвредна, но ее наличие также свидетельствует о возможном присутствии болезнетворных бактерий. Количественные показатели определяются коли-тиром, т,е. наименьшим количеством кубических сантиметров воды, содержащим одну кишечную палочку (300 см 3 ), или коли-тестом, т.е. наибольшим количеством кишечных палочек, содержащихся в 1 л воды ( 0 C | Второ-степен. компо-ненты, мг/л | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Na + + K + | Ca 2+ | Mg 2+ | HCO3 — | SO4 2- | Cl — | ||||||||||||||||||||||||||||||||||||||||||||||
| 25,0 | 6,5 | 33,0 | CO2=18 Br2=0,6 |
Выполнить следующие виды работ:
а) Пересчитать результаты анализа из ионной формы в миллиграмм-эквивалентную и эквивалент-процентную формы и составить таблицу.
б) Оценить воду по степени минерализации.
в) Определить и оценить воду по всем видам жесткости.
д) Определить и оценить воду по всем видам агрессивности.
е) Произвести классификацию подземных вод по химическому составу.
ж) Выразить химический состав подземных вод в виде:
2) прямоугольника солевого состава
з) Оценить пригодность воды для питьевого водоснабжения.
Порядок выполнения работы
а) Для перерасчета результатов анализа согласно заданию составляется таблица 10.
В природной воде содержание K + составляет всего 4 – 10% от содержания Na + , поэтому все расчеты производятся по Na + .
Таблица 10 — Порядок пересчета из ионной формы в другие
| Основные ионы | мг/л | мг∙экв/л | экв./проц. | пересчетные коэффициен-ты | прочие определения, мг/л |
| Катионы: Na + K + Ca 2+ Mg 2+ | 482,85 20,96 106,86 | 79,07 3,43 17,50 | 0,0435 0,0256 0,0499 0,0822 | CO2=18,0 Br2=0,6 | |
| ∑ ∑r + Анионы HCO3 — Cl — SO4 2- ∑ ∑r — Всего | 610,67 1,15 545,67 56,16 602,98 | 0,19 90,50 9,31 | 0,0164 0,0282 0,0208 |
б) Определяем степень минерализации
Таблица 11 — Классификация подземных вод по общей минерализации
| Оценка воды (раствора) | Минерализация г/л |
| Пресная Солоноватая Соленая Горько-соленая Слабые рассолы Крепкие рассолы | До 1 1 – 3 3 – 10 10 – 50 50 – 100 >100 |
Согласно классификации данная вода горько-соленая (М = 34,940 г/л).
в) Определяем все виды жесткости
Общая жесткость равна 20,96 + 106,86 = 127,82 мг-экв/л
Карбонатная жесткость равна 1,15 мг-экв/л
Постоянная жесткость равна 127,82 – 1.15 = 126,67 мг-экв/л
Таблица 12 — Классификация природных вод по общей жесткости
| Оценка воды | Жесткость, мг-экв/л |
| Очень мягкая Мягкая Умеренно-жесткая Жесткая Очень жесткая | До 1,5 1,5 – 3,0 3,0 – 6,0 6,0 – 9,0 >9,0 |
Согласно таблицы 12 данная вода относится к очень жестким.
г) По значению активной реакции определяем pH среду
Таблица 13 — Классификация природных вод по активной реакции
| Признак | Значение pH |
| Весьма кислые Кислые Нейтральные Слабощелочные Высокощелочные | 9 |
Так как в нашем анализе pH = 6,5, данная среда – кислая.
д) Определяем агрессивные свойства данной воды
— так как значение HCO3 — равно 1,15 мг-экв/л, т.е меньше 1,5 мг-экв/л, агрессивность выщелачивания присутствует;
— так как pH = 6,5, больше 5,0, общекислотная агрессивность отсутствует;
— в нашем анализе содержание свободной углекислоты составляет 18,0 мг/л. Из таблицы 14 берем значения коэффициентов a = 0,00 и b = 17. Вычисляем по формуле: a∙Ca + b = 17. Так как содержание свободной углекислоты составляет 18,0 мг/л, т.е. больше, чем определенное по формуле, углекислая агрессивность присутствует.
— Так как в данном анализе содержание SO4 2- составляет 2700 мг/л при содержании Cl — = 19350 мг/л, сульфатная агрессивность присутствует.
— Содержание Mg 2+ составляет 1300 мг/л (>1000), применяем формулу К — SO4 2- , т.е. 7000 – 2700 = 4300, 1300 0 C pH6,5 ( 5 )
По химическому составу вода хлоридно-натриевая, бромисто-углекислая.
Рисунок 15—Прямоугольник солевого состава.
з) Оценка воды для питьевого водоснабжения
Таблица 15 — Нормативы ГОСТ 2874-82
| № | Показатель | ПДК, не более | Данные анализа |
| Активная реакция, pH Сухой остаток, мг/л Общая жесткость, мг∙экв/л Хлориды Cl — , мг/л Сульфаты SO4 2 , мг/л | 6,0 – 9,0 | 6,5 127,82 |
Вывод: Данная вода по сухому остатку, общей жесткости, содержанию хлоридов и сульфатов не подходит для практического применения.
Таблица 14 — Значения коэффициентов «a» и «b» для определения углекислой агрессивности водной среды.
| Карбонат. жестк. мг-экв/л | Суммарное содержание Cl — + SO4 2- | ||||||||||
| 0 — 200 | 201 -400 | 401 — 600 | 601 — 800 | 801 — 1000 | >1000 | ||||||
| a | b | a | b | a | b | a | b | a | b | b | b |
| 1,4 1,8 2,1 2,5 2,9 3,2 3,6 4,0 4,3 4,7 5,0 5,4 5,7 6,1 6,4 6,8 7,1 7,5 7,8 8,2 8,6 9,0 | 0,01 0,04 0,07 0,10 0,13 0,16 0,20 0,24 0,28 0,32 0,36 0,40 0,44 0,48 0,54 0,61 0,67 0,74 0,81 0,88 0,96 1,04 | 0,01 0,04 0,06 0,08 0,11 0,14 0,17 0,20 0,24 0,28 0,32 0,36 0,40 0,44 0,47 0,51 0,55 0,60 0,65 0,70 0,76 0,81 | 0,01 0,03 0,05 0,07 0,09 0,11 0,14 0,16 0,19 0,22 0,25 0,29 0,32 0,36 0,40 0,44 0,48 0,53 0,58 0,63 0,68 0,73 | 0,00 0,02 0,04 0,06 0,08 0,10 0,12 0,15 0,17 0,20 0,23 0,26 0,29 0,33 0,36 0,40 0,44 0,48 0,53 0,58 0,63 0,67 | 0,00 0,02 0,04 0,06 0,07 0,09 0,11 0,13 0,16 0,19 0,22 0,24 0,27 0,30 0,33 0,37 0,41 0,45 0,49 0,53 0,57 0,61 | 0,00 0,02 0,04 0,05 0,07 0,08 0,10 0,12 0,14 0,17 0,19 0,22 0,25 0,28 0,31 0,34 0,38 0,41 0,44 0,48 0,52 0,56 |
Вопросы для контроля знаний студентов
1. Перечислите основные физические свойства подземных вод и показатели, которыми они характеризуются.
2. Что входит в понятие «состав подземных вод»?
3. Каковы источники минерализации подземных вод? Что входит в понятие общей минерализации воды?
4. Что называется агрессивной углекислотой? Перечислите все виды агрессивности воды по отношению к бетону.
5. Каковы свойства жесткой воды и в каких единицах выражается жесткость?
6. Почему при кипячении жесткость уменьшается?
7. Какой показатель pH должна иметь вода, чтобы ее можно было отнести к кислотной, активной по отношению к металлам?
8. Как оценивается пригодность воды для питьевых целей? При каком коли-титре вода считается допустимой к употреблению без кипячения?
9. Как проводится пересчет результатов анализа воды из весовой формы в эквивалент-процентную?
10. Чем отличаются минеральные воды от минерализованных?
Список использованных источников
1. Ларионов А.К. Занимательная гидрогеология. – М.: Недра, 1979. – 155 с.
2. Николадзе Г.И. Улучшение качества подземных вод. – М.: Стройиздат, 1988. – 366 с.
3. Пешковский Л.М., Перескокова Т.М. Инженерная геология. – М: Высшая школа, 1982. – 344 с.
4. Седенко М.В. Основы гидрогеологии и инженерной геологии. – М: Недра, 1979. – 216 с.
5. Ташенов К.М. Подготовка технической воды. – А: КазГАСА, 1977. – 173 с.
6. Толстой М.П., Малыгин В.А. Геология и гидрогеологи. – М: Недра, 1988. – 274 с.
источник
Как все жидкости, вода обладает особыми свойствами:
- вода мало изменяет свой объем при изменении давления и температуры, и в этом отношении она сходна с твердым телом и отличается от газа, который весьма сильно изменяет свой объем;
- вода обладает текучестью, т. е. не имеет собственной формы и принимает форму сосуда, в котором находится, и в этом отношении она отлична от твердого тела и сходна с газом.
Многие физические свойства воды являются аномальными и не обнаружены у других веществ. При плавлении вода не расширяется, как почти все остальные вещества, а сжимается. Плотность воды растет с повышением температуры от 0 до 4 ◦ C и лишь при более высоких температурах начинает уменьшаться. По сравнению с другими веществами вода отличается необычно высокими удельной теплоемкостью, удельной теплотой плавления и кипения.
Определяющее влияние на физические свойства подземных вод оказывают растворенные в них соли и газы, а также воздействие высоких давлений и температур в пластовых условиях.
Температура и давление подземных вод зависят от глубины залегания. С увеличением глубины залегания возрастает как температура, так и давление. При температуре 374 ◦C (критическая температура) исчезают различия физических свойств жидкости и пара. Вода при температуре выше 374 ◦ C находится в надкритическом состоянии. Критическая температура минерализованных водных растворов еще выше и может достигать 400–425 ◦ C.
Измерение давления высотой столба воды очень удобно и часто применяется на практике. Давление в 1 кгс/см 2 (техническая атмосфера) соответствует столбу пресной воды высотой 10 м. Таким образом, гидростатическое давление подземных вод увеличивается на 1 ат на каждые 10 м глубины. Между единицами измерения давления в разных системах существуют следующие соотношения:
1 ат = 1 кгс/см 2 = 10 м вод. ст. = 0,981 бар = 0,0981 МПа = 0,981 · 10 5 Па.
Гидростатическое давление определяется по формуле:
где P — гидростатическое давление, Па; ρ — плотность воды, кг/м 3 ; g — ускорение свободного падения, м/с 2 ; H — высота столба воды, м.
Давление в недрах подразделяется на горное и пластовое. Горное или геостатическое давление обусловлено силой тяжести перекрывающей толщи горных пород. Величина горного давления Pг определяется по формуле, аналогичной формуле (ηгеот = Qфак.год./ Qмак. год.), и имеет следующий вид:
Если давление измерять в мегапаскалях (МПа), то c = 102 000, если в кгс/см 2 , то c = 10000.
Пластовое давление (Pпл) — это давление жидкости, насыщающей горные породы, и по своему происхождению оно близко к гидростатическому давлению:
Для глубоких пластов платформенных бассейнов h равна примерно глубине залегания пласта от поверхности.
При температуре 4 ◦ C вода имеет максимальную плотность 1000 кг/м 3 . При температуре 100 ◦ C ее плотность — 958,4 кг/м 3 , при 300 ◦ C — 712,5 кг/м 3 . За счет пониженной плотности в недрах происходит конвективное восходящее движение нагретых подземных вод.
Плотность подземных вод зависит также от химического состава и концентрации растворенных солей. Если пресные подземные воды имеют плотность, близкую к 1000кг/м 3 , то плотность концентрированных рассолов достигает 1200 кг/м 3 и более.
Сжимаемость жидкости при изменении внешнего давления характеризуется коэффициентом сжимаемости (упругости). Он равен отношению изменения объема жидкости при изменении давления на единицу к первоначальному ее объему. Принято считать, что вода практически несжимаема. Коэффициент сжимаемости для чистой воды равен 5 · 10 −5 1/ат. Однако упругие свойства воды играют важнейшую роль в подземной гидродинамике, за счет упругих сил создается напор подземных вод.
Единица измерения коэффициента сжимаемости в международной системе (СИ) — 1/Па = м 2 /Н.
Температурное расширение жидкостей характеризуется коэффициентом температурного расширения. Он равен отношению изменения объема жидкости при изменении температуры на 1 ◦ C к первоначальному объему. Единица измерения коэффициента температурного расширения 1/ ◦ C.
Температура и давление действуют на плотность воды в противоположном направлении.
Вязкостью называется свойство жидкости сопротивляться сдвигающим усилиям. Вязкость проявляется только при движении жидкости как внутреннее трение или сопротивление скольжению жидких слоев друг относительно друга под действием внешних сил. Вязкость характеризуется коэффициентом абсолютной вязкости. Величину, обратную коэффициенту абсолютной вязкости, называют текучестью. В международной системе абсолютная вязкость измеряется в Па · с. Используется также кинематическая вязкость γ, равная частному от деления абсолютной вязкости μ на плотность ρ (γ = μ/ρ). В системе СИ кинематическая вязкость измеряется в м 2 /с.
Вязкость природных вод увеличивается с ростом минерализации, но основное влияние оказывает температура. Повышение температуры приводит к значительному уменьшению вязкости подземных вод, что значительно облегчает их фильтрацию через мельчайшие поры.
Температура и давление определяют, в каком состоянии (твердом, жидком или газообразном) находится вода в недрах. В большей части земной коры вода находится в жидком состоянии. Кипение подземных вод в глубоких горизонтах с температурой выше 100 ◦ C не происходит, так как с увеличением глубины возрастает давление и как следствие растет температура кипения воды. К примеру, под давлением 10 атм вода закипает при температуре 179 ◦ C. Такое давление подземных вод наблюдается на глубине 100 м, где температура значительно ниже точки кипения.
Вода обладает высокой растворяющей способностью. Подземные воды на путях своего движения соприкасаются с разнообразными горными породами и при взаимодействии с ними обогащаются многими химическими соединениями. Под химическим составом воды обычно понимают состав растворенных в воде веществ. В подземных водах найдено более 60 химических элементов в виде ионов, недиссоциированных молекул различных солей, коллоидов минерального и органического происхождения, газов.
Главными в природных водах являются шесть ионов, к которым относятся три аниона — хлор Cl − , сульфат SO 2− и гидрокарбонат HCO − 3 , и три катиона — натрий Na + , кальций Ca 2+ и магний Mg 2+ . Сочетание преобладающих в растворе ионов характеризует химический состав подземных вод (гидрокарбонатно-кальциевый, хлоридно-натриевый и т. д.).
Суммарное содержание в воде растворенных ионов, солей и коллоидов называется минерализацией воды. Она обычно выражается в граммах на один литр раствора (г/л). Минерализация природных вод изменяется в очень широких пределах. Имеется несколько классификаций природных вод по степени минерализации. По классификации В. И. Вернадского различают пресные воды (минерализация до 1 г/л), очень слабо соленые (1–10 г/л), слабосоленые (10–35 г/л), соленые (35–50 г/л), рассолы (более 50 г/л). Позднее другие исследователи (И.К. Зайцев, М. Г. Валяшко, Н.И. Толстихин и др.) предложили называть рассолами природные растворы с минерализацией 35 г/л, обосновывая это верхней границей солености океанической воды. Известны рассолы с содержанием солей до 700 г/л.
При разработке технологических систем с использованием термальных вод более удобным является следующая классификация:
- термальные воды с низкой минерализацией (до 10 г/л), которые могут использоваться без предварительной водоподготовки;
- термальные воды со средней минерализацией (10–35 г/л), требующие предварительной очистки, они могут использоваться только в двухконтурных системах;
- термальные воды с высокой минерализацией (35–200 г/л и более), которые могут использоваться только в двухконтурных системах.
Существуют определенные зависимости между минерализацией подземных вод и их химическим составом. Пресные воды относятся преимущественно к гидрокарбонатному типу. Хлористые соли хорошо растворимы, поэтому содержание хлоридов в подземных водах обычно растет одновременно с их минерализацией. В рассолах средней концентрации (до 150 г/л) часто преобладают ионы хлора и натрия, а в крепких рассолах — ионы хлора, кальция и магния.
Из общих химических свойств воды особое значение имеют реакция среды и жесткость.
Реакция среды, т. е. щелочно-кислотные свойства воды, определяются концентрацией ионов водорода H+, которая зависит от содержания в воде двуокиси углерода и гидролизующихся солей тяжелых металлов. В чистой воде, обладающей нейтральной реакцией, ионы водорода возникают за счет диссоциации самих молекул воды, причем их концентрация одинакова с концентрацией гидроксильных ионов OH − и равна 10 −7 г · ион/л. Поскольку эта величина очень малая, принято выражать концентрацию водородных ионов только показателем степени, взятым с обратным знаком, и обозначать через pH. Если среда имеет нейтральную реакцию, то ее pH = 7. В кислой среде pH меньше 7, в щелочной среде — больше 7.
Геотермальные воды подразделяются по значению pH: сильнокислые (pH ≤ 3,5); кислые (3,5 8,5).
Жесткость воды определяют по содержанию в воде ионов кальция и магния и выражают в мг-экв/л. Различают жесткость общую, карбонатную и некарбонатную. Общая жесткость воды определяется суммарным содержанием в ней кальция и магния. Карбонатная жесткость определяется наличием в воде бикарбонатов кальция и магния, некарбонатная жесткость — наличием солей сильных кислот кальция и магния.
По общей жесткости (Жо, мг-экв/л) воды подразделяются: очень мягкие (Жо ≤ 1,2); мягкие (1,2 11,7).
Воды с высокой карбонатной жесткостью дают накипные отложения в трубопроводах и теплообменных аппаратах энергетических установок.
На формирование химического состава подземных вод влияют следующие группы факторов:
- состав первоначальной воды в бассейне осадконакопления;
- степень промытости пород инфильтрационными водами;
- характер и интенсивность процессов взаимодействия вод с породами (выщелачивание пород, окислительно-восстановительные реакции, реакции катионного обмена и др.);
- интенсивность смешения и взаимного вытеснения вод разного происхождения и разного состава, а также ряд других процессов.
Формирование подземных вод происходит с момента их захоронения в толще осадков или поступления в горную породу. Происходит последовательное изменение минерализации и химического состава вод с глубиной. Гидрохимическая зональность подземных вод тесно связана с гидродинамической зональностью, под которой понимают изменение условий водообмена и степени подвижности подземных вод с глубиной.
Интенсивность водообмена в земной коре замедляется с глубиной. В гидрогеологии выделяют три гидродинамические зоны подземных вод: активного водообмена, затрудненной циркуляции и застойного режима.
С увеличением глубины и замедлением водообмена происходит возрастание минерализации подземных вод. Одновременно с ростом общей минерализации подземных вод по разрезу изменяется их химический состав. Пресные воды чаще всего имеют гидрокарбонатно-кальциевый состав; солоноватые по составу разнообразны, а соленые и рассолы, как правило, являются водами хлоридно-натриевого состава с увеличением в них содержания кальция и магния по мере роста минерализации. В верхней зоне активного водообмена (до глубины 500 м, а в некоторых артезианских бассейнах практически отсутствует) циркулируют инфильтрационные воды. С глубиной в пределах верхней зоны происходит постепенное нарастание минерализации, что отражает все более затрудненные условия водообмена и все меньшее влияние инфильтрации.
Формированию пресных и слабоминерализованных вод способствуют наличие раскрытых структур, где водоносные горизонты имеют выходы на поверхность в областях питания и разгрузки, большая мощность и высокая проницаемость водоносных пород, восходящие тектонические движения. Формированию соленых и рассольных вод благоприятствуют закрытые структуры, где связь водоносных горизонтов с поверхностью существенно затруднена, мала проницаемость водоносных пород, имеются соленосные отложения, нисходящие тектонические движения. При восходящих тектонических движениях усиливается инфильтрационный водообмен, водоносные слои освобождаются от минерализованных вод морского происхождения. При погружении слоев, напротив, происходит захоронение морских вод, выжимание воды из глин, что препятствует инфильтрационному водообмену.
В артезианских бассейнах наблюдается изменение состава подземных вод и повышение их минерализации от областей питания к областям разгрузки. Такая закономерность связана с тем, что по мере своего движения воды обогащаются солями. Наиболее резко возрастает минерализация подземных вод с глубиной в районах, где в разрезе присутствуют соленосные отложения. Концентрированные рассолы встречаются именно в таких районах.
Температура и давление оказывают существенное влияние на условия водообмена вод глубоких горизонтов и физико-химические процессы взаимодействия вод с горными породами. При высоких температурах снижается вязкость воды и увеличивается проницаемость пород, что облегчает водообмен. Условия водообмена зависят также от величины и природы давления, действующего на подземные воды, и градиентов давления.
С повышением температуры растворимость некоторых минералов резко увеличивается. Повышение температуры влияет также на сорбцию, диффузию и другие процессы, протекающие при взаимодействии воды с породой.
Химический состав вод определяют методами аналитической химии в специальных лабораториях. Содержание ионов выражают в массовой, эквивалентной и процент-эквивалентной формах.
Наиболее часто используется массовая форма, где содержание каждого иона выражается в миллиграммах (иногда в граммах) в 100 граммах или 1 литре раствора.
Для определения эквивалентной формы содержания данного иона необходимо его количество, выраженное в миллиграммах или граммах, разделить на эквивалент. Эквивалентом иона называют частное от деления ионной массы на валентность иона.
В эквивалентной форме сумма анионов всегда равна сумме катионов.
Процент-эквивалентная форма получается из эквивалентной формы. Она показывает относительную долю иона в общей сумме всех ионов. Общая сумма всех ионов, взятых в эквивалентной форме, приравнивается 100 %. Содержание каждого иона выражают в процентах от суммы всех ионов.
Для наглядного изображения состава вод также используют формулу М. Г. Курлова, представляющая собой дробь, где в числителе указано содержание анионов, а в знаменателе — содержание катионов в процент-эквивалентной форме, причем их сумма принимается за 200 %. Ионы записывают в убывающем порядке. Перед чертой отмечают главные компоненты газового состава и минерализацию в граммах на литр. После черты пишут температуру воды. Приведем пример:
Из приведенной формулы следует, что главным газовым компонентом является метан, минерализация воды равна 56 г/л, температура воды 65 ◦C, среди анионов 78% экв. хлор-иона и 22% экв. сульфат-иона, а среди катионов 48, 38 и 14% экв. натрия, кальция и магния соответственно.
По этой формуле легко классифицировать и систематизировать анализы химического состава природных вод.
Существуют несколько десятков классификаций подземных вод по ионному составу, но распространение получили немногие. В большинстве классификаций применяется процент-эквивалентная форма выражения состава вод. Во всех классификациях авторы считают, что таксономическое значение анионов выше, чем катионов. В результате воды разделены на три основных класса: гидрокарбонатные, сульфатные и хлоридные.
В классификации Н. И. Толстихина внутри классов выделены подклассы по преобладающему катиону — кальциевый, магниевый и натриевый.
По О. А. Алекину указанные классы также разделены по преобладающим катионам на три группы: кальциевую, магниевую и натриевую. В пределах групп по соотношению ионов устанавливаются четыре типа вод:
- воды первого типа характеризуются соотношением HCO − 3 > Ca 2+ + Mg 2+ , они обычно связаны с изверженными породами;
- воды второго типа определяются соотношением HCO − 3 2+ + Mg 2+ − 3 + SO 2− 4 и связаны с осадочными породами и продуктами их выветривания (поверхностные и грунтовые воды);
- для вод третьего типа характерно соотношение Cl − > Na + или HCO − 3 + SO 2− 4 2+ + Mg 2+ , к этому типу относятся воды морей и сильно минерализованные подземные воды;
- в водах четвертого типа HCO − 3 = 0, т. е. эти воды кислые и поэтому находятся только в сульфатном и хлоридном классах.
В своей классификации В. А. Сулин разделил воды на 4 типа по характерным соотношениям главных ионов: сульфатно-натриевый, гидрокарбонатно-натриевый, хлор-магниевый и хлор-кальциевый. Далее типы вод разделены на группы и подгруппы по преобладающему аниону и катиону.
Среди газов, сопутствующих подземным водам, наиболее широко распространены азот N2, углекислота CO2 , сероводород H2S, метан CH4, тяжелые углеводороды (этан C2H6, пропан C3H8, бутан C4H10 и др.). В малых количествах встречаются аргон Ar, гелий He и некоторые другие газы.
Растворимость газов в воде зависит от давления, температуры, химического состава воды и газа. Растворимость газов растет с повышением давления и уменьшается с повышением температуры. Растворимость газов в подземных водах увеличивается с глубиной, так как рост давления дает больший эффект, чем рост температуры.
Подземные воды, залегающие на больших глубинах, нередко содержат в растворенном состоянии значительное количество газов, достигающее 10 м 3 в 1 м 3 воды. По прогнозным оценкам общее количество углеводородных и других газов, растворенных в подземных водах, на два порядка больше, чем в газовых и нефтегазовых залежах. Газовый и ионный составы подземных вод тесно связаны друг с другом. При увеличении концентрации растворенных в воде солей растворимость газов падает. В свою очередь, наличие в воде растворенных газов влияет на переход в раствор некоторых солей, а дегазация воды может повлечь частичное выпадение солей в осадок.
Необходимо отметить, что в подземных водах повсеместно содержатся и органические вещества. Общее количество органического углерода в подземных водах составляет десятки и сотни миллиграммов в 1 л. В них установлено наличие углеводородов, органических кислот, фенолов и других соединений. Органические вещества поступают в подземные воды в результате биохимических процессов, выщелачивания из горных пород и взаимодействия с нефтяными залежами.
В зависимости от газового состава, а также геологических, геохимических и температурных условий формирования выделяются пять основных генетических типов термальных подземных вод: сероводородно-углекислые (фумарольные), углекислые, азотно-углекислые, азотные (щелочные) и метановые.
Сероводородно-углекислые геотермальные воды формируются в зоне непосредственного воздействия очагов современной вулканической деятельности и распространены на Камчатке и Курильских островах. Они подразделяются на термы глубинного происхождения, насыщенные высокотемпературными газами, и поверхностного происхождения, залегающие в верхних слоях вулканогенных пород. Минерализация сероводородно-углекислых терм обычно невелика (3–5 г/л), но иногда достигает 20 г/л и более. Преобладающими среди анионов являются хлориды и сульфаты. Температура вод колеблется от 40 до 100 ◦ C.
Углекислые геотермальные воды генетически связаны с толщами осадочных отложений, прорванных молодыми магматическими породами. Углекислота, насыщающая подземные воды в сфере магматических очагов, образуется при воздействии высоких температур на окружающие породы. Химический состав сложный и разнообразный. Содержание кремниевой кислоты доходит до 200 мг/л, а общая минерализация от 2 до 40 г/л. Углекислые воды распространены в восточной Камчатке, на Памире и в районе Кавказских минеральных вод (Пятигорск, Железноводск, Ессентуки).
Азотно-углекислые геотермальные воды (парогидротермы) — сильно перегретые воды, температура которых на сравнительно небольшой глубине достигает 200–300 ◦ C. На поверхности воды появляются в виде пароводяных струй (гейзеры) или кипящих источников. При вскрытии таких вод скважинами также образуются пароводяные фонтаны. Формирование азотно-углекислых терм происходит в восстановительных высокотемпературных условиях в непосредственной близости от активно действующих вулканов. Приурочены такие воды к вулканическим или вулканогенным осадочным породам. Встречаются на Камчатке (Долина Гейзеров, Паужетские источники), в Новой Зеландии, Италии, Исландии. Азотно-углекислые термы характеризуются обычно невысокой минерализацией (2–5 г/л) и хлоридно-натриевым составом. Отличительной чертой таких вод является высокое содержание кремниевой кислоты (300–600 мг/л).
Азотные (щелочные) геотермальные воды бывают как атмосферного и глубинного, так и морского происхождения. Они широко распространены в горно-складчатых и платформенных областях. Вода атмосферного происхождения характеризуется низкой минерализацией (менее 1,5 г/л), гидрокарбонатно-натриевым и сульфатно-натриевым составом и высоким содержанием кремниевой кислоты (до 200 мг/л). Формирование химического состава этих вод происходит в результате выщелачивания пород инфильтрационными водами. Вода морского происхождения отличается высокой минерализацией (до 40 г/л), хлоридно-натриевым составом и наличием характерных микрокомпонентов — брома и йода.
Метановые геотермальные воды широко распространены в нефтегазоносных артезианских бассейнах Русской и Сибирской платформ, Западно-Сибирской низменности, Северного Кавказа и других районов. Эти воды приурочены к осадочным отложениям глубинных частей артезианских бассейнов. Минерализация вод составляет от нескольких граммов до 400–500 г/л. Воды малой минерализации по составу являются гидрокарбонатно-натриевыми, высокоминерализованные воды и рассолы имеют хлоридно-натриевый состав.
Газонасыщенность (Г, мг/л) термальных вод характеризуется как слабая (Г ≤ 100), средняя (100 1000).
источник