Грунтовые воды залегают на первом от земной поверхности водоупорном слое. Они представляют собой разновидность подземных вод.
В регионах, где наблюдается климат с повышенной влажностью, процессы инфильтрации (впитывания) протекают более оживленно, вследствие чего уменьшается содержание минералов и солей в почвах и горных породах. Иногда присутствует обратный процесс: чрезмерное испарение влаги, содержащейся в грунтах, это приводит к повышению в них концентрации солей.
Стандартное исследование грунтовой воды – обязательная процедура при совершении инженерно-геологических исследований участка, который планируется под застройку. Выполнение стандартного анализа вод этого типа совершается в лабораторных условиях, так как для определения степени жесткости образца, его минерализации, способности оказывать разрушающее действие на стройматериалы необходимо специальное оборудование.
Минерализация воды – количественный показатель, указывающий концентрацию солей в жидкости. Для определения этого параметра вода выпаривается, затем проводится анализ образовавшихся в результате твердых веществ.
- Пресная – соли отсутствуют; Слабоминерализованная: на литр воды приходится 1-2 г солей; Малая: содержание солей колеблется в пределах 2-5 г/л; Среднеминерализованная, концентрация минеральных веществ составляет 5-15 г/л; Высокоминерализованная (15-30 мг/л); Рассол (30-150 мг солей на литр воды); Крепкий рассол (в литре жидкости содержится 150 г солей и больше).
Жесткость грунтовых вод – важный показатель, если речь идет о создании скважины для добычи питьевой воды. Определяется параметр содержанием ионов магния и кальция. Степень чистоты грунтовой воды, отсутствие в ней вредных веществ – эти свойства свидетельствуют и об отсутствии загрязнений грунта, что особенно важно при строительстве жилых объектов.
Показатель агрессивности, способности разрушать стройматериалы, также важен, он обязательно исследуется при совершении инженерных изысканий на стройплощадке. Под действием химических веществ, содержащихся в грунтовых водах, бетон и другие строительные материалы могут утратить свою прочность. Поэтому стандартный анализ грунтовой воды обязательно включает в себя определение агрессивности среды. Она бывает следующих видов:
- Углекислотная; Общекислотная; Магнезиальная; Сульфатная; Выщелачивающая.
При исследовании грунтовой воды определяют показатель кислотно-щелочного баланса. Он измеряется в единицах, нейтральное значение равно 7. Если параметр рН меньше этой цифры, значит вода кислотная: она оказывает разрушающее действие на бетон. При этом не важно, какой именно портландцемент входит в бетонную смесь.
Насколько сильным будет разрушающее действие такой воды, зависит от содержания в ней кислоты, ее способности к регенерации, скорости восстановительных процессов и давления, оказываемого грунтовой водой на бетон. Имеет значение и состав бетона: содержание в нем цемента, используемый наполнитель.
Показатель рН указывает на присутствие кислоты и ее концентрацию. Этот параметр становится известным после проведения предварительного исследования грунтовых вод. Для установления, какое именно вещество входит в состав жидкости, и с целью узнать его концентрацию проводится химический анализ.
При низком показателе рН можно утверждать, что в воде присутствуют органические кислоты и растворенная углекислота. Иногда в грунтовые воды попадают соединения серной и сернистой кислот, содержащихся в торфяных почвах. При наличии значительного агрессивного влияния грунтовых вод следует позаботиться об улучшении качества бетона: повысить содержание цемента, снизить количество воды в смеси.
Приступать к выбору строительных материалов и проектированию фундамента следует после определения качественных и количественных показателей грунтовых вод. Имея результаты этих исследований, можно избежать многих неприятностей:
- Усадки и разрушения фундамента; Появления в здании трещин; Сезонных затоплений грунтовыми водами; Иных негативных факторов.
Знание о возможных проблемах позволяет еще на начальном этапе работы над проектом объекта создать систему защиты (дренаж), подобрать оптимально подходящий для имеющихся условий фундамент. Если не планируется строительство подвального этажа, можно обойтись оборудованием качественной изоляции от влаги, которая будет препятствовать увлажнению стен. Иногда необходима гидроизоляция фундамента.
источник
Тел: +7 (495) 728-94-19
Тел: +7 (963) 659-59-00
Москва, Олонецкий пр. д. 4/2
выполняем работы по г. Москве
и всей Московской области
Геология
Грунтовая лаборатория
Грунтовая лаборатория
Оснащенность лаборатории
Область аккредитации
Типы исследуемых грунтов
песчаные грунты
глины, суглинки, супеси
заторфованные грунты
техногенные грунты
Механические свойства грунтов
испытания грунтов на срез
компрессионные испытания
трехосное сжатие
свободное набухание
Физические свойства грунтов
гранулометрический состав
природная влажность
показатель текучести
предел пластичности
пористость, коэфф. пористости
определение плотности грунта
Химический анализ
химанализ водной вытяжки
коррозийная агрессивность
Библиотека
ООО «Буровики»:
Контакты
Рекомендательные письма
Допуски и Лицензии
Цены и сроки, прайс лист
Написать письмо
1 400 рублей за метр. Подробнее
Почему стоит заказать именно у нас
Грунтовые воды относятся к разновидностям подземных вод, которые залегают на водоупоре, расположенном ближе к поверхности. На территориях с влажным климатом происходит развитие интенсивных процессов инфильтрации, а также подземного стока, что приводит к выщелачиванию грунтов и горных пород. В некоторых случаях происходит излишнее их испарение, что приводит к засолению почвы. Поэтому стандартный анализ грунтовой воды, когда выполняются инженерно-геологические изыскания для проектирования зданий (сооружений), считается обязательным.
Стандартный анализ грунтовой воды выполняется в условиях лаборатории для получения показателей минерализации образца, его жесткости, агрессивности по отношению к различным материалам строительства (в первую очередь к стали, бетону и алюминиевым оболочкам кабелей), электропроводность и т.д. Минерализацией следует считать сумму всех минеральных веществ, которые растворены в грунтовой воде. Данный показатель получается методом выпаривания исследуемого образца. Следует различать такие степени минерализации грунтовых вод:
Жёсткость грунтовой воды определяется исходя из наличия ионов кальция и магния. Эти химические показатели важны при бурении скважин для поиска пресной воды населению. Также под застройку домов (коттеджей, сооружений) геология участка исследуется на показатель чистоты и безопасности для проживания в данной местности. А, как известно грунтовые воды являются главными показателями чистоты грунта.
Проводя инженерные изыскания на отводимом участке (площадке) важно учитывать фактор агрессивности грунтовых вод. Грунтовые воды могут оказывать разрушающий эффект для бетона и других строительных материалов. Для этого в условиях лаборатории стандартный анализ грунтовой воды выполняется также для получения показателя агрессивности. Агрессивность грунтовых вод бывает таких типов:
- выщелачивающая;
- общекислотная;
- сульфатная;
- магнезиальная;
- углекислотная
СП 11-105-97 Часть I. Общие правила производства работ Приложение Н (обязательное)
Показатели химического состава подземных и поверхностных вод
и методы их лабораторных определений при инженерно-геологических изысканиях
Показатели химического состава воды
Коррозионная активность воды к оболочкам кабелей
Метод испытания или обозначение государственного
стандарта на методы определения
температура в момент взятия пробы, °С
вкус и привкус при температуре 20 °С
Примечание — При проведении комплексных изысканий состав определяемых компонентов следует устанавливать с учетом требований СП 11-102-97
Результаты анализа грунтовой воды позволяет определить уровень ее рН. Если он пребывает ниже уровня нейтрального значения, которое составляет 7 единиц, то вода является кислотной. В таком случае она может разрушать бетон, вне зависимости от того, какого типа портландцемент использован в нем. Степень разрушения также зависит от вида и концентрации кислоты, возможности непрерывного обновления кислоты, скорости течения и давление грунтовой воды на бетон, расхода цемента, непроницаемости бетона и типа заполнителя.
Сама по себе величина рН является определяющим фактором вида или концентрации присутствующей кислоты, ведь это всего лишь мера степени кислотности. В качестве предварительных данных измерения рН очень полезны и позволяют получить представление о наличии или отсутствии кислот. Однако в большинстве случаев необходимым является проведение химического анализа, при котором определяется характер и концентрация кислоты. Как правило, кислотность естественных грунтовых вод, которые имеют низкий рН, вызвана органическими кислотами и растворенной углекислотой, а также, в отдельных случаях, сернистой и серной кислотой, которая поступает из соединений серы в торфяных грунтах. По мере увеличения интенсивности агрессивного воздействия можно повышать качество бетона, например, увеличивать расход цемента с более низким водоцементным отношением.
В зависимости от типа агрессивности грунтовых вод проектировщик принимает решения по выбору материала для строительства строения, а также глубины фундамента.
Анализ грунтовой воды необходим для получения детальной информации об участке исследований. Зная особенности данной жидкости можно своевременно предотвратить неприятные последствия: разрушение, усадка фундамента, трещины на здании, сезонное подтопление и т.д. Для этого проектировщики на первоначальных стадиях проектирования объекта планируют защитные мероприятия (дренажную систему), а также по возможности выбирают более подходящий для данной среды тип фундамента. Для зданий, не имеющих подвальных помещений и при высоком уровне грунтовых вод достаточно просто изолировать стены строения от влаги (не дать возможности поднятию уровня грунтовых вод по стенам). В некоторых случаях выполняют гидроизоляцию фундамента. В любом случае, необходимо учитывать тот факт, что грунтовые воды неблагоприятно влияют на строение в разные времена года (особенно зимой и во время таяния) и заранее принимать меры по их устранению.
источник
Химический анализ подземных вод может служить качественным показателем использования воды для хозяйственно-питьевого водоснабжения, бальнеологических, промышленных и хозяйственных целей, а также диагностическим признаком при гидрохимических методах поисков и разведки месторождений полезных ископаемых.
Результаты химического анализа подземных вод могут быть выражены в табличной или сокращенной отчетной форме в виде формулы Курлова.
1). Табличная форма выражения химического анализа.
Количественно концентрация катионов и анионов выражается в г/дм 3 , мг/дм 3 , а эквивалентное содержание – миллимолях (ммоль) и процентах (%).
Пример расчета химического анализа воды в табличной форме приводится ниже.
| Ионы | Содержание, мг/дм 3 | Эквивалентное содержание | |
| ммоль | % | ||
| Na + Ca 2+ Mg 2+ | 88,04 22,75 15,62 | 69,9 17,6 12,5 | |
| Сумма катионов | — | 126,41 | |
| Cl — SO4 2 — HCO3 — | 98,40 17,43 3,51 | 82,5 14,5 3,0 | |
| Сумма анионов | — | 119,34 | |
| М (сухой остаток) | — | — | |
| СО2(свободный) | — | — | |
| рН водородный показатель | 5,3 | — | — |
| Т воды, градус С | — | — |
Эквивалентное (молярное) содержание определяется путем умножения каждого иона на пересчетный коэффициент, учитывающий его атомный вес и валентность и представляющий собой величины, обратные эквивалентным массам ионов (таблица 2).
| Катионы | Коэффициент | Анионы | Коэффициент |
| Na + Ca 2+ Mg 2+ | 0,0435 0,0499 0,08222 | Cl — SO4 2- HCO3 — | 0,0282 0,0208 0,0164 |
Для пересчета в %-эквивалентную форму суммы катионов и анионов в миллимолях принимаются за 100%, а затем определяется доля каждого катиона и аниона в % от соответствующей суммы катионов и анионов.
Химический анализ считается достоверным, если ошибка анализа не превышает 5%.
В нашем случае С = 2,88%. Анализ достоверен.
2) Сокращенная форма выражения химического анализа (формула М.Г. Курлова)
Формула Курлова представляет собой псевдодробь, в числителе которой в порядке убывания в %-эквивалентной форме располагаются анионы, а в знаменателе – катионы. Ионы, содержание которых менее 1%, в формулу не включаются. Проценты округляют до целых чисел.
Слева от дроби указывается содержание газов в мг/дм 3 и минерализация (М) в г/дм 3 , за которую принимается сухой остаток. Справа записывают значение (рН), температуру воды (Т) в градусах Цельсия, дебит источника в м 3 /сут и содержание микроэлементов, если такие имеются.
В нашем случае формула Курлова (таблица 1):
3) Наименование воды по химическому составу.
Наименование химического типа подземных вод должно состоять из двух частей, отражающих преобладающий анионный и катионный состав воды. Наименование химического типа воды начинается с ее анионного, а затем катионного состава в %-эквивалентной форме, превышающего 20% от суммы миллимолярной концентрации. Перечисление ионов производится в порядке возрастания концентрации – от меньшего значения к большему.
В сокращенном анализе анионы представлены хлоридами, сульфатами и гидрокарбонатами, а катионы – натрием, кальцием и магнием. В нашем случае вода хлоридно-натриевая.
4) Классификация воды по минерализации.
В зависимости от величины минерализации, за которую принимается сухой остаток, подземные воды классифицируются в соответствии с приведенной таблицей 3.
| Минерализация М, г/дм 3 | Подгруппа | Группа |
| £ 0,5 >0,5-1,0 | Весьма пресные Пресные | Пресные |
| >1,0-1,5 >1,5-3,0 >3,0-5,0 >5,0-10,0 >10,0-25,0 | Весьма слабосолоноватые Слабо солоноватые Умеренно солоноватые Солоноватые Сильно солоноватые | Солоноватые |
| >25,0-36,0 >36,0-50,0 | Слабосоленые Сильносоленые | Соленые |
| >50,0-150,0 >150,0-350,0 >350,0 | Рассолы слабые Рассолы крепкие Рассолы весьма крепкие (рапа) | Рассолы |
В нашем случае М = 6,9 г/дм 3 . Вода солоноватая.
Реакция воды обусловлена величиной концентрации водородных ионов рН, которая представляет собой обратный логарифм концентрации ионов водорода. Классификация воды по водородному показателю приведена в таблице 4.
| Водородный показатель рН при Т22 о С | Подгруппа | Группа |
| £ 3,5 >3,5-4,5 >4,5-5,5 >5,5-6,0 | Весьма кислая Кислая Умеренно кислая Слабокислая | Кислая |
| >6,0-8,0 | Нейтральная | Нейтральная |
| >8,0-8,5 >8,5-9,0 >9,0-9,5 >9,5 | Слабощелочная Умеренно щелочная Щелочная Весьма щелочная | Щелочная |
В нашем случае рН = 5,3. Вода умеренно кислая.
6) Классификация подземных вод по температуре воды.
Классификация воды по температуре приведена в таблице 5.
| Температура, Т о С | Наименование |
| 0-4 >4-20 >20-37 >37-50 >50-75 >75-100 >100-200 >200-374 | Переохлажденная Очень холодная Холодная Теплая Очень теплая Горячая Очень горячая Слабо перегретая Весьма перегретая |
Примечание: воды с температурой от 20 до 100 о С называются термальными.
В нашем случае Т15 о С. Вода холодная.
Жесткость воды имеет большое значение при использовании подземных вод для питьевого водоснабжения, промышленных и хозяйственных целей. Жесткость воды обусловливается содержанием в ней солей кальция и магния. Измеряется в миллимолях (мг-экв/дм 3 ).
Различают общую жесткость (ОЖ), устранимую или временную жесткость (УЖ) и постоянную жесткость (ПЖ).
Общая жесткость обусловлена присутствием в воде гидрокарбонатов, хлоридов и сульфатов кальция и магния и равняется сумме устранимой и постоянной жесткости.
Устранимая жесткость обусловлена присутствием в воде гидрокарбонатов кальция и магния. Такая жесткость получила название карбонатной (КЖ) и может быть устранена при кипячении
Карбонат кальция и магния выпадает в осадок, образуя накипь. При использовании такой воды для промышленных и коммунальных целей происходит отложение карбоната кальция и магния на стенках котлов и трубопроводов, что приводит к выводу их из эксплуатации.
При высоком содержании НСО3 — в воде, превышающем суммарную концентрацию кальция и магния, вся жесткость считается карбонатной.
Постоянная жесткость обусловлена наличием в воде сульфатов и хлоридов кальция и магния и равняется разности между общей и карбонатной жесткостью.
Классификация воды по общей жесткости приводится в таблице 6 (ГОСТ 6055-86).
| Содержание в ммоль | Группа жесткости |
| £ 1,5 >1,5-3,0 >3,0-6,0 >6,0-9,0 >9,0 | Очень мягкая Мягкая Умеренно жесткая Жесткая Очень жесткая |
Подземные воды, жесткость которых превышает 7 ммоль, не могут быть использованы для питьевого и промышленного водоснабжения.
В нашем случае общая жесткость составляет 38,37 ммоль, устранимая (карбонатная) – 3,50 ммоль, постоянная – 34,86 ммоль. Вода очень жесткая, непригодная для питьевого и промышленного водоснабжения.
8) Пригодность для питьевого водоснабжения.
Пригодность воды для питьевого водоснабжения нормируется ГОСТ 6055-86 «Вода питьевая». В рамках сокращенного гидрохимического анализа нормативными являются минерализация, общая жесткость, содержание Cl — и SO 2- 4 , а также величина рН с предельно допустимыми концентрациями, приведенными в таблице 7.
| Наименование показателей | ПДК | Содержание в нашем примере | Степень пригодности |
Минерализация М, мг/дм 3 Общая жесткость ОЖ, ммоль 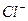 , мг/дм 3 , мг/дм 3 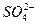 , мг/дм 3 рН , мг/дм 3 рН | 6,5-8,5 | 38,37 5,3 | Не пригодна Не пригодна Не пригодна Не пригодна Не пригодна |
В нашем случае вода по всем компонентам не пригодна для водоснабжения.
9) Пригодность для ирригационных целей.
Пригодность использования подземных вод, в том числе и шахтных, для ирригационных целей в сельском хозяйстве нормируется степенью минерализации воды и расчетным ирригационным коэффициентом. Классификация воды по минерализации, нормирующая степень пригодности для орошения сельскохозяйственных угодий, приведена в таблице 8.
| Минерализация, г/дм 3 | Степень пригодности для орошения |
| £1,7 >1,7-5,0 >5,0 | Пригодна Пригодна условно (возможно засоление) Не пригодна |
В нашем случае минерализация 6,9 г/дм 3 . Вода для орошения не пригодна.
Расчет ирригационного коэффициента выполняется в зависимости от соотношения ионов натрия, хлора и сульфатов в эквивалентной форме в миллимолях.


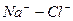
 |
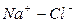

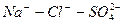
Во втором случае избыточное содержание катионов натрия может быть нейтрализовано содержащимся в воде сульфат-ионом. В третьем случае избыток натрия накапливается в почве в виде поглощенных катионов.
В первых двух случаях вода улучшению не подлежит, в третьем случае воду можно улучшить добавкой гипса. Классификация воды по ирригационному коэффициенту приведена в таблице 9.
| Ирригационный коэффициент | Характеристика воды |
| >18 >6-18 ³1,2-6,0 + — , Кир= 0,58. Вода очень плохая и улучшению не подлежит. 10) Агрессивность подземных вод. Подземные воды в зависимости от состава могут оказывать разрушающее действие на бетоны, цементы и металлы. Оценка агрессивности подземных вод по отношению к бетонам марки W4 и металлам производится на основании таблиц 5-7 и 26 СНиП 2.03.11-85 «Защита строительных конструкций от коррозии» (в скобках указаны номера таблиц согласно СНиП). Дата добавления: 2015-04-18 ; просмотров: 71 ; Нарушение авторских прав источник Любой человек, который учился в школе, с легкостью ответит вам на вопрос о том, на сколько процентов человек состоит из воды. И показатель этот составляет 80%. Питьевая вода является очень важным источником здоровья и хорошего повседневного самочувствия, потому ее качество является более чем важным для человека. Методы очистки сточных вод. По этим причинам имеет огромное значение то, какая химия содержится в воде, которую каждый день потребляет человек. То же самое касается и грунтовых вод, добываемых из загородных участков. При желании или необходимости существует возможность произвести лабораторный химический анализ питьевой воды. Только в случае, если анализ грунтовых вод был произведен в специализированной профессиональной лаборатории, он может иметь наиболее точную степень результатов, которые не подлежат сомнениям. Лаборатория должна быть хорошо оснащенной и обязана использовать современные методы по определению качества воды. Структурные схемы очистки сточных вод от нефтепродуктов. Перед тем как сдавать воду для выполнения необходимого анализа в конкретную лабораторию, необходимо узнать, какой репутацией обладает эта лаборатория, и изучить ценовой вопрос. Стоит собрать как можно более подробную информацию об отзывах о качестве работы лаборатории. Одним из признаков уровня работы лаборатории является предоставление не только информации о составе грунтовых вод, но и о том, какими физическими и химическими свойствами она обладает, о том, какую микрофлору она содержит, об уровне концентрации ионов водорода (уровень рН).
Схема получения анализа воды. Довольно часто грунтовые источники, питающие колодцы, располагаются недостаточно глубоко и больше всех подвергаются различным видам загрязнений, которые возникают в итоге технологического развития человечества. Такими загрязнениями чаще всего являются отходы с предприятий, работающих с химическими веществами и химические загрязнители, попадающие в состав грунтовых вод, расположенных в верхних слоях грунта после использования на угодьях сельского хозяйства. В конечном итоге все это может оказаться в колодцах. Для наиболее верного подбора системы очищения воды, взятой из колодца, нужно учесть и то, что состав биологических и химических элементов может быть разным, в зависимости от конкретного сезона. Чтобы учесть этот фактор, анализ воды из колодца необходимо будет произвести два раза за год (осень и весна, к примеру). Во время выполнения первых двух исследований воды из колодца стоит выполнить эту процедуру по наиболее возможному количеству элементов, загрязняющих источники. Произвести эти исследования необходимо в профессиональной лаборатории. После этого можно приступать к процессу выбора очищающей системы, с оглядкой на результаты исследований. Дальнейший анализ можно выполнять периодически. С этой целью можно купить специализированные наборы, с помощью которых можно выполнять исследование уровня чистоты грунтовых вод, следуя обнаруженным признакам загрязнения. Чтобы собрать необходимое количество воды для того, чтобы можно было выполнить нужные исследования, можно использовать стеклянную бутылку 0,5 л, которую нужно обязательно промыть с помощью проточной воды. Во время процесса промывания бутылки запрещено использовать любые очищающие средства, дабы не загрязнить ими набираемую воду. Наполняться бутылка должна таким образом, чтобы внутри не осталось никакого воздуха. После набирания воды бутылку можно хранить не больше 24 часов, поскольку в ином случае она утратит прежние свойства и окажется неподходящей для выполнения исследований. Для наиболее верного выбора систем, выполняющих функции извлечения грунтовых вод из скважины и ее очищения вы будете вынуждены провести исследования состава воды, содержащейся в скважине. Особенно если скважина является единственным способом снабжать водой ваш дом или хозяйство. Состав воды, находящейся в скважине, может иметь достаточно заметные отличия от состава воды из колодца. Наблюдать это можно по той причине, что в воде из скважины могут встречаться загрязняющие вещества, которые встречаются в глубинных слоях грунта чаще, чем на поверхности. Это могут быть: кадмий, алюминий, марганец, мышьяк. Загрязнение подземных вод. Проводить исследования состава воды из скважины можно во время любого сезона в течение года. Нужно лишь правильно приготовить емкость для забора воды, выполнить забор необходимого количества воды и отнести образец на анализ в течение 24 часов с момента забора. В течение процесса лабораторных исследований обычно определяются следующие параметры:
Выполнение лабораторных исследований на должном профессиональном уровне окажет отличную помощь в том, чтобы узнать, как можно использовать воду и можно ли ее использовать. Кроме того, результаты анализа помогут наиболее удачно подобрать подходящую систему для фильтрования воды. К таким водам на участке загородного дома, как правило, причисляют атмосферные осадки, которые обычно собирают в некоторые емкости, обладающие хорошей вместительностью. Затем эти воды могут быть использованы с целью полива всяческих грядок и огородов. В наше время окружающая среда в некоторых районах подвергается техногенным воздействиям настолько сильно, что даже атмосферные осадки могут иметь достаточно высокий уровень загрязнения. Традиционная схема очистки сточных вод. По этой причине по таким водам тоже должен быть произведен анализ на предмет различных загрязняющих веществ. Если этого не сделать, то существует опасность использования загрязненной воды для полива растущих на огороде овощей, после чего свинец, соли тяжелых металлов и многие другие разновидности химических загрязнителей могут попасть к вам на стол вместе с овощами, впитавшими в себя эти токсины вместе с водой. Исследования сточных вод вполне успешно выполняются в обычных СЭС-лабораториях. После завершения анализа делается вывод о том, пригодна ли вода к использованию, или ее нужно предварительно очищать перед применением. Пробу воды можно делать таким же способом, как это делается при заборе воды из колодца. Бывает такое, что требуются лишь только исследования микробиологического состава воды, которая используется. Данное действие тоже выполняется только в профессиональной лаборатории. В основном данное исследование отличается только методом собирания образца для анализа. С целью забора образцов и сохранения их в надлежащем состоянии до самого момента начала исследования обычно пользуются специальными герметичными пакетами, которые можно купить в лабораториях СЭС. Можно сделать следующий вывод: во многих районах экологическая ситуация оставляет желать лучшего или ухудшается. Данные процессы, несомненно, влияют на качество грунтовых вод. По этой причине перед началом использования колодца или скважины нужно обязательно провести исследования воды, содержащейся в источнике. И поставить фильтрующую систему, если в ней есть необходимость. Далее можно периодически выполнять профилактическую проверку качества питьевой воды из грунтовых вод. Что касается сточных вод, то проверка тоже нужна, особенно если поблизости находятся крупные предприятия, выбрасывающие большое количество загрязнителей через трубы в атмосферу. источник Химический, микробиологический анализы воды из скважин, и центрального водоснабжения, с примером допустимых показателейВода – это источник энергии и жизни человека, поэтому на всех этапах строительства, начиная с изысканий, обязательно проводят анализ воды из скважин, колодцев и водоемов, находящихся непосредственно на территории объекта. Состав воды подвержен постоянному воздействию внешних факторов, ведь не исключено, что ранее около водоема, скважины или колодца располагались промышленные предприятия, захоронения тяжелых металлов или несанкционированная свалка отходов. Определить годность воды к использованию в бытовых условиях может своевременный анализ воды. Исследования помогают установить химический состав и свойства воды и выявить концентрацию всех вредных примесей. Это необходимо для обеспечения любого объекта строительства качественной питьевой водой, а также для расчетов и выбора подходящего очистительного и распределительного оборудования. От состава и свойств воды зависит расчетный срок службы прокладываемых коммуникаций и здоровье людей, использующих ее для питьевых или бытовых нужд. Именно по этой причине одним из основных этапов геоизысканий является обязательное проведение различных анализов воды из скважины, которое назначается застройщиками любых объектов, в том числе и промышленных. При этом стоит учесть, что подобные лабораторные исследования рекомендуется проводить систематически, так как химический состав воды подвержен изменениям под действием внешней среды.
Показатели качества воды определяются:
Результаты проверки указывают на количество определенных веществ в разных единицах измерения. При знании норм можно самостоятельно оценить основные показатели. Если все в норме, то жидкость можно считать чистой и пригодной к использованию. В противном случае нужно проводить дополнительную фильтрацию. Обычно в результатах указывают предельно допустимую концентрацию (ПДК) примесей. Этот показатель говорит, что количество определенного вещества не несет негативного воздействия. ПДК прописываются в нормативных документах. Исследование производят для установления точного химического состава воды, а также для оценки основных свойств. Характер исследования может отличаться в зависимости от поставленных задач. Химический анализ воды подразделяют на общий и специальный. Во время общего анализа воды определяется ее общая характеристика, необходимая для ее классификации, а также для получения информации о содержании отдельных солей и ионов. Данные результаты имеют широкое назначение. Согласно СанПиН 2.1.4.559-96, на сегодняшний день в результате исследования воды обязательно устанавливают концентрацию ионов кальция, магния, натрия, которые наряду с другими составляют основу шестикомпонентного анализа, также позволяющего определить содержание железа и уровень pH. Исследование не включает в себя определение газового состава. Краткое описание основных исследуемых в процессе химического анализа показателей:
Среди специальных анализов подземных вод важное место занимают:
Анализы воды из скважины проводят как в стационарных лабораторных условиях, так и с использованием полевых лабораторных установок непосредственно на объекте строительства. В полевых условиях часто используют исследовательские лаборатории и передвижные конструкции для анализа, разработанные учеными А. А. Резниковым (ПЛАВ), И. Ю. Соколовой и другими. Данный вид оборудования обычно состоит из упакованных смонтированных комплектов оборудования, посуды и реактивов, которые предназначены для исследований объемным, колориметрическим и нефелометрическим методами. Химическая экспертиза воды имеет широкий спектр действия и применяется для:
Для точности результатов рекомендуют соблюдать следующие требования:
К образцу прилагают документацию, содержащую информацию о виде источника (колодец, скважина, природный водоем и т. д.), место пробы, правильную дату и время забора, а также точный юридический адрес источника. Изображение результатов химического анализа Качество воды из скважины и ее состав можно определить несколькими методиками. Каждая из них устанавливает определенный показатель. Химический состав воды из скважины, водоема или колодца обычно изображают в ионной, процент-эквивалентной или эквивалентной форме. Ионная форма позволяет выразить химический состав питьевой воды в виде отдельных ионов, содержащихся в ней. Они выражаются в миллиграммах (мг) или же в граммах (гр), изредка данные могут быть предоставлены как отношение к массе и объему исследуемой жидкости. Сегодня все сертифицированные лаборатории, куда доставляются пробы, предоставляют результаты гидрохимических исследований в ионной форме, которая является основным изображением состава воды. Ионная форма считается основной и используется для дальнейших переходов. Если надо выполнить перевод результатов, изображенных в виде отношения к единице объема, к составу, отнесенному к единице массы, количество отдельных ионов нужно поделить на плотность, а в случае обратного перехода — помножить. Эквивалентная форма изображения результатов и получила значительное распространение. Она дает развернутое представление о свойствах воды, позволяет определить содержание ионов и установить происхождение вод. Форма используется в аналитических целях и позволяет контролировать результаты. Эквивалент иона представляет собой частное от деления ионной массы на валентность иона. В качестве примера можно рассмотреть содержание иона натрия в эквивалентном виде иона: Na+ = 23/1, а эквивалент иона С = 35,5/1, из этого следует вывод, что на 23 единицы массы иона Na+ приходится 35,5 единицы иона, выраженных в эквивалентах. Исходя из этого, нужно отметить, что для перехода от ионной формы к эквивалентному изображению результатов нужно разделить количество иона, выраженное в миллиграммах (мг) или граммах (гр), на величину эквивалента иона. Процент-эквивалентная форма позволяет более наглядно показать ионно-солевой состав, соотношение между ионами, а также определяет черты сходства вод с различной величиной минерализации, что делает данную форму наиболее распространенной. Но изображение содержания солей в составе исследуемых жидкостей только в одной из вышеперечисленных форм не дает возможности установить абсолютное содержание ионов в воде. По этой причине желательно предоставить результаты исследований, изобразив их в эквивалентной и ионной формах. источник Титрованием NaOH с индикатором фенол- фталеином — содержание определяемого компонента в . Титрованием HCl с индикатором фенол- фталеином — содержание определяемого компонента в мг/л. — окисляемость воды в мг/л О . Титрованием НСl с индикатором метилоранжем — количество раствора известной концентрации, израсходованное на титрование взятого объема пробы воды (или добавленное в образцовый при колориметри- ровании), в мл. Титрованием трилона «Б» с индикатором ЕТ-00 — поправочный коэффициент к нормальности этого раствора. Титрованием трилона «Б» с индикатором мурексидом — концентрация стандартного раствора. — объем исследуемой воды, взятой для определения, в мл. Титрованием MgCl с индикатором ЕТ-00 — количество трилона «Б», добавленное в пробу, в мл. Титрованием AgNO в присутствии индикатора K Cr O : I — эмпирическим раствором (1 мл AgNO 1 мг Cl’) и — общее количество KMnO , добавленное в пробу, в мл. — количество KMnO , пошедшее на окисление органических веществ в дистиллированной воде, мл. II — децинор- мальным (1 мл 0,1 AgNO 0,1 мг/эк в Cl’) — количество KMnO , пошедшее на окисление 10 мл раствора H C O , в мл. — количество раствора J , добавленное в пробу, мл. Титрованием KMnO в кислой или щелочной среде — поправочный коэффициент к нормальности раствора J. Титрованием Na S O (иодометрия) — количество раствора Na S O , израсходованное на титрование пробы, в мл. Метод колори- С сульфо- салициловой кислотой — поправочный коэффициент к нормальности раствора Na S O . Окисление Mn до MnO в присутствии катализатора AgNO — количество стандартного раствора, взятого для приготовления образцового раствора, в мл. С молибдено- вокислым аммонием — высота столба жидкости в цилиндре с образцовым раствором. С циркон- ализариновым красителем — высота столба жидкости в цилиндре с исследуемой водой. — вес прокаленного остатка определяемого вещества в мг. С дисульфо- феноловым реактивом — вес чашки с сухим остатком в мг. — вес сухого остатка прибавленного раствора соды в мг. 1000 — коэффициент для пересчета содержания определяемого компонента в 1 литре воды. 2 — коэффициент пересчета в СО (условно считают, что с НСl оттитровывается только 1/2 общего содержания СО ). С отделением Са , Mg , Fe , Al аммиачно- спиртовым раствором 30 — эквивалентный вес иона Са». 61 — эквивалентный вес иона НСО . 20,04 — эквивалентный вес иона Са . Выпариванием при 130 °С с содой 12,16 — эквивалентный вес иона Mg . 35,5 — эквивалентный вес иона Сl’. По разности между общей жесткостью и ионом Са 4,4 — коэффициент пересчета в СО своб. (1 мл 0,1 NaOH соответствует 4,4 мг СО своб.). По разности между содержанием общего и трехвалентного железа 0,17 — коэффициент пересчета в H S (1 мл 0,01 раствора иода, соответствует 0,17 мг H S). 0,08 — титр 0,01 раствора KMnO , выраженный в мг O . 2,4 — коэффициент пересчета в SO (1 мл 0,05 раствора трилона «Б» соответствует 2,4 мг иона SO ). 0,0208 — коэффициент для пересчета мг-л SO в . 0,028 — коэффициент для пересчета мг/л иона Cl’ в . 0,043 — коэффициент для пересчета мг/л (Na+K) в . 0,4114 — коэффициент для пересчета BaSO в SO . 0,3235 — коэффициент для пересчета суммы (Na +К ) на Na . При отборе проб должна быть исключена любая возможность случайного загрязнения воды. Бутыли тщательно моют внутри и снаружи. Резиновые пробки кипятят в 1%-ном растворе соды, затем промывают водой и 1%-ным раствором соляной кислоты, после чего несколько раз ополаскивают дистиллированной водой. Если для отбора применяют стаканы и пробоотборники, они также должны быть тщательно вымыты. Пробки хранят в чистом деревянном плотно закрываемом ящике, что исключает возможность загрязнения. Отбор проб воды является ответственным моментом, определяющим качество исследований и надежность результатов анализа. Перед отбором пробы тщательно вымытые руки, бутыли, стаканы, пробоотборники, пробки два, три раза ополаскивают отбираемой водой. В открытый источник бутыль погружают и она заполняется водой. Если источник мелкий, воду отбирают стаканом, сливая в бутыль воду по стенке. Перед отбором проб из скважин и колодцев откачивают застоявшуюся воду так, чтобы столб воды сменился свежей не менее двух-трех раз. Для отбора проб целесообразно применять пробоотборник конструкции Е.В.Симонова. Между уровнем воды в бутыли и пробкой нужно оставить воздушное пространство объемом 5-10 см . Немедленно после заполнения бутыль закупоривают пробкой. Обтирают бутыль сухим полотенцем и переворачивают вверх дном, следя за тем, чтобы вниз не стекали капли воды. Если пробка остается сухой, можно считать, что герметичность укупорки достигнута. На бутыль наклеивают этикетку, в которой должны быть указаны: назначение анализа, адрес места отбора, наименование водоема, водотока, колодца, номер скважины, глубина и дата отбора, условия погоды, фамилия исполнителя, отобравшего пробу. В зависимости от назначения анализа отбирают следующие количества воды: для целей питьевого водоснабжения 1,5 л, и, кроме того, для определения каждого из неустойчивых компонентов по 0,25 л; для оценки агрессивных и коррозионных свойств 1,0 л и для определения по специальному заданию стабильности и содержания ионов марганца и фтора по 0,5 л. Отобранные пробы воды доставляют в лабораторию с сопроводительными ведомостями, в которых повторено содержание этикеток. С целью определения неустойчивых компонентов отбирают отдельные пробы по 250 мл воды в каждой. Окисляемость, содержание сероводорода, нитратов, нитритов, аммония, железа и стабильность рекомендуется определять на месте взятия пробы, немедленно после отбора. Если этого сделать нельзя, неустойчивые компоненты воды консервируют. Консервируя окисляемость и соединения азота, к 250 мл отдельно взятой пробы воды добавляют 0,5 мл 25%-ного раствора серной кислоты, проверенной на отсутствие аммония. Для консервации сероводорода в бутыль емкостью 250 мл предварительно наливают 6-10 мл 10%-ного раствора ацетата кадмия или 1-2 мл 50%-ного раствора едкого натрия. Для стабилизации железа воду подкисляют соляной кислотой. Дозу раствора кислоты устанавливают, титруя 250 мл исследуемой воды с метилоранжем до появления розового окрашивания. Во вновь отобранную пробу воды добавляют установленную дозу соляной кислоты. Мутные воды после подкисления отстаивают в течение часа и переливают в чистую посуду. Если в дальнейшем при стоянии выпадает осадок гидрата окиси железа, его растворяют подкислением воды. Для определения стабильности в бутыль на 500 мл отбирают пробу воды, в которую всыпают 30 г мраморного порошка для нахождения щелочности в воде, насыщенной углекислым кальцием. Лаборант записывает в рабочий журнал сведения с этикетки на бутыли и отмечает в журнале даты доставки пробы воды в лабораторию, начала и окончания анализа. (Формы рабочих журналов приведены в приложениях NN 5, 6 и 7). Исследуемую воду перед анализом подвергают предварительной обработке в двух случаях: когда она мутна или окрашена. В нефильтрованной воде определяют: прозрачность, содержание сероводорода и железа. Для объемных и колориметрических определений воду фильтруют в том случае, когда прозрачность ее ниже 30 см по шрифту. Для весовых определений воду во всех случаях фильтруют, окрашенные же воды не обесцвечивают. Для колориметрических определений окрашенные воды предварительно обесцвечивают. 1. Фильтрование. Воду фильтруют через беззольный бумажный фильтр, промытый несколько раз дистиллированной, а затем 2-3 раза исследуемой водой. Порциями профильтрованной воды промывают и склянку, в которую воду фильтруют. Профильтрованная вода должна тотчас же поступить в работу. 2. Обесцвечивание. Наиболее распространенным реагентом для обесцвечивания воды является гидрат окиси алюминия, который образуется в воде при прибавлении к ней сернокислого алюминия. Процесс обесцвечивания идет наиболее эффективно при рН=5. Этот способ обесцвечивания дает хорошие результаты при определении: аммонийных солей, нитритов (при цветности воды до 1000°), нитратов (до 300°) и хлоридов. Реактивы. 1. Раствор сульфата алюминия (13,9 г химически чистого Al (SO ) ·18H O растворяют в 100 мл дистиллированной воды). 2. Раствор едкого калия (7 г химически чистого KOH растворяют в 100 мл дистиллированной воды). Оба раствора практически эквивалентны и их нормальность примерно равна 1,25. Реактивы и дистиллированная вода не должны содержать соединений азота и хлоридов. Рекомендуется проверять эквивалентность соотношений обоих растворов. Для этого на 100 мл дистиллированной воды вносят 1 мл раствора едкого калия, 3 капли раствора индикатора метилрота (0,5%), а затем из градуированной пипетки вносят раствор сернокислого алюминия до ясного перехода желтой окраски в малиново-красную. Число мл израсходованного раствора сернокислого алюминия выражает величину поправочного коэффициента ( ) данного раствора щелочи. В зависимости от степени мутности, окрашенности и щелочности воды на 200-400 мл исследуемой пробы, налитой в мерный цилиндр, вносят при перемешивании 0,5-1-2-4 мл раствора сернокислого алюминия. Последний с бикарбонатами дает гидроокись алюминия: Al (SO ) +3Ca(HCO ) =2Al(OH) +3CaSO +6CO . Полное обесцвечивание происходит при конечной реакции среды около pH=5, что получается, если количество внесенного раствора сернокислого алюминия численно равно величине щелочности в мг-экв в данном (200-400 мл) объеме воды. Так, если щелочность исследуемой воды соответствует 2,5 мг-экв в 1 л, то щелочность в 400 мл равна 1 мг-экв, и на этот объем воды необходимо внести 1 мл раствора сернокислого алюминия. Если же величина щелочности в данном объеме воды больше, то соответственно до равных числовых значений добавляют количество раствора сернокислого алюминия или несколько понижают щелочность воды путем добавки титрованного раствора чистой серной кислоты. В тех случаях, когда требуется внести раствор сернокислого алюминия в количестве, превышающем щелочность в данном объеме воды, необходимо дополнительно внести раствор едкого калия, количество которого рассчитывают по формуле: где — необходимое количество мл раствора KOH, — количество мл раствора Al (SO ) , добавлено в пробу, — щелочность воды в мг-экв в данном объеме воды, — поправочный коэффициент к нормальности раствора Al (SO ) . Пример: На 400 мл исследуемой воды со щелочностью 0,8 , внесен 1 мл раствора сернокислого алюминия, здесь требуется добавить раствор едкого калия в количестве, равном Реакция среды контролируется по величине рН. Для измерения температуры воды применяют ртутный термометр со стоградусной шкалой и делениями на 0,1 градуса, опуская его непосредственно в водоем или в пробу воды в бутыли. При этом нужно соблюдать меры предосторожности против нагревания воды лучами солнца, рукой или другими источниками тепла. Термометр выдерживают в воде не менее 5 минут и измеряют температуру с точностью до 0,1 градуса. Извлеченный из воды термометр протирают сухим полотенцем и измеряют температуру воздуха в тени, не на ветру. Запахи делятся на две группы: I группа — запахи естественного происхождения (от живущих или отмерших в воде организмов, от влияния берегов, окружающих почв, дна и т.д.); II группа — искусственного происхождения (от промышленных сточных вод, от обработки воды реагентами на водопроводе). Характер запаха определяют при температуре воды 15-20°. Воду наливают в широкогорлую колбу емкостью 150-200 мл на ее объема, накрывают часовым стеклом и встряхивают вращательными движениями, после чего колбу открывают и втягивают носом воздух. Запахи первой группы классифицируют по таблице 3. Запах мокрой щепы, древесной коры Прелый, свежевспаханной земли Запахи естественного происхождения, не похожие на предыдущие Запахи второй группы характеризуют по соответствующим веществам: фенольный, хлорфенольный, камфорный, нефтяной, хлорный. Интенсивность запаха выражают в баллах при температуре 15-20 °С и при нагревании до температуры около 60 °С. При этом поступают так же, как при определении характера запаха. Оценка в баллах дается по таблице 4. Запах совсем не ощущается. Запах, обычно не замечаемый, обнаруживается опытным исследователем. Запах, обнаруживаемый потребителем, если на запах обратить его внимание. Запах, легко замечаемый и могущий вызвать неодобрительные отзывы о воде. Запах, обращающий на себя внимание и могущий заставить воздержаться от питья. Запах, настолько сильный, что вода непригодна для питья. Мутность зависит от наличия в воде взвешенных веществ и коллоидных примесей. В зависимости от степени прозрачности воду условно подразделяют на: 1) прозрачную, 2) слабо опалесцирующую, 3) опалесцирующую, 4) слегка мутную, 5) мутную и 6) сильно мутную. Для количественного определения прозрачности применяют два метода: «по кресту» и по Снеллену. Прозрачность «по кресту» определяют при регулярном контроле работы очистных сооружений и качества воды в водопроводной сети. В лаборатории прозрачность воды устанавливают по Снеллену путем чтения стандартного шрифта через столб воды, налитой в цилиндр диаметром 2,5-2,0 см с плоским дном, градуированный по высоте на 30 см, начиная от дна. Цилиндр неподвижно укрепляют в штатив так, чтобы шрифт находился на расстоянии 4 см от дна цилиндра. Перед анализом воду хорошо взбалтывают, тотчас же переливают в цилиндр и, быстро сливая воду из боковой трубки, отмечают высоту столба, при которой чтение шрифта становится возможным. Прозрачность выражают в сантиметрах, с точностью до 0,5 см. Работать нужно в хорошо освещенной комнате, но не на прямом солнечном свету. Образцы стандартного шрифта приложены к ГОСТу 3351-46*. Причиной окраски природных вод обычно являются вещества, извлекаемые водой из торфа, гумуса, болотной почвы, отмерших растений и т.п. Для качественного определения цветности 100 мл воды в колбе из бесцветного стекла просматривают на белом фоне. По окраске воду характеризуют как: бесцветную, светло-желтую, желтоватую и интенсивно-желтую. Количественно цветность воды определяют путем сравнения с растворами, имитирующими цветность воды — шкалой цветности. Для приготовления шкалы цветности используют основные растворы: платиново-кобальтовый (раствор N 1) или раствор двуххромовокислого калия и сернокислого кобальта (раствор N 2). Приготовление основных растворов и шкалы цветности Приготовление раствора N 1. Отвешивают на аналитических весах 1,245 г хлороплатината калия (KPtCl ), что соответствует 500 мг платины и 1,01 г кристаллического хлористого кобальта (CoCl ·6H O). Навески помещают в литровую колбу и растворяют, приливая немного дистиллированной воды, затем добавляют 100 мл концентрированной соляной кислоты и колбу до метки доливают дистиллированной водой. Цветность такого раствора равна 500°. Приготовление раствора N 2. 0,0875 г двуххромовокислого калия растворяют в чистой посуде в небольшом количестве дистиллированной воды. В отдельной посуде растворяют 2,0 г сернокислого кобальта. Оба раствора смешивают в литровой колбе и прибавляют 1 мл химически чистой серной кислоты (удельного веса 1,84). Колбу доливают до метки дистиллированной водой. Цветность этого раствора также равна 500°. Растворы N 1 и N 2 хранят в темном месте. Они пригодны для приготовления шкалы цветности в течение одного года. Шкалу цветности готовят из основных растворов N 1 и N 2, в цилиндрах Несслера одинакового диаметра и высоты, емкостью 100 мл, изготовленных из бесцветного стекла. В цилиндры приливают различные количества раствора N 1 и раствора N 2. Объем растворов доводят до 100 мл дистиллированной водой. Шкалу цветности из основного платино-кобальтового раствора N 1 готовят в соответствии с таблицей 5. Количество основного раствора в мл Кол-во дистиллированной воды в мл Для приготовления шкалы цветности из основного раствора N 2 готовят вспомогательный раствор. 1 мл химически чистой серной кислоты (удельного веса 1,84) доводят дистиллированной водой до 1 литра. Затем смешением основного раствора и вспомогательного в соотношениях, указанных в таблице 6, получают шкалу цветности. Количество основного раствора в мл Кол-во вспомогательного раствора в мл Цилиндры шкалы закрывают пробками и хранят в темном месте. Через 2-3 месяца шкалу из основных растворов приготовляют заново. Количественное определение цветности. Мутные воды прозрачностью ниже 30 см по Снеллену перед определением цветности фильтруют. В цилиндр, однотипный с теми, в которых приготовлена шкала цветности, наливают 100 мл исследуемой воды и сравнивают со шкалой цветности. Цилиндры просматривают сверху на белом фоне до тех пор, пока окраска исследуемой воды не будет близка или тождественна окраске раствора в одном из цилиндров шкалы цветности. Цветность от 1° до 50° выражают с точностью до 1°, Если исследуемая вода имеет цветность выше 80°, то для анализа берут меньший объем воды и разбавляют дистиллированной водой до объема 100 мл. Цветность в этом случае находят умножением результата на кратность разбавления. Взятую из открытого водоема воду прозрачностью 20 см и менее по Снеллену хорошо взбалтывают и наливают в мерный цилиндр до высоты 30 см. Воде дают постоять в течение часа в защищенном от солнечных лучей и нагревания месте. Воды прозрачностью по Снеллену 20 см и менее, пробы которых отобраны из подземных источников, отстаивают в течение 24 часов. Осветление описывают качественно: незначительное, слабое, сильное, вода прозрачна, а выпавший осадок характеризуют по количеству: нет, незначительный, большой. Указывают толщину слоя большого осадка в мм или в отношении общего объема пробы воды. По качеству осадки подразделяют на кристаллические, аморфные, хлопьевидные, илистые, песчаные. Отмечают цвет осадка — бесцветный, сероватый, бурый, черный. Содержание в воде взвешенных веществ определяют весовым методом. Для отделения взвешенных веществ воду фильтруют через бумажные фильтры, тигли Гуча или центрифугируют. Объем воды, необходимый для анализа, зависит от предполагаемого содержания в ней взвешенных веществ и может быть принят по таблице 7. Предполагаемое содержание взвешенных веществ в мг/л 1. Определение взвешенных веществ фильтрованием. Плотные бумажные обеззоленные фильтры помещают по одному в бюксы и просушивают в сушильном шкафу при температуре 105° до постоянного веса. Бюксы с фильтрами взвешивают на аналитических весах. Пробу воды тщательно взбалтывают и быстро, не давая осесть взвеси, отбирают в мерную колбу необходимое для анализа количество воды и пропускают через подготовленные бумажные фильтры. Если фильтрат мутный, его следует пропустить вторично через тот же фильтр. Переносят фильтры вместе с находящимися в них взвешенными веществами в бюксы, в которых взвешивались фильтры, и высушивают в сушильном шкафу до постоянного веса при температуре 105 °С. Содержание взвешенных веществ в анализируемой воде в мг/л рассчитывают по формуле: где — содержание взвешенных веществ в мг/л; — вес бюкса после просушивания с бумажным фильтром и взвешенными веществами в г; — вес бюкса с бумажным фильтром без осадка в г; — коэффициент приведения к объему в 1 л; — объем воды в мл, взятый для анализа; 1000 — множитель для пересчета г в мг. 2. Метод центрифугирования. В высушенную при 105 °С до постоянного веса пробирку наливают воду и центрифугируют в центрифуге марки СМ-3 в течение 15 минут. Затем жидкость над осадком осторожно отбирают резиновой грушей, наливают новую порцию исследуемой воды в ту же пробирку и вновь центрифугируют. Эти операции повторяют до тех пор, пока весь взятый для определения объем воды не будет процентрифугирован. Затем стенки пробирки омывают дистиллированной водой, взмучивая осадок, и вновь центрифугируют. После сливания воды над осадком промывание повторяют вторично, после чего пробирку с осадком высушивают до постоянного веса в сушильном шкафу при температуре 105°. Содержание взвешенных веществ рассчитывают по той же формуле (пункт 1). 3. Определение потери при прокаливании взвешенных веществ. Фильтр со взвешенными веществами помещают в предварительно прокаленный и взвешенный тигель. Тигель с осадком прокаливают в электрическом муфеле при 800° в течение 30 минут до достоянного веса, охлаждают и взвешивают. Разница в весе между взвешенными веществами и прокаленными, приведенная к 1 литру, равна потере при прокаливании. Воды, содержащие сероводород, корродируют водопроводные трубы, котельный металл и железобетонные сооружения. Питьевая вода не должка содержать даже следов сероводорода, так как уже малейшие его концентрации сообщают ей неприятный вкус и запах. Реактивы. 1. Раствор уксуснокислого кадмия 10%; 2. соляная кислота концентрации 1:1; 3. раствор иода 0,01 ; 4. раствор гипосульфита натрия 0,01 ; 5. раствор свежеприготовленного крахмала 0,5%; 6. свинцовая бумага. Качественная проба. Присутствие сероводорода устанавливают по свойственному этому газу запаху тухлых яиц или при помощи бумаги, пропитанной раствором уксуснокислого свинца. Смоченная дистиллированной водой такая бумага чернеет, если ее держать над водой, содержащей сероводород, вследствие образования сернистого свинца. Количественное определение. В склянку на 250 мл с притертой пробкой наливают 6-10 мл уксуснокислого кадмия и осторожно наполняют исследуемой водой почти доверху. Закрыв склянку пробкой, осторожно перемешивают ее содержимое. Через 5 часов (или после доставки пробы в стационарную лабораторию) осадок сульфида кадмия отфильтровывают и тщательно промывают горячей водой. Фильтрат с осадком помещают в ту склянку, где производилось осаждение, приливают в нее 20 мл раствора иода, подкисляют 5 мл соляной кислоты, фильтр измельчают стеклянной палочкой и избыток иода оттитровывают раствором гипосульфита натрия до слабо-желтого окрашивания. Затем добавляет 1 мл свежеприготовленного раствора крахмала и продолжают титрование до обесцвечивания раствора. Определение содержания нитратов основано на том, что они под действием дисульфофеноловой кислоты переходят в нитропроизводные фенола, которые дают со щелочами соединения, окрашивающие раствор в желтый цвет. Реактивы. 1. Дисульфофеноловый реактив; 2. раствор аммиака 10%; 3. основной стандартный раствор азотнокислого калия, 1 мл которого содержат 0,1 мг нитратов; 4. раствор сернокислого серебра, 1 мл которого соответствует 1 мг хлора. Качественная проба с приближенной количественной оценкой. В пробирку, диаметром 14 мм, из бесцветного стекла наливают по стенке 1 мл исследуемой воды и 1 мл дисульфофеноловой кислоты. Содержимое пробирки перемешивают и через 20 минут по интенсивности окраски устанавливают приближенное содержание нитратов по таблице 8. Окраска при наблюдении сбоку Содержание азота нитратов в мг/л Уловима только при сравнении с контролем Количественное определение. Цветные и мутные воды перед анализом обесцвечивают и фильтруют. Для определения берут такой объем исследуемой воды, содержание азота в котором находится в пределах 0,02-0,1 мг. Воду отбирают пипеткой, помещают в фарфоровую чашечку, добавляют раствор сернокислого серебра, в количестве, эквивалентном содержанию хлоридов в данном объеме воды, и упаривают досуха. Если вода предварительно подвергалась коагулированию и имеет рН около 5,0, пробу перед выпариванием подщелачивают, добавив к ней 0,1 раствора щелочи из расчета 2 мл на 100 мл исследуемой воды. К охлажденному сухому остатку добавляют 1 мл дисульфофенолового реактива и тотчас же тщательно растирают стеклянной палочкой до полного смешения с высушенным остатком. Через 10 минут в чашку добавляют 10 мл дистиллированной воды, перемешивают и вносят 10 мл аммиака (раствор должен после этого иметь отчетливый запах аммиака). В присутствии нитратов появляется желтое окрашивание. Раствор переносят в мерную колбу и доводят дистиллированной водой до метки 100 мл. 3атем готовят 2-3 образцовых раствора, исходя из ожидаемого содержания нитратов. При этом рабочий стандартный раствор (0,2-1,0 мл) выпаривают в фарфоровых чашечках, не допуская прокаливания, обрабатывают, как указано выше, и доводят объем раствора дистиллированной водой до 100 мл. Колориметрируют в цилиндрах Генера. Сливая воду через кран из того или другого цилиндра, находят ту высоту столба жидкостей, при котором окраска в обоих цилиндрах при рассмотрении сверху на белом фоне становится одинаковой. В присутствии хлоридов получают уменьшенное количество нитратов. Хлориды связывают добавкой сернокислого серебра. Выпавший осадок солянокислого серебра отфильтровывают. Определение содержания нитритов основано на образовании азокрасок при взаимодействии в кислой среде нитрит-ионов и ароматических аминов (реактив Грисса). Реактив Грисса с нитритами дает окраску от розовой до ярко-красной. Реактивы. 1. Реактив Грисса; 2. стандартный раствор азотистокислого натрия (1 мл раствора содержит 1 мг NO ); 3. рабочий раствор азотистокислого натрия (1 мл раствора содержит 0,002 мг нитрит-иона). Качественная проба. В пробирку диаметром 13-14 мм наливают 10 мл исследуемой воды, прибавляют 0,1-0,2 г реактива Грисса и нагревают в течение 5 минут при 70-80 °С. Содержание нитритов приближенно находят по таблице 9. Окрашивание при рассмотрении сбоку Окрашивание при рассмотрении сверху вниз Содержание азота нитритов в мг/л Количественное определение. Мутные и цветные воды предварительно обесцвечивают и фильтруют. Берут такой объем исследуемой воды, концентрация азота в котором находится в пределах 0,01-0,004 мг. Взятый объем воды помещают в цилиндр Генера и объем доводят до 100 мл дистиллированной водой. Затем готовят 2-3 образцовых раствора в зависимости от предполагаемого содержания нитритов, доводя взятый объем стандартного раствора до 100 мл дистиллированной водой. Перемешивают и оставляют стоять 30 минут. Нагревание раствора на водяной бане до 50-60 °С ускоряет развитие окраски. Сравнивают окраски растворов в цилиндрах Генера, рассматривая на белом фоне сверху. Сливая воду из цилиндров, находят такую высоту столба жидкости, при которой окраски в обоих цилиндрах одинаковы. Северные и глубоководные артезианские воды содержат минеральный аммоний, который не обладает вредными для здоровья человека свойствами. Присутствие аммония в поверхностных и верховодных источниках может указывать на возможное загрязнение воды, что имеет большое значение для оценки питьевых качеств воды с санитарной точки зрения. Содержание аммонийных солей определяют колориметрически с реактивом Несслера, который с NH дает желтое окрашивание. Подготовка пробы воды к анализу. На точность получаемых результатов оказывает влияние: мутность, цветность, жесткость, содержание железа, сульфатов и свободной углекислоты. Если вода обладает цветностью более 30°, ее обесцвечивают; мутную воду отфильтровывают или обрабатывают коагулянтом. Если образовавшаяся при добавлении реактива Несслера муть не исчезает при подкислении раствора серной кислотой в концентрации 1:3, то в воде имеются сульфиды, которые необходимо удалить. Для этого на каждые 100 мл исследуемой воды добавляют 10 капель 30% раствора уксуснокислого цинка, перемешивают, отстаивают в цилиндре в течение 2-х часов и из отстоявшейся жидкости отбирают пробу для определения. При жесткости более 4 воду умягчают, прибавляя на 100 мл 2 мл раствора едкого натрия и кальцинированной соды. Раствор перемешивают и отстаивают в течение 2-х часов. Реактивы. 1. Реактив Несслера; 2. сегнетова соль; 3. стандартный раствор хлористого аммония, 1 мл которого содержит 0,05 мг аммонийного азота; 4. безаммиачная дистиллированная вода; 5. раствор уксуснокислого цинка 30%; 6. раствор едкого натрия и кальцинированной соды (см. приложение N 1 — приготовление специальных реактивов, буферных растворов и индикаторов). Качественная проба. В пробирку диаметром 13-14 мм отбирают 10 мл исследуемой воды, прибавляют 0,2-0,3 г сегнетовой соли, а затем 0,2 мл реактива Несслера. По развившейся желтой окраске через 10 минут судят о приближенном содержании аммония по таблице 10. Окрашивание при рассматривании сверху вниз Окрашивание при рассматривании сбоку Интенсивно-бурое, раствор мутный Количественное определение. Берут такой объем воды, концентрация аммония в котором находится в пределах 0,03-0,07 мг, и доводят до 100 мл дистиллированной безаммиачной водой. Затем готовят 2-3 образцовых раствора согласно ожидаемой концентрации аммония, разбавляя взятый объем рабочего стандартного раствора до 100 мл безаммиачной водой. Исследуемую воду и образцовые растворы переносят в цилиндры Генера, добавляют по 0,2 г сегнетовой соли и по 2 мл реактива Несслера. После добавления каждого реактива растворы перемешивают. Окраски сравнивают через 10 минут (см. § 2 настоящей главы). При содержании аммония более 5 мг/л анализируемую воду предварительно разбавляют. В сильно загрязненных водах или в водах с солесодержанием свыше 3000 мг/л содержание аммония определяют с отгонкой. Для этого 300 мл анализируемой воды вливают в колбу с притертой стеклянной пробкой, через которую пропущена трубка дефлегматора, соединенного с холодильником. В колбу вводят 10 мл фосфатной буферной смеси (14,3 г одноосновного фосфата калия KH PO и 90,15 двуосновного фосфата калия — K HPO ·3H O) помещают в мерную литровую колбу, растворяют в безаммиачной воде и доводят объем раствора до метки 1 литр. Содержимое колбы кипятят до тех пор, пока от взятого объема не останется 100 мл. В отгоне определяют содержание аммония и пересчитывают на 1 литр, учитывая взятый для отгона объем воды. Почти все воды содержат железо. Значительные количества его портят вкус питьевой воды. Соли железа образуют нерастворимые осадки на стенках водопроводных труб и котлов, кольматируют дренажи и водозаборные фильтры. Все это вызывает необходимость точного учета содержания железа для обезжелезивания воды в необходимых случаях. 1. Сульфосалициловый метод. Наиболее точным считают колориметрический метод с сульфосалициловой кислотой. Он основан на способности сульфосалициловой кислоты или ее натриевой соли давать с ионами железа окрашенные комплексные соединения. В слабокислой среде сульфосалициловая кислота реагирует только с ионами трехвалентного железа с образованием комплексов, окрашивающих раствор в красный цвет. В слабощелочной среде она реагирует с солями как трехвалентного, так и двухвалентного железа с образованием комплексов, окрашивающих раствор в желтый цвет. Реактивы. 1. Водный раствор сульфосалициловой кислоты 10%; 2. раствор соляной кислоты (см. приложение N 1. Приготовление специальных растворов); 3. раствор аммиака 10%; 4. стандартный раствор железоаммонийных квасцов [FeNH (SO ) ·12H O], 1 мл которого содержит 0,01 мг железа. Определение содержания общего железа. Если концентрация железа не превышает 1,0 мг/л, для анализа берут 10 мл исследуемой воды, содержание железа в которых не превышает 0,01 мг. Воду с большим содержанием железа разбавляют так, чтобы в 10 мл полученного раствора содержание железа было не выше 0,01 мг. Затем прибавляют по 5 мл растворов сульфосалициловой кислоты и аммиака и перемешивают. В таких же цилиндрах готовят шкалу стандартных растворов, наливая из микробюретки 0,1; 0,2 и т.д. до 1,0 мл стандартного раствора соли железа, доводят объем жидкости в цилиндрах до 10 мл дистиллированной водой и добавляют те же реактивы, какие были прибавлены в исследуемую воду. Через 10 минут после приготовления растворов окраски сравнивают, просматривая цилиндры на белом фоне сверху. Определение содержания трехвалентного железа. Методики определения содержания трехвалентного и общего железа аналогичны за исключением того, что в исследуемую воду и во все цилиндры шкалы стандартов вместо раствора аммиака приливают по 0,1 мл раствора соляной кислоты. Раствор окрашивается в красный цвет. После 10-минутного стояния пробу колориметрируют. Содержание Fe рассчитывают по той же формуле, что и для общего железа (см. таблицу 2). Определение содержания двухвалентного железа. Концентрацию двухвалентного железа вычисляют по разности: . 2. Родановый метод. При отсутствии сульфосалициловой кислоты или сульфосалицилового натрия содержание железа определяют колориметрически с роданистым аммонием. Родановый метод основан на взаимодействии в сильнокислой среде окисного железа и родана с образованием комплекса, окрашивающего раствор в красный цвет. Реактивы. 1. Стандартный раствор железоаммонийных квасцов, 1 мл которого содержит 0,01 мг железа; 2. раствор роданистого аммония или калия (NH SCN) 50%; 3. персульфат аммония в кристаллах [(NH ) S O ]; 4. соляная кислота удельного веса 1,19, свободная от железа. Определение содержания общего железа. В мерную колбу на 100 мл берут такой объем исследуемой воды, содержание железа в котором находится в пределах 0,05-0,2 мг. Объем раствора доводят до 100 мл дистиллированной водой. Затем добавляют 2 мл соляной кислоты и несколько кристаллов персульфата аммония. Содержимое колбы перемешивают и одновременно готовят 2-3 образцовых раствора. В мерные колбы вносят требуемое количество мл стандартного раствора и объемы доводят дистиллированной водой до метки «100», добавляют 2 мл кислоты HCl, несколько кристаллов персульфата и перемешивают. Одновременно в колбы (с исследуемой водой и стандартными растворами) вносят по 2 мл роданистого аммония и, перемешав, сравнивают окраски в цилиндрах Генера. Сливая раствор из цилиндра с более интенсивной окраской, находят такую высоту столба жидкости, при которой интенсивность окрасок в обоих цилиндрах одинакова. Определение содержания трехвалентного железа. Анализ выполняют так же как и для общего железа, за исключением того, что в исследуемую воду и стандартные образцы не добавляют персульфат аммония. Сравнивать полученные окраски необходимо немедленно, так как интенсивность их быстро падает. Концентрацию окисного железа рассчитывают по формуле расчета общего железа (см. таблицу 2). Определение содержания двухвалентного железа. Содержание закисного железа определяют по разности: 1. Условия определения. Окисляемость марганцевокислым калием является условным показателем, характеризующим содержание в воде восстановителей (окисляющихся веществ). Ее выражают в мг/л кислорода, пошедшего на окисление. Определению окисляемости в кислой среде мешают хлориды при концентрации более 300 мг/л, т.к. образующийся хлористый марганец обесцвечивает титруемую пробу. При высоком содержании хлоридов анализ выполняют в щелочной среде. Реактивы. 1. Раствор марганцевокислого калия 0,01 ; 2. раствор щавелевой кислоты 0,01 ; 3. раствор серной кислоты в концентрации 1:3; 4. раствор гидрата окиси калия или натрия 50%. 2. Определение в кислой среде. В коническую плоскодонную колбу объемом 250 мл отбирают пипеткой 100 мл исследуемой воды. Добавляют в нее 5 мл разбавленной серной кислоты, 3-4 капилляра (для равномерного кипения), точно 10 мл раствора марганцевокислого калия. Кипятят 10 минут от начала кипения, а затем добавляют точно 10 мл раствора щавелевой кислоты и обесцветившийся раствор титруют из бюретки по каплям раствором марганцевокислого калия до устойчивого слабо-розового оттенка. Если после кипячения вода обесцвечивается или буреет, то определение повторяют, добавив в повторную пробу 10-30 мл раствора марганцевокислого калия или разбавив исследуемую воду в 2-3 раза. Для установления титра марганцевокислого калия в оттитрованную до слабо-розового цвета и еще горячую жидкость прибавляют 10 мл 0,01 раствора щавелевой кислоты и оттитровывают тотчас же раствором марганцевокислого калия до слабо-розовой окраски. Находят поправку » «. где — поправочный коэффициент нормальности, — количество KMnO , пошедшее на титрование, в мл. 3. Определение окисляемости в щелочной среде. К 100 мл исследуемой воды прибавляют 0,5 мл раствора щелочи, 10 мл раствора марганцевокислого калия и кипятят ровно 10 минут от начала кипения. Охладив колбу до 50-60 °С, приливают 5 мл серной кислоты и 10 мл раствора щавелевой кислоты. После обесцвечивания титруют марганцевокислым калием до появления устойчивого розового окрашивания, не исчезающего в течение 1 минуты. Стабильность характеризует свойство воды не выделять и не растворять осадок карбоната кальция. Оно зависит от содержания в воде свободной углекислоты. На месте отбора пробы определяют общую щелочность исследуемой воды (§ 10 настоящей главы). Пробу с мраморной крошкой, отобранную для определения щелочности воды, насыщенной углекислым кальцием (гл.II, § 2), встряхивают в течение часа на шуттель-машине. После часового отстаивания воду фильтруют и в 100 г фильтрата определяют щелочность воды, насыщенной углекислым кальцием, в ( ). Стабильность рассчитывают по формуле Вода считается стабильной, если величина стабильности равна единице. К 100 мл исследуемой воды добавляют 0,2-0,3 г сегнетовой соли (она препятствует осаждению гидроокисей металлов), 3 капли 1% раствора фенолфталеина и титруют 0,1 раствором едкого натрия до слабо-розового окрашивания, сохраняющегося в течение 3-х минут. Окрашенные воды разбавляют для снижения интенсивности окраски. Воды по своим свойствам могут быть щелочные, кислые и нейтральные. Количественно эти свойства характеризуются концентрацией водородных ионов в воде и обозначаются символом рН. При рН При рН=6,5-7,5 — нейтральная. При рН=7,5-8,5 — слабощелочная. При рН>8,5 — сильнощелочная. Концентрация водородных ионов — важнейшая характеристика воды. Коррозионные свойства и питьевые качества воды во многом определяются величиной рН, зависящей от содержания в воде свободных кислот и общей концентрации солей. Экспериментально рН устанавливают колориметрическим и электрометрическим (потенциометрическим) методами. 1. Колориметрический метод с универсальным индикатором. Колориметрический метод основан на свойстве кислотно-основных индикаторов менять свою окраску в зависимости от концентрации водородных ионов в растворе. Наиболее быстрым и простым является предложенный Н.И.Алямовским метод определения рН с универсальным индикатором. В пробирку наливают воду до метки 5 мл, прибавляют 0,1 мл универсального индикатора. Перемешивают раствор легким встряхиванием и определяют рН, сразу сравнивая на белом фоне при рассмотрении сверху окраску воды в пробирке со стандартной цветной шкалой на стекле, составленной для рН в интервалах от 4,0 до 8,2. Отмечают то значение рН шкалы, с окраской которого совпала окраска раствора в пробирке. Если раствор в пробирке окажется более ярким, чем крайний зеленый эталон шкалы, записывают значение рН>8,2, если более ярким, чем крайний красный эталон, записывают значение рH 2. Потенциометрический метод. Метод наиболее точен и применяется для мутных и окрашенных вод, буферных растворов, служащих для колориметрических определений pH, а также природных и сточных вод со значительными колебаниями значений pH. В некоторых приборах измерения основаны на компенсации электродвижущей силы, возникающей на электродах, груженных в исследуемую воду. Для массовых анализов более удобны приборы, у которых на шкалу гальванометра нанесены значения рН, определяемые по отклонению стрелки гальванометра. Наиболее распространены в последнее время потенциометры марок ППМ-03, ЛПУ-0,1 и «Агрохимик». 1. Виды щелочности. Общая щелочность природных вод обусловлена содержанием бикарбонатов, карбонатов и гидратов кальция, магния и щелочных металлов. Количественно щелочность равна суммарному содержанию в воде ионов СО , НСО и ОН’. Если в воде нет карбонатных и гидратных ионов, то общая щелочность равна содержанию в воде иона НСО . Реактивы. 1. Растворы: HCl 0,1 ; 2. фенолфталеина 1%-ный; 3. метилоранжа 0,1%-ный. 2. Определение содержания карбонатов (СО ). К 100 мл исследуемой воды добавляют 3-5 капель 1% раствора фенолфталеина. Если вода остается бесцветной, в ней отсутствует карбонатный ион, а если она окрашивается в розовый цвет, ее при постоянном помешивании титруют раствором соляной кислоты до обесцвечивания. 3. Определение содержания бикарбонатов (HCO ). Если в исследуемой воде есть карбонат-ион, то содержание иона HCO устанавливают в пробе после определения содержания CO . В остальных случаях к 100 мл исследуемой воды добавляют 3 капли раствора метилового оранжевого и титруют раствором соляной кислоты до перехода желтой окраски в оранжевую. 4. Определение содержание карбонатов, бикарбонатов и гидратов при совместном их присутствии. При совместном присутствии ионов CO , НСО и ОН’ на основании результатов титрования рассчитывают содержание этих ионов в по таблице 11. Результаты титрования в мл 0,1 раствором HCl Содержание в анализируемой воде, ионов источник |
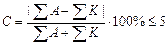

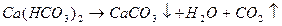
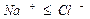
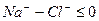
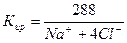
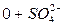
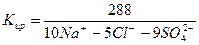
 Емкости, используемые для анализа воды
Емкости, используемые для анализа воды Вода в процессе визуального исследования
Вода в процессе визуального исследования Чистая водопроводная вода
Чистая водопроводная вода Вода с избыточным содержанием железа и меди
Вода с избыточным содержанием железа и меди