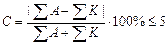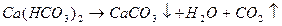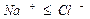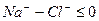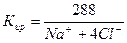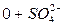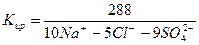Основными задачами химического анализа подземных вод в практике гидрогеологических исследований являются:
- изучение закономерностей формирования и распространения подземных вод различного состава;
- оценка состава и свойств подземных вод для питьевого, технического, сельскохозяйственного, лечебного и других видов исследования;
- исследования подземных вод как критерии при поисках месторождений полезных ископаемых — нефти, газа, солей, различных руд;
- оценка подземных вод как химического сырья для получения йода, брома, бора и других элементов.
Существует четыре типа химических анализов подземных вод: полевой, сокращенный, полный и специальный.
Полевой анализ наиболее прост, он применяется для предварительной характеристики подземных вод района. Его проводят в полевых условиях в походных гидрохимических лабораториях, часто упрощенными методами. При полевом анализе определяют: физические свойства воды, ее pH, наличие Сl — , SO 2- 4 , NO — 3, HCO — 3, СО3 2- , общую жесткость, присутствие Са 2+ , Fe 2+ , Fe 3+ , NH + 4 , N0 — 2, С02своб; вычисляют: Na + + К + , карбонатную жесткость, Mg 2+ и общую минерализацию.
Сокращенный анализ . Этот анализ производят более точными методами в стационарных лабораториях. При сокращенном анализе определяют: физические свойства воды, величину pH, содержание ионов и компонентов (Сl — , SO 2- 4 — , NO — 3, HCO — 3, СО3 2- , Na + , К + , Ca 2+ , Mg 2+ , Fe 2+ , Fe 3+ , NH + 4 , N0 — 2, свободную и агрессивную углекислоту С02, Si02, окисляемость, сухой остаток, жесткость общую, карбонатную и некарбонатную.
Полный анализ применяется для подробной характеристики химического состава подземных вод. Он производится наиболее точными методами в стационарных лабораториях. Анализ позволяет произвести контроль определений как по сухому остатку, так и по суммам мг-экв катионов и анионов. При полном анализе определяют: физические свойства воды, ее pH, наличие Сl — , SO 2- 4 — , NO — 3, HCO — 3, СО3 2- , Na + , К + , Ca 2+ , Mg 2+ , Fe 2+ , Fe 3+ , NH + 4 , N0 — 2, С02 своб и C0 2arpec, Si 0 2, окисляемость, сухой остаток; вычисляют: жесткость общую, карбонатную и некарбонатную, С0 2агрес.
Специальный анализ. Помимо характеристик, определяемых при перечисленных выше типах анализа, этот анализ включает установление специальных показателей (микрокомпонентов, органических веществ, газов, Eh и др.) по особому заданию в соответствии с целевым назначением исследований. Количество отбираемой для анализа воды зависит от точности и чувствительности анализа и минерализации воды. Чем выше требования к чувствительности и точности анализа, тем больше должен быть объем пробы; пресные и слабо минерализованные воды отбирают в ббльших объемах, чем сильно минерализованные. При полевом анализе обычно бывает достаточно 0,5 л воды, при сокращенном — от 0,5 до 1,0 л (в зависимости от минерализации), а при полном — от 1,0 до 2,0 л. Для определения неустойчивых (изменяющихся во времени) компонентов — С02, H 2 S, 02, Fe и др. — применяют специальные методы отбора и хранения проб.
Результаты химического анализа воды выражают в массовых количествах веществ, растворенных в 1 л (или в 1 кг воды), в эквивалентных количествах или в процент-эквивалентных количествах (%-экв) воды. В гидрогеологической практике принято массовые количества компонентов выражать в миллиграммах на 1 л (мг/л), а эквивалентные количества ионов — в миллиграмм-эквивалентах (мг-экв) каждого иона в 1 л воды.
Величину сухого (плотного) остатка получают взвешиванием пробы после выпаривания воды. Сумму ионов определяют суммированием массы всех ионов, содержащихся в исследуемой воде. Сумма минеральных веществ — более полное выражение, чем сумма ионов, так как она учитывает и недиссоциированные неорганические вещества Si0 2 и Fe 2 03.
В настоящее время принята ионная форма выражения химических анализов воды. Данные лабораторных анализов подземных
вод, выраженные в мг/л, подвергаются дальнейшей обработке (табл.ниже).
источник
Основными задачами химического анализа подземных вод в практике гидрогеологических исследований являются:
- • изучение закономерностей формирования и распространения подземных вод различного состава;
- • оценка состава и свойств подземных вод для питьевого, технического, сельскохозяйственного, лечебного и других видов исследования;
- • исследования подземных вод как критерии при поисках месторождений полезных ископаемых — нефти, газа, солей, различных руд;
- • оценка подземных вод как химического сырья для получения йода, брома, бора и других элементов.
Существует четыре типа химических анализов подземных вод: полевой, сокращенный, полный и специальный.
Полевой анализ наиболее прост, он применяется для предварительной характеристики подземных вод района. Его проводят в полевых условиях в походных гидрохимических лабораториях, часто упрощенными методами. При полевом анализе определяют: физические свойства воды, ее pH, наличие СГ, S04 _ , NO3, HCOj, СО 2- , общую жесткость, присутствие Са 2+ , Fe 2+ , Fe 3+ , NH4, N02, С02своб; вычисляют: Na + + К + , карбонатную жесткость, Mg 2+ и общую минерализацию.
Сокращенный анализ. Этот анализ производят более точными методами в стационарных лабораториях. При сокращенном анализе определяют: физические свойства воды, величину pH, содержание ионов и компонентов (СГ, S04
Ca 2+ , Mg 2+ , Fe 2+ , Fe 3+ , NH4, N02, свободную и агрессивную углекислоту С02, Si02, окисляемость, сухой остаток, жесткость общую, карбонатную и некарбонатную.
Полный анализ применяется для подробной характеристики химического состава подземных вод. Он производится наиболее точными методами в стационарных лабораториях. Анализ позволяет произвести контроль определений как по сухому остатку, так и по суммам мг-экв катионов и анионов. При полном анализе определяют: физические свойства воды, ее pH, наличие СГ, SO4 — , NO3, HCOJ, СО3 2 -, Na + , К + , Са 2+ , Mg 2+ , Fe 2+ , Fe 3+ , NHj, NOJ, С02своб и C02 arpec, Si02, окисляемость, сухой остаток; вычисляют: жесткость общую, карбонатную и некарбонатную, С02 агрес.
Специальный анализ. Помимо характеристик, определяемых при перечисленных выше типах анализа, этот анализ включает установление специальных показателей (микрокомпонентов, органических веществ, газов, Eh и др.) по особому заданию в соответствии с целевым назначением исследований. Количество отбираемой для анализа воды зависит от точности и чувствительности анализа и минерализации воды. Чем выше требования к чувствительности и точности анализа, тем больше должен быть объем пробы; пресные и слабо минерализованные воды отбирают в больших объемах, чем сильно минерализованные. При полевом анализе обычно бывает достаточно 0,5 л воды, при сокращенном — от 0,5 до 1,0 л (в зависимости от минерализации), а при полном — от 1,0 до 2,0 л. Для определения неустойчивых (изменяющихся во времени) компонентов — С02, H2S, 02, Fe и др. — применяют специальные методы отбора и хранения проб.
Результаты химического анализа воды выражают в массовых количествах веществ, растворенных в 1 л (или в 1 кг воды), в эквивалентных количествах или в процент-эквивалентных количествах (%-экв) воды. В гидрогеологической практике принято массовые количества компонентов выражать в миллиграммах на 1 л (мг/л), а эквивалентные количества ионов — в миллиграмм-эквивалентах (мг-экв) каждого иона в 1 л воды.
Величину сухого (плотного) остатка получают взвешиванием пробы после выпаривания воды. Сумму ионов определяют суммированием массы всех ионов, содержащихся в исследуемой воде. Сумма минеральных веществ — более полное выражение, чем сумма ионов, так как она учитывает и недиссоциированные неорганические вещества Si02 и Fe23.
В настоящее время принята ионная форма выражения химических анализов воды. Данные лабораторных анализов подземных вод, выраженные в мг/л, подвергаются дальнейшей обработке (табл. 7.1).
Результаты химического анализа подземных вод
Разнообразие химического состава подземных вод вызывает необходимость в их систематизации. Существуют различные формы и множество способов наглядного изображения химического состава вод (графики, формулы, коэффициенты и т.п.).
Формула Курлова. Принцип этой формулы — изображение содержащихся в воде ионов в убывающем порядке в виде псев- додроби, в числителе которой записаны анионы, а в знаменателе — катионы. Слева от дроби формулы приводятся следующие показатели: SP — микроэлементы (Br, I, As) и свободные газы (С02 и др.), мг/л, а также общая минерализация воды М в г/л; справа — pH, температура воды t и дебит D [14, 21].
Ионы, содержание которых в воде менее 10%, в формуле не указываются, однако некоторые исследователи считают, что следует указывать все ионы, входящие в состав подземных вод. В общем виде формула Курлова имеет вид:
Например, паспорт воды знаменитого кисловодского нарзана по формуле Курлова будет иметь следующий вид:
Формула Курлова была предложена в 1928 г., а затем претерпела некоторые изменения. Наиболее рациональным представляется вариант этой формулы, предложенный И.Ю. Соколовым в 1970 г. Он заключается в следующем.
- 1. В левой части формулы записывают (в мг/л) содержание газов, а затем микрокомпонентов, если их количество превышает норму для отнесения подземных вод к минеральным или представляет геохимический интерес.
- 2. Далее указывают величину минерализации воды М в виде дроби: в числителе — в г/л, с точностью до одного десятичного знака, в знаменателе — в эквивалентной форме, выраженной в мг-экв/л суммы анионов.
- 3. В знаменателе псевдодроби записывают в нисходящем порядке все катионы, в числителе — анионы, содержание которых составляет более 1%-экв (с точностью до целых процентов).
- 4. После псевдодроби указывают показатели, характеризующие состояние воды (pH и Eh) и ее температуру, а также перманга- натную окисляемость (в мг О/л). Для сильно минерализованных вод и рассолов в конце формулы проставляют плотность воды.
Формула Курлова позволяет полно отразить все важнейшие химические характеристики исследуемой воды и при этом считать эквивалентное и массовое содержание найденных при анализе ионов. Наименование воды по ее ионному составу, т.е. чтение этой формулы, согласно ГОСТу 13273—73 на минеральные воды таково: сначала называют подчиненные ионы, потом — преобладающие. Так, название воды, записанное в виде приведенной выше формулы, следующее: сульфатно-гидрокарбонатная, кальциево-натриевая вода (в названии обычно учитывают два катиона и два аниона или ионы, содержание которых равно или превышает 25%-экв).
Жесткость. Для пресной воды различают общую, временную (или устранимую) и постоянную жесткость. Общая жесткость обусловлена суммарным содержанием в воде ионов Са 2+ и Mg 2+ . Временную (устранимую) жесткость придают воде карбонаты кальция и магния, осаждающиеся при кипячении воды в виде накипи вследствие разрушения гидрокарбонат-иона:
Разность между общей и временной жесткостью называют постоянной жесткостью, она связана с присутствием сульфатов и галоидов кальция и магния. В настоящее время в России принято выражать жесткость в мг-экв/л (1 мг-экв/л соответствует содержанию 20,04 мг/л Са 2+ или 12,16 мг/л Mg 2+ ).
Для графического изображения химического состава вод пользуются различными геометрическими фигурами (квадратом, треугольником и т.д.), на сторонах которых откладываются преобладающие шесть катионов и анионов, а также различными химическими формулами, например, формулой Курлова, которую часто называют паспортом подземных вод (рис. 7.2).
Рис. 7.2. Способы графического изображения химического состава воды [20, 21]:
I, II — графики-прямоугольники (соответственно без учета и с учетом минерализации); III — график-круг; IV, V — графики-треугольники (соответственно катионного и анионного состава); 7 — К + ; 2 — Na + ; 3 — Mg 2+ ; 4 — Са 2+ ; 5 — NOj; 6 — Cl — ;
К основным видам гидрогеохимической графики относятся гидрогеохимические карты, профили, колонки, разрезы, которые позволяют комплексно изучать гидрохимический режим подземных вод и выявлять определенные закономерности формирования химического состава подземных вод.
источник
Химический анализ подземных вод может служить качественным показателем использования воды для хозяйственно-питьевого водоснабжения, бальнеологических, промышленных и хозяйственных целей, а также диагностическим признаком при гидрохимических методах поисков и разведки месторождений полезных ископаемых.
Результаты химического анализа подземных вод могут быть выражены в табличной или сокращенной отчетной форме в виде формулы Курлова.
1). Табличная форма выражения химического анализа.
Количественно концентрация катионов и анионов выражается в г/дм 3 , мг/дм 3 , а эквивалентное содержание – миллимолях (ммоль) и процентах (%).
Пример расчета химического анализа воды в табличной форме приводится ниже.
| Ионы | Содержание, мг/дм 3 | Эквивалентное содержание | |
| ммоль | % | ||
| Na + Ca 2+ Mg 2+ | 88,04 22,75 15,62 | 69,9 17,6 12,5 | |
| Сумма катионов | — | 126,41 | |
| Cl — SO4 2 — HCO3 — | 98,40 17,43 3,51 | 82,5 14,5 3,0 | |
| Сумма анионов | — | 119,34 | |
| М (сухой остаток) | — | — | |
| СО2(свободный) | — | — | |
| рН водородный показатель | 5,3 | — | — |
| Т воды, градус С | — | — |
Эквивалентное (молярное) содержание определяется путем умножения каждого иона на пересчетный коэффициент, учитывающий его атомный вес и валентность и представляющий собой величины, обратные эквивалентным массам ионов (таблица 2).
| Катионы | Коэффициент | Анионы | Коэффициент |
| Na + Ca 2+ Mg 2+ | 0,0435 0,0499 0,08222 | Cl — SO4 2- HCO3 — | 0,0282 0,0208 0,0164 |
Для пересчета в %-эквивалентную форму суммы катионов и анионов в миллимолях принимаются за 100%, а затем определяется доля каждого катиона и аниона в % от соответствующей суммы катионов и анионов.
Химический анализ считается достоверным, если ошибка анализа не превышает 5%.
В нашем случае С = 2,88%. Анализ достоверен.
2) Сокращенная форма выражения химического анализа (формула М.Г. Курлова)
Формула Курлова представляет собой псевдодробь, в числителе которой в порядке убывания в %-эквивалентной форме располагаются анионы, а в знаменателе – катионы. Ионы, содержание которых менее 1%, в формулу не включаются. Проценты округляют до целых чисел.
Слева от дроби указывается содержание газов в мг/дм 3 и минерализация (М) в г/дм 3 , за которую принимается сухой остаток. Справа записывают значение (рН), температуру воды (Т) в градусах Цельсия, дебит источника в м 3 /сут и содержание микроэлементов, если такие имеются.
В нашем случае формула Курлова (таблица 1):
3) Наименование воды по химическому составу.
Наименование химического типа подземных вод должно состоять из двух частей, отражающих преобладающий анионный и катионный состав воды. Наименование химического типа воды начинается с ее анионного, а затем катионного состава в %-эквивалентной форме, превышающего 20% от суммы миллимолярной концентрации. Перечисление ионов производится в порядке возрастания концентрации – от меньшего значения к большему.
В сокращенном анализе анионы представлены хлоридами, сульфатами и гидрокарбонатами, а катионы – натрием, кальцием и магнием. В нашем случае вода хлоридно-натриевая.
4) Классификация воды по минерализации.
В зависимости от величины минерализации, за которую принимается сухой остаток, подземные воды классифицируются в соответствии с приведенной таблицей 3.
| Минерализация М, г/дм 3 | Подгруппа | Группа |
| £ 0,5 >0,5-1,0 | Весьма пресные Пресные | Пресные |
| >1,0-1,5 >1,5-3,0 >3,0-5,0 >5,0-10,0 >10,0-25,0 | Весьма слабосолоноватые Слабо солоноватые Умеренно солоноватые Солоноватые Сильно солоноватые | Солоноватые |
| >25,0-36,0 >36,0-50,0 | Слабосоленые Сильносоленые | Соленые |
| >50,0-150,0 >150,0-350,0 >350,0 | Рассолы слабые Рассолы крепкие Рассолы весьма крепкие (рапа) | Рассолы |
В нашем случае М = 6,9 г/дм 3 . Вода солоноватая.
Реакция воды обусловлена величиной концентрации водородных ионов рН, которая представляет собой обратный логарифм концентрации ионов водорода. Классификация воды по водородному показателю приведена в таблице 4.
| Водородный показатель рН при Т22 о С | Подгруппа | Группа |
| £ 3,5 >3,5-4,5 >4,5-5,5 >5,5-6,0 | Весьма кислая Кислая Умеренно кислая Слабокислая | Кислая |
| >6,0-8,0 | Нейтральная | Нейтральная |
| >8,0-8,5 >8,5-9,0 >9,0-9,5 >9,5 | Слабощелочная Умеренно щелочная Щелочная Весьма щелочная | Щелочная |
В нашем случае рН = 5,3. Вода умеренно кислая.
6) Классификация подземных вод по температуре воды.
Классификация воды по температуре приведена в таблице 5.
| Температура, Т о С | Наименование |
| 0-4 >4-20 >20-37 >37-50 >50-75 >75-100 >100-200 >200-374 | Переохлажденная Очень холодная Холодная Теплая Очень теплая Горячая Очень горячая Слабо перегретая Весьма перегретая |
Примечание: воды с температурой от 20 до 100 о С называются термальными.
В нашем случае Т15 о С. Вода холодная.
Жесткость воды имеет большое значение при использовании подземных вод для питьевого водоснабжения, промышленных и хозяйственных целей. Жесткость воды обусловливается содержанием в ней солей кальция и магния. Измеряется в миллимолях (мг-экв/дм 3 ).
Различают общую жесткость (ОЖ), устранимую или временную жесткость (УЖ) и постоянную жесткость (ПЖ).
Общая жесткость обусловлена присутствием в воде гидрокарбонатов, хлоридов и сульфатов кальция и магния и равняется сумме устранимой и постоянной жесткости.
Устранимая жесткость обусловлена присутствием в воде гидрокарбонатов кальция и магния. Такая жесткость получила название карбонатной (КЖ) и может быть устранена при кипячении
Карбонат кальция и магния выпадает в осадок, образуя накипь. При использовании такой воды для промышленных и коммунальных целей происходит отложение карбоната кальция и магния на стенках котлов и трубопроводов, что приводит к выводу их из эксплуатации.
При высоком содержании НСО3 — в воде, превышающем суммарную концентрацию кальция и магния, вся жесткость считается карбонатной.
Постоянная жесткость обусловлена наличием в воде сульфатов и хлоридов кальция и магния и равняется разности между общей и карбонатной жесткостью.
Классификация воды по общей жесткости приводится в таблице 6 (ГОСТ 6055-86).
| Содержание в ммоль | Группа жесткости |
| £ 1,5 >1,5-3,0 >3,0-6,0 >6,0-9,0 >9,0 | Очень мягкая Мягкая Умеренно жесткая Жесткая Очень жесткая |
Подземные воды, жесткость которых превышает 7 ммоль, не могут быть использованы для питьевого и промышленного водоснабжения.
В нашем случае общая жесткость составляет 38,37 ммоль, устранимая (карбонатная) – 3,50 ммоль, постоянная – 34,86 ммоль. Вода очень жесткая, непригодная для питьевого и промышленного водоснабжения.
8) Пригодность для питьевого водоснабжения.
Пригодность воды для питьевого водоснабжения нормируется ГОСТ 6055-86 «Вода питьевая». В рамках сокращенного гидрохимического анализа нормативными являются минерализация, общая жесткость, содержание Cl — и SO 2- 4 , а также величина рН с предельно допустимыми концентрациями, приведенными в таблице 7.
| Наименование показателей | ПДК | Содержание в нашем примере | Степень пригодности |
Минерализация М, мг/дм 3 Общая жесткость ОЖ, ммоль 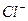 , мг/дм 3 , мг/дм 3 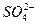 , мг/дм 3 рН , мг/дм 3 рН | 6,5-8,5 | 38,37 5,3 | Не пригодна Не пригодна Не пригодна Не пригодна Не пригодна |
В нашем случае вода по всем компонентам не пригодна для водоснабжения.
9) Пригодность для ирригационных целей.
Пригодность использования подземных вод, в том числе и шахтных, для ирригационных целей в сельском хозяйстве нормируется степенью минерализации воды и расчетным ирригационным коэффициентом. Классификация воды по минерализации, нормирующая степень пригодности для орошения сельскохозяйственных угодий, приведена в таблице 8.
| Минерализация, г/дм 3 | Степень пригодности для орошения |
| £1,7 >1,7-5,0 >5,0 | Пригодна Пригодна условно (возможно засоление) Не пригодна |
В нашем случае минерализация 6,9 г/дм 3 . Вода для орошения не пригодна.
Расчет ирригационного коэффициента выполняется в зависимости от соотношения ионов натрия, хлора и сульфатов в эквивалентной форме в миллимолях.


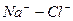
 |
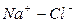

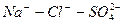
Во втором случае избыточное содержание катионов натрия может быть нейтрализовано содержащимся в воде сульфат-ионом. В третьем случае избыток натрия накапливается в почве в виде поглощенных катионов.
В первых двух случаях вода улучшению не подлежит, в третьем случае воду можно улучшить добавкой гипса. Классификация воды по ирригационному коэффициенту приведена в таблице 9.
| Ирригационный коэффициент | Характеристика воды | |||||||||||||||
| >18 >6-18 ³1,2-6,0 + — , Кир= 0,58. Вода очень плохая и улучшению не подлежит. 10) Агрессивность подземных вод. Подземные воды в зависимости от состава могут оказывать разрушающее действие на бетоны, цементы и металлы. Оценка агрессивности подземных вод по отношению к бетонам марки W4 и металлам производится на основании таблиц 5-7 и 26 СНиП 2.03.11-85 «Защита строительных конструкций от коррозии» (в скобках указаны номера таблиц согласно СНиП). Дата добавления: 2015-04-18 ; просмотров: 71 ; Нарушение авторских прав источник
|
| Материалы химического анализа подземных вод (табл. 3). Варианты
Оборудование: Работа выполняется на развернутом тетрадном листе в одном из вариантов. По результатам химического опробования водоносного горизонта (табл. 3):
1. Обработка химических анализов подземных вод К главным химическим компонентам подземных вод относятся: хлор-ион Сl — , сульфат-ион SО4 2- , гидрокарбонатный НСО3 — и карбонатный СО3 2- ионы, а также ионы щелочных и щелочноземельных металлов натрия Nа + и калия К + , кальция Са 2+ и магния Мg 2+ , железа и кремния (в коллоидном состоянии). Химический анализ воды выражают в трех формах: ионной, миллиграмм-эквивалентной и процент-эквивалентной. В природной воде молекулы солей почти полностью диссоциированы на ионы, поэтому основной формой выражения результатов анализа воды является ионная форма. Содержание каждого иона в лабораторных условиях определяют в граммах или миллиграммах в объеме 1 л. Для выяснения ряда показателей химического состава воды данные ионной формы пересчитывают в миллиграмм-эквивалентную и процент-эквивалентную. Для пересчета данных анализа из ионной формы в миллиграмм-эквивалентную необходимо количество миллиграммов каждого иона в 1 л воды разделить на его эквивалентную массу (ионная масса, деленная на валентность). Результаты определений для массовых анализов рекомендуется выражать в ионной и процент-эквивалентной форме целыми числами, а миллиграмм-эквивалентную – с точностью до второго десятичного знака. Для пересчета результатов анализа из миллиграмм-эквивалентов в процент-эквиваленты сумму миллиграмм-эквивалентов анионов и катионов принимают порознь за 100 % и вычисляют процентное содержание каждого иона в отдельности (табл.5). Имея химический анализ воды в трех формах, можно определить основные показатели химического состава воды: минерализацию, жесткость, составить формулу химического состава, определить агрессивность. Пример выражения результатов химического анализа воды в трех формах 2. Определение минерализации воды и реакции по рН Минерализация характеризует общее содержание в воде растворимых солей, а также веществ, находящихся во взвешенном и коллоидном состоянии. Для определения минерализации необходимо взять сумму анионов (А) и катионов (К) в ионной форме: Существуют различные классификации подземных вод по минерализации. Ниже приводится классификация В.И.Вернадского, соответствующая требованиям практического использования подземных вод:
Пример. Согласно данным табл. 3, минерализация составляет: 246 + 77 + 34 + 265 + 218 + 286=1126 мг/л или 1,1 г/л. Вода относится к слабосолоноватым. Реакция водывыражается показателем рН, который представляет собой десятичный логарифм концентрации водорода Н+, взятый с положительным знаком: По величине активной реакции pH воды делятся следующим образом:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||