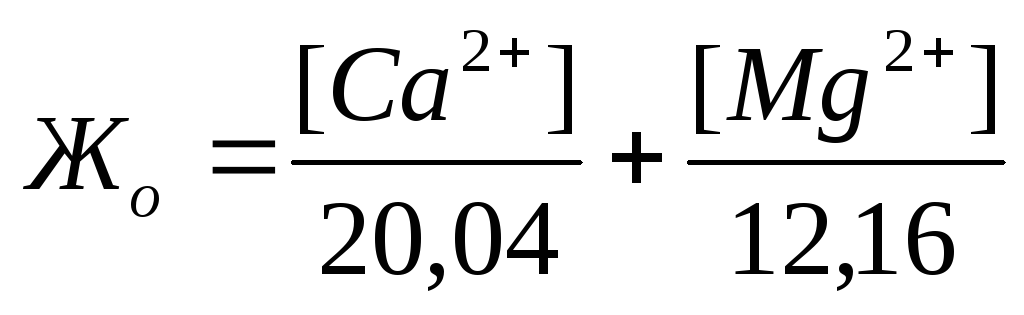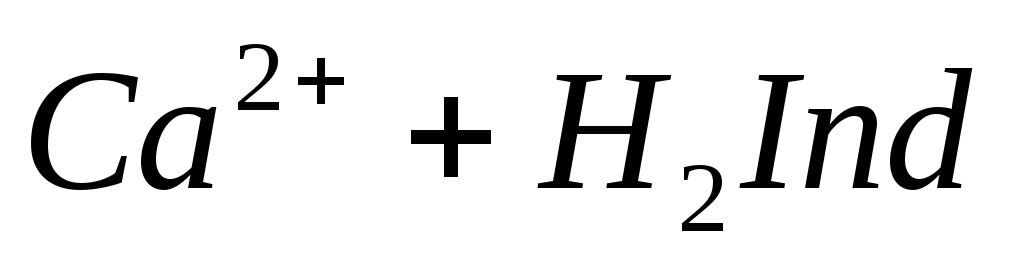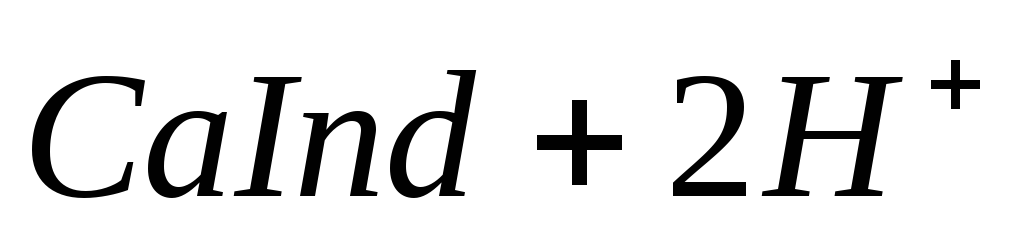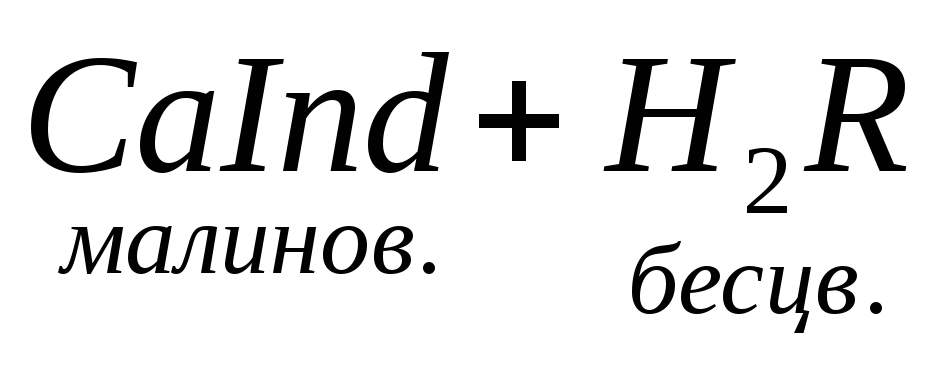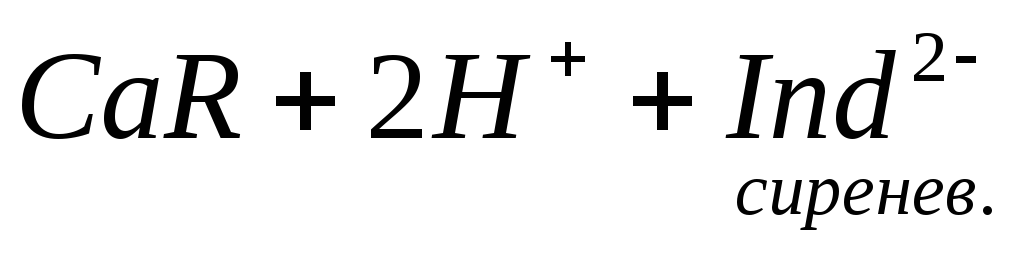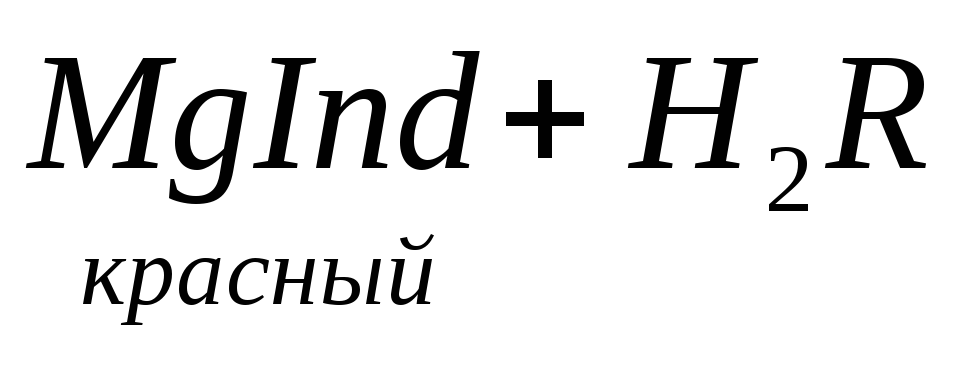Вода – это источник жизни, но она может стать и причиной отравления или заболевания.
Кроме полезных минералов вода растворяет в себе вредные химические вещества, а также является благоприятной средой для обитания микроорганизмов.
Прежде, чем использовать воду в хозяйстве, нужно убедиться в ее безопасности.
Перед использованием воды в хозяйстве или на производстве необходимо произвести предварительную подготовку: из питьевой воды нужно удалить все вредные вещества и оставить питательные минералы, а для производства нужно понизить жесткость воды и содержание тяжелых металлов.
Чтобы узнать, какие именно вещества нужно удалить из воды производится химический и бактериологический анализ. На основании полученных результатов можно подобрать подходящее очистное оборудование.
Контроль эффективности работы фильтрации воды можно определить путем проведения повторного анализа. Сравнив результаты двух последних отборов проб можно судить о правильности выбора очистного оборудования.
Минерализация – это сумма всех растворенных веществ в воде. Этот параметр еще называют солесодержанием. Единицей измерения минерализации является миллиграмм на литр (мг/л.). Существуют нормы, определяющие пригодность воды для питья. Предельно-допустимый уровень минерализации для питьевой воды составляет 500 мг/л.
Для проведения анализа на уровень минерализации в воде необходимо произвести предварительную подготовку пробы. Она заключается в разложении органических веществ и выделения определяемых элементов, которые остаются в виде неорганических соединений. Выделяется два основных метода подготовки проб: сухой – нагревание в печи, мокрый – использование кислот-окислителей.
Одним из приборов для подготовки проб является СВЧ минерализатор. Его принцип действия: подготавливаемая проба и окислительные реагенты помещаются в стеклянный сосуд, плотно закрытый крышкой. Колба переносится в СВЧ минерализатор, и прибор включается в работу. При повышении температуры ускоряется процесс окисления, и все органические примеси разлагаются за короткий промежуток времени.
Проведение анализа воды осуществляется несколькими методами, каждый из которых предназначен для определения конкретного вещества или группы веществ.
Люминесценция и фотометрия – этот метод основан на явлении люминесценции, то есть свечении. Тестируемая вода подвергается действию ультрафиолета, и различные вещества проявляют свою реакцию: ответное свечение определенного цвета.
Для фиксации этой реакции применяются регистрирующие приборы. С помощью этого метода определяется содержание следующих примесей: нефтепродукты, нитриты, нитраты, фосфаты, анионные вещества, цианиды, формальдегидов и сероводород.
ИК-спектрометрия – это анализ воды для определения наличия нефтепродуктов и жиров. Принцип действия инфракрасного спектрометра – пропускание инфракрасного излучения через воду, что вызывает колебание молекул, распространяющееся неравномерно. По длинам волн определяется примесь того или иного вещества.
Полярография – это метод анализа воды для определения концентрации ионов кадмия, цинка, свинца, органических веществ. В его основе лежит движение ионов в результате электролитической диссоциации.
Масс-спектрометрия – это анализ структуры вещества на основании отношения массы вещества к заряду ионов. Этот метод позволяет определить изотопный состав молекул.
Потенциометрия – это метод анализа воды, позволяющий определить водородный показатель (рН) и наличие фторидов. Он основан на измерении электродвижущих сил.
Дозиметрия – это метод анализа воды, выявляющий радиоактивные примеси.
Электроосмос – это процесс движения жидкости через капилляры под воздействием электрического поля.
Цель физико-химического анализа воды – выявление состава растворенных веществ. Полученная информация дает возможность применить подходящее очистное сооружение, чтобы предотвратить отравление человека, загрязнение окружающей среды или нарушения технологического процесса.
Химический анализ воды применяется во многих сферах жизни: в быту – для получения чистой и полезной питьевой воды, в промышленности – для контроля очистных сооружений сточных вод, в промышленных технологических процессах – для получения конденсата с минимальным содержанием растворенных примесей.
Существует различное оборудование для проведения анализа воды: портативные приборы для бытового использования и высокоточное лабораторное оборудование, способное проводить анализы бытовой и промышленной воды.
Анализатор жидкости «ФЛЮОРАТ – 02 – 5М» выполняет функции флуориметра, фотометра, хемилюминоминометра. Этот прибор позволяет определять содержание в воде следующих веществ: алюминия, бериллия, бора, ванадия, марганца, меди, молибдена, взвешенных частиц, мышьяка, нефтепродуктов, никеля, нитрита, общего железа, общего хрома, олова, селена, фенолов, флуоресцеина, формальдегида, цианидов и цинка.
Технические характеристики аппарата:
- Время измерения – не более 16 с.
- Допустимая погрешность 0.02.
- Рабочий спектральный диапазон 200-900 мм.
- Температура окружающего воздуха 10-350С.
- Средний срок службы – не менее 5 лет.
- Габариты: 305х320х110 мм.
- Масса – 6,5 кг.
- Питание от электросети 220 В.
- Питание от батареи 12 В.
- Частота тока 50 Гц.
Цена прибора: 564 000 рублей.
Экотестер «СОЭКС» — это дозиметрический прибор для бытового пользования, позволяющий определить радиоактивные излучения гамма-частиц и бета-частиц. Этот прибор обладает второй функцией – определение содержания нитратов в воде и продуктах питания.
- диапазон измерения радиоактивности 3-100000 мкР/ч;
- диапазон измерения концентрации нитратов: 20-5000 мг./кг;
- время измерения: 10 сек;
- питание: 2 батареи аккумуляторы, заряжаемые от электросети 220 В. 10 часов непрерывной работы.
Спектрометр TRIDION™-9 GC-TMS способен производить анализ воды, воздуха и почвы. Это портативный анализатор, производящий качественный и количественный анализ воды (химический и биологический состав воды).
- размеры 380*390*229 мм;
- вес: 14,5 кг;
- рабочая температура: 5-400С;
- влажность: до 100%;
- электропитание: от литиевой батареи;
- ввод пробы: впрыск жидкости;
- предел обнаружения: от РРВ до РРМ для большинства веществ;
- запись данных: USB накопитель.
СВЧ-минерализатор «МИНОТАВР®-2» — прибор минерализации воды под воздействием микроволнового поля. Его назначение – разложение органических веществ в воде для проведения физико-химического анализа.
Цена прибора: 357 000 рублей.
Чтобы получить официальный документ о пригодности воды к использованию в хозяйстве или на производстве нужно обратиться в сертифицированную лабораторию.
Корректность анализов будет зависеть от соблюдения технологии отбора проб и возможностей оборудования. Гарантию на чистоту анализа можно получить только в лаборатории.
источник
Вода (питьевая, дождевая, сточная, артезианская) представляет собой удобный объект для анализа, так как при использовании большинства физико-химических методов ей не требуется дополнительная пробоподготовка. Однако, это еще и очень непростой объект, так как в воде нормируется огромное количество показателей как по элементному составу, так и по органическим веществам, бактериям и проч.
Метод оптической эмиссионной спектрометрии с индуктивно-связанной плазмой (ИСП-спектрометрия) это выскоточный метод элементного анализа растворов, позволяющий определять очень малые количества тяжелых металлов в воде. Метод позволяет одновременно определять в растворе практически всю таблицу Менделеева. Очень быстрый анализ воды на множество компонентов. Удобен, когда требуется элементный анализ большого количества проб.
Оптико-эмиссионный спектрометр с индуктивно-связанной плазмой ICP-5000 — современный высокоточный прибор обеспечивающий быстрый анализ большого количества проб.
Вольтамперометрический анализ — это мощный метод определения тяжелых металлов и некоторых других токсичных элементов (мышьяк и проч.) в воде. Чувствительность метода высока и может регулироваться с изменением параметров выделения вещества на электроде. Возможно одновременное определение нескольких компонентов из одного эксперимента.
Метод очень интересен для экологических лабораторий благодаря высокой чувствительности и низкой стоимости оборудования.
Вольтамперометрический анализатор ТА-Lab — современный вольтамперометричесий анализатор, ориентированный на проведение измерений в рутинном анализе.
Потенциометрические измерения используются при анализе воды всегда. Прежде всего это измерения pH (pH-метрия). Другими вариантами потенциометрического исследования являются определение фторида и других анионов и катионов в растворе с помощью ионоселективных электродов.
Мы предлагаем широкий выбор ионоселективных электродов для потенциометрических и ионометрических измерений и pH-метр/иономер ИТАН.
Пламенно-фотометрический анализ широко используется для определения таких щелочных и щелочноземельных элементов как K, Na, Li, Ca, Sr, Ba. Метод прост и дешев с точки зрения приборного оформления, а для определения натрия и калия в воде это едва ли не самй чувствительный метод анализа.
Пламенный фотометр ФПА-2-01 это высокоавтоматизированный современный прибор для определения ионов щелочных (натрий, калий, литий) и некоторых щелочноземельных (кальций, стронций) металлов в растворах (водах, почвах, продуктах питания и проч.).
Один из старейших физико-химических методов количественного анализа самых разных образцов. Для анализа в пробу воды добавляют т.н. «цветные реагенты». Повсеместно используется в экологических и других лабораториях благодаря огромному количеству утвержденных методик и низкой стоимости оборудования
Спектрофотометрический метод позволяет определять в воде не только элементный состав (тяжелые металлы, токсичные элементы) но и органические соединения (антибиотики, токсины и проч.), а также другие нормируемые параметры.
Аналитические весы необходимы в любой лаборатории, прежде всего для пробоподготовки.
Мы можем предложить надежные выскоточные аналитические весы, микровесы и лабораторные весы. Гарантия на модели весов которые мы предлагаем составляет от 2 до 5 лет.
Одним из важнейших условий любого химического анализа является минимизация внесения загрязнений в анализируемую пробу. Именно поэтому повсеместно в аналитических лабораториях используют системы очистки воды. Невозможно обеспечить высокую точность анализа, когда вода или реактивы вносят в пробу определяемый компонент или мешающие определению примеси.
Если концентрация определяемого компонента в растворе мала часто применяют концентрирование пробы, которое проводят упариванием раствора. Концентратор образцов обеспечивает простой и удобный путь такого упаривания, одновременно защищая пробу от окисления или перегрева.
Лабораторные плитки представляют собой стандартное оборудование в лаборатории в которой планируется проводить какую-либо пробоподготовку или нагревание образцов.
Мы можем предложить Вам современные удобные и надежные плитки с программным управлением.
Нет необходимости объяснять для чего в лаборатории нужна мебель (и почему это должна быть именно лабораторная мебель). ЯРС АНАЛИТ предлагает Вам качественную, надежную и долговечную мебель для заводских лабораторий, научно-исследовательских и учебных лабораторий и практикумов институтов и университетов, Мы предлагаем вытяжные шкафы, столы различного назначения, тумбы и шкафы для хранения, мойки и прочее, необходимое в лаборатории. Вы можете выбрать размеры Вашей мебели, материалы из которых она будет изготовлена а также цветовую гамму. При необходимости мы поможем Вам с проектированием расстановки мебели в помещении, сделаем специальные изделия под размер Вашего помещения.
OOO «ЯРС АНАЛИТ»
ЛАБОРАТОРНОЕ НАУЧНОЕ И АНАЛИТИЧЕСКОЕ ОБОРУДОВАНИЕ
Телефоны отделов продаж:
Казань : +7(927)436-8071
Москва : +7(499)322-4425
Электронная почта:
Казань :
Москва :
источник
Здравствуйте! Скажите, пожалуйста, какие бывают методы экспресс-анализа качества качества питьевой воды. Если можно, расскажите поподробнее. И, если вас не затруднит, изображение установок, приборов и т.п., с помощью которых эти методы можно осуществить. Заранее спасибо! Карина
Уважаемая Карина! Действующая сегодня в России система анализа и контроля нормируемых химических и микробиологических показателей воды основана на дифференцированном определении их концентрации и сопоставлении ее с нормируемыми значениями. Кроме общего физико-химического контроля, направленного на определение жесткости воды, сухого остатка, а также наиболее распространенных в воде компонентов как естественного происхождения, так и внесенных в процессе водоподготовки (алюминий, мышьяк, нитраты, нитриты, полиакриламид, свинец, фтор, железо, марганец, медь, полифосфаты, сульфаты, хлориды, цинк), новые нормативные документы предусматривают ряд специальных операций анализа и контроля воды. Это – вирусологический, паразитологический, токсикологический (в том числе определение содержания веществ, обладающих канцерогенным и мутагенным действием при весьма низких концентрациях – пестицидов, полициклических ароматических углеводородов, летучих галогенорганических соединений, ртути, сурьмы, цианидов и др.), радиационный контроль (определение суммарной объемной активности альфаи бета-частиц и, при необходимости, радионуклеидного состава загрязнений).
В целом человечество синтезировало свыше 7 млн. химических веществ, 70 тыс. из которых применяются в повседневной жизни. По данным ВОЗ, вода сейчас содержит 13 тысяч потенциально токсичных веществ и каждый год добавляется от 500 до 1000 новых. Выявлено и нормировано же только около тысячи вредных веществ для водных объектов хозяйственно-бытового и культурно-бытового использования и около 700 веществ для рыбно-хозяйственных водоемов. При этом существующие методы анализа могут выявить ПДК лишь 10% общего количества нормированных веществ. К тому же, процессы эти сложны и длительны. Чтобы определить все показатели воды, нужно иметь соответствующее техническое оснащение, научный и технический потенциал, средства на приобретение реактивов. А это далеко не каждой лаборатории под силу. Стоимость анализа на определение содержания высокотоксичных соединений с низкими значениями ПДК может составлять сотни и тысячи долларов, причем такой анализ необходимо проводить в нескольких пунктах и с определенной периодичностью. Таким образом, проводить хороший анализ воды с каждым годом все сложнее.
Правда, на практике можно, конечное, проводить и экспресс-анализ воды на основе обобщенных показателей, таких как биохимическое или химическое потребление кислорода, содержание общего или растворимого органического углерода (для определения суммарного количества органических веществ, потребляющих кислород), содержание адсорбируемых или экстрагируемых органических галогенов (для выявления суммарного содержания галогеносодержащих органических соединений, представляющих серьезную опасность для окружающей среды), измерение уровня рН, мутности, цвета воды, органолептики и др. Внедрение обобщенных показателей в практику экспресс анализа существенно снижает число определяемых методами аналитической химии структурных компонентов, и в ряде случаев ограничивается лишь определением следов тяжелых металлов такими аппаратными методами, как атомно-абсорбционная или атомно-эмиссионная спектроскопия, о которых уже говорилось на нашем сайте.
Но даже если полный перечень вредных веществ и загрязнений определен, и количество каждого из них ниже ПДК, гарантировать высокое качество воды методом экспресс-анализа достаточно сложно. Связано это с групповым воздействием на организм содержащихся в воде веществ и химических элементов. Их взаимовлияние может настолько трансформировать воздействие на организм человека, что ПДК на отдельное вещество или химический элемент не будет отражать их истинную токсичность.
Все эти проблемы свидетельствуют о необходимости определять качество питьевой воды не только по структурному составу, но и по интегральной функциональной характеристике. Такой функциональный подход можно использовать как метод оперативного экспресс-анализа, что весьма существенно для системы экомониторинга. Существующая система обеспечения единства измерений физических параметров жидких сред на современной промышленной метрологически аттестованной аппаратуре разработана достаточно хорошо только для традиционных химических показателей. По бактериологическим показателям измерения проводятся стандартизированными “лабораторными” методами, характеризуемыми исключительной надежностью. Но эти методы анализа длительны и трудоемки (результаты можно получить только через 24-48 ч), их нельзя реализовать в системе автоматизированного контроля и трудно использовать в полевых условиях.
Из методов исследования интегральных характеристик среды наиболее доступно биотестирование. Биотестирование воды на токсичность проводят на совокупности водных организмов, позволяющей оценивать действие того или иного химического компонента на сложный биоценоз. В качестве оценочного критерия функционального качества воды могут быть выбраны выживаемость, скорость размножения, жизненная активность микроорганизмов. При проведения экспресс-анализа этим методом должны быть стандартизированы условия проведения опыта (температура среды, освещенность, кислотность, состав питательного раствора, количество живых организмов и т.д.).
При этом наиболее сложная задача мониторинга экспрессными методами – измерение бактериального и вирусного состава водной среды. Из современных инструментальных средств можно отметить лазерные системы проведения микробиологических исследований (лазерной, инфракрасной спектроскопии).
Многие вопросы аппаратного обеспечения гидромониторинга могут быть решены с помощью сенсоров – чувствительных элементов устройств экспресс-анализа, которые можно устанавливать непосредственно в местах загрязнения, а показания считывать дистанционно в автоматическом режиме работы аппаратуры. Для определения загрязнений природных и сточных вод наиболее распространены электромеханические преобразователи (амперометрические, потенциометрические, ионоселективные, на основе полевых транзисторов). Так, амперометрические сенсоры применяют для определения содержания в сточных водах СО2, аммиака, этанола, глутаминовой кислоты.
Биосенсоры просты в исполнении, доступны, обладают широкими возможностями распознавания индивидуальных компонентов, в том числе и различных бактериальных форм, при массовом производстве дешевы. Ферментативные реакции биохимической природы по своей скорости на 9-12 порядков превосходят аналогичные химические реакции. Их проведение не требует жестких агрессивных условий (высокой температуры, сильной щелочности или кислотности). Фермент в ходе реакции не расходуется, действуя лишь как высокоспецифичный катализатор, и может быть использован многократно и в малых количествах. Отличительная особенность ферментных сенсоров и иммуносенсоров – исключительная селективность при определении отдельных органических веществ, в том числе пестицидов.
На основе биосенсоров могут быть созданы многокомпонентные анализаторы, способные распознавать одновременно несколько биологических компонентов. С созданием многокомпонентных датчиков-анализаторов появляется возможность построения автоматизированной информационно-измерительной системы на базе низкоскоростной компьютерной сети.
Широкое применение сенсоры также могут найти в экспрессных тест-системах. Принцип их действия заключается в введении исследуемой пробы воды в систему, содержащую выявляемый фермент и его субстрат, с последующей регистрацией изменения оптических свойств тест-системы. Этот процесс в первую очередь – тест на наличие в пробах воды ингибирующих ферменты загрязняющих веществ антропогенного происхождения (органические вещества и тяжелые металлы, поступающие с выносом рек), а также на возникающую в таких условиях неблагоприятную ситуацию, способствующую развитию патогенной микрофлоры. Предназначены тест-системы для контроля функционального состояния и качества различных многокомпонентных природных сред (природных вод, донных отложений, взвесей и др.).
На сегодняшний день существуют следующие методы анализа воды, которые могут быть использованы для экспресс-анализа:
титрометрия
потенциометрия
спектрофотометрия
турбидиметрия
нефелометрия
кондуктометрия
атомно-абсорбционная спектрофотометрия
фотометрия и пламенная фотометрия
газовая хроматография
флюорометрия
При этом измеряются физические (значение рН, жёсткость воды), химические (содержание в воде железа, хлора, нитратов, фосыатов, тяжёлых металлов, перманганатная окисляемость) и токсикологические характеристики воды (ПДК).
Конечное, существует много других быстрых способов проверить воду на качество: попробовать ее и наверняка ощутить в муниципальной водопроводной воде добавление хлора, протестировать воду с помощью органов чувств, например на даче из поселкового водопровода, и почувствовать запах железа, отстаивать воду в течение нескольких часов и тогда может появиться белый осадок (с большой вероятностью это свидетельство повышенного содержания солей). Но все вышеперечисленные методы анализа воды имеют существенный недостаток — субъективность и большую вероятность ошибки. Единственно точный и надежный способ проверки воды на качество, пригодность для питья — это анализ воды.
Обычно делается несколько видов анализа воды:
Сокращенный анализ воды
Полный химический анализ воды
Определение отдельных групп показателей качества воды
Для того, чтобы судить о качестве воды обычно достаточно сделать сокращенный анализ воды, но в некоторых случаях необходимо протестировать воду на дополнительные показатели или провести полный анализ воды.
В настоящее время существует множество портативных тест-систем, позволяющих проводить экспресс-анализ воды в полевых условиях. Часто эти системы укомплектованы всеми необходимыми реагентами, индикаторами и специальным оборудованием, типа портативных спектрофотометров и фотокалориметров. Яркий пример таких тест-систем — системы CHEMetrics — уникальный набор экспресс-анализа качества воды в условиях производства и при полевых исследованиях.
Портативные тест-наборы «CHEMetrics» уже укомплектованы всем необходимым для проведения 30 анализов. Основной измерительный модуль выполнен в виде самозаполняемых ампул и объединяет в себе необходимые для экспресс-анализа точность и надежность. При этом анализ воды занимает около 5 минут.
Самонаполняемые ампулы содержат единичную дозу реагента, pH-буферированного и упакованного под вакуумом для сохранения аналитических свойств. Уникальность системы в том, что ампулы «CHEMetrics» подходят для колориметрического, фотометрического и титриметрического анализа.
Питьевая вода должна удовлетворять следующим качествам: питьевая вода должна быть безопасна в эпидемическом отношении, безвредна по химическому составу и обладать благоприятными органолептическими свойствами. На их основе в различных странах создаются нормативные документы в области качества питьевой воды.
Пересмотр нормативов качества питьевой воды в нашей стране осуществлялся примерно каждые 10 лет. Пересмотру подвергалась не только нормативная база, но и соответствующее методическое обеспечение выполняемых определений. Следует отметить, что при этом затрагивались в основном методики микробиологических и физико-химических анализов, вопросы органолептических показателей не рассматривались на протяжении нескольких десятилетий. Между тем, выполнение анализов на мутность, цветность и контроль запаха вызывают определенные трудности в практике производственного контроля технологии водоподготовки.
На данный момент испытательным лабораториям предлагается контролировать конкретный нормируемый показатель «мутность» двумя методами, определяющими разные физические характеристики водного объекта: фотометрией и нефелометрией. Таким образом, под одним термином «мутность» предлагается измерять различные характеристики анализируемой среды. При этом установленный норматив оставлен по ГОСТ 2874-82, для которого установлен фотометрический метод определения показателя.
Серьезной переработки требует и существующая методика определения цветности. С переходом от определения цветности визуальным методом к фотометрическому выявились две проблемы. С одной стороны, при снятии полного спектра поглощения стандартного раствора цветности определено, что максимум поглощения приходится на интервал длин волн 350-354 нм, и, таким образом, регламентация длины 413 нм приводит к нарушению одного из основных условий спектрофотометрических измерений. С другой стороны, измерения на длине волны 413 нм принципиально завышают результаты по сравнению с визуальной шкалой.
Представляется целесообразным, учитывая, что зона максимального светопоглощения анализируемой воды может изменяться с течением времени в зависимости, например, от состава природной воды по содержанию органических загрязнений, предусмотреть возможность в методике экспериментального определения зоны максимального светопоглощения и все дальнейшие измерения проводить именно на этой длине волны.
Другой немаловажной проблемой производственного контроля являются вопросы определения и классификации запахов природной и питьевой воды. Согласно рекомендациям ВОЗ привкус и запах питьевой воды не должны вызывать неприятных ощущений у потребителя. При этом для привкуса и запаха питьевой воды не предлагается никакой конкретной величины по показаниям их влияния на здоровье. По отечественным нормативным документам запах и привкус питьевой воды строго нормируются и единственный метод определения данных показателей — органолептический. Характер запаха воды предлагается определять «ощущением воспринимаемого запаха». Без строгой стандартизации метода определения и перечня характеров запахов, в такой ситуации существенно возрастает роль субъективного фактора при оценке качества питьевой воды. Получаемые результаты трудно воспроизводятся в рамках одной лаборатории между отдельными испытателями и практически не воспроизводятся между различными лабораториями даже в рамках единого предприятия. Поэтому, на сегодняшний день с учетом ужесточения требований к качеству питьевой воды вопросы методологии контроля органолептических показателей требуют серьезного пересмотра.
Кроме того, нет чётких нормативов на состав питьевой воды (солевой, микроэлементный, микробиологический), характеризующий ее биологическую активность.
В настоящее время существуют пять основных условных показателей качества питьевой воды:
1.Химические. По ним определяется состав и количество химических веществ и элементов, которые образовались после обработки воды перед подачей её в водопроводы. В частности определяется содержание в воде остаточного свободного хлора, серебра и хлороформа.
2.Органолептические. Этот вид показателей отвечает за вкусовые показатели: запах, цвет, мутность.
3.Токсикологические. С их помощью контролируется отсутствие или наличие в воде в пределах допустимых норм таких опасных веществ как фенолов, свинца, алюминия, мышьяка, пестицидов.
4.Микробиологические. По ним производят определение отсутствия в воде опасной микрофлоры.
5.Общие, в первую очередь влияющие на органолептику воды. С их помощью определяются такие параметры как общая жёсткость, отсутствие нефтепродуктов, допустимые пределы по: железу, нитратам, марганцу, кальцию, магнию, сульфидам, уровню pH.
1.Определение pH универсальным индикатором
2.Определение общей жесткости воды
3.Определение окисляемости воды
4.Определение концентрации катионов железа
5.Определение сульфатов
6.Определение ионов свинца
7.Определение ионов меди
8.Определение концентрации активного хлора в свободной и связанной формах
9.Определение органических веществ в воде
10.Определение концентрации нитрат-аниона
1. Водородный показатель рН
В пробирку наливают 5 мл исследуемой воды, 0. 1 мл универсального индикатора, перемешивают и по окраске раствора оценивают величину рН.
Розово — оранжевая
рН около 5
рН можно определить с помощью индикаторной бумаги, сравнивая её окраску со шкалой. По индикаторной бумаге более точное определение, чем визуально.
Жесткость воды обуславливается присутствием в ней ионов кальция, магния и железа и анионов: гидрокарбонат, хлорид, сульфат и нитрат. Общая жесткость складывается из карбонатной (временной) и некарбонатной (постоянной). Временная жесткость обусловлена содержанием гидрокарбонатов кальция, магния, железа. Она устраняется кипячением воды; постоянная жесткость объясняется содержанием сульфатов, хлоридов, нитратов кальция, магния, железа и не устраняется кипячением, а только химическим путем или методом ионно-обменной адсорбции. Общая и временная жесткость воды определяется путем титрования пробы воды растворами точно известной концентрации, а постоянная рассчитывается по разнице между общей и временной жесткостью.
Общая жесткость воды определяется по ГОСТ 4151-72 . Метод определения общей жесткости. Метод основан на образовании прочного комплексного соединения трилона Б с ионами кальция и магния.
Колбы конические вместимостью 250см3-3шт, капельница, трилон Б (комплексон III, двунатриевая соль этилендиаминтетрауксусной кислоты), аммоний хлористый, аммиак водный 25 %-ный раствор, натрий хлористый, спирт этиловый, хромоген черный специальный ЕТ-00(индикатор)
Приготовление 0, 05 н. раствора трилона Б.
9, 31 г трилона Б растворяют в дистиллированной воде и доводят до 1 дм 3 . Если раствор мутный, то его фильтруют. Раствор устойчив в течение нескольких месяцев. Можно приготовить раствор трилона Б фиксанала.
Приготовление буферного раствора.
10 г хлористого аммония (NH4Cl) растворяют в дистиллированной воде, добавляют 50см3 25 %-ного раствора аммиака и доводят до 500 см 3 дистиллированной водой.
Приготовление индикатора эриохрома черного
Раствор индикатора хромогена черного устойчив в течение 10 сут. Допускается пользоваться сухим индикатором. Для этого 0, 25 г индикатора смешивают с 50 г сухого хлористого натрия, предварительно тщательно растертого в ступке.
В коническую колбу на 250 мл вносят 100 мл исследуемой воды, прибавляют 5 мл буферного раствора и на кончике шпателя индикатора (эриохрома черного). Раствор перемешивают и медленно титруют 0, 05 н раствором трилона Б до изменения окраски индикатора от вишневой до синей.
Уравнение взаимодействия трилона Б (комплексона III) с ионами металлов (Ca 2+ , Mg 2+ , Fe 2+ ), содержащимися в воде:
Расчет общей жесткость производят по формуле:
Xмг. экв/л = (Vмл*Nг. экв/л*1000мг. экв/г. экв) / V1мл. ,
где: V — объем раствора трилона «Б», пошедшего на титрование, мл.
N — нормальность раствора трилона «Б» г. экв\л.
V1объем исследуемого раствора, взятого для титрования, мл.
3. Определение окисляемости воды (качественное с приближенной количественной оценкой)
Оборудование и реактивы: пробирки, H2SO4(1:3), 0, 01н КМпО4.
Определение.
5мл исследуемой воды прилить в пробирку, добавить 0, 3мл раствора H2SO4(1:3) и 0, 5мл 0, 01н раствора перманганата калия. Смесь перемешать, оставить на 20 минут. По цвету раствора оценить величину окисляемости по таблице 1.
Таблица 1
Окраска пробы воды
Окисляемость, мг/л
1. Ярко-лиловорозовая
2. лиловорозовая
3. слаболиловорозовая
4. бледнолиловорозовая
5. бледнорозовая
6. розовожелтая
7. желтая
1
2
4
6
8
12
16
4. Определение ионов железа
Оборудование и реактивы: 50% раствор KNCS, HCl-24%
Таблица 2
Приближенное определение ионов Fe +3
Окрашивание, видимое при рассмотрение пробирки сверху вниз на белом фоне
Примерное содержание ионов железа Fe +3
Отсутствие
Едва заметное желтовато-розовое
Слабое желтовато-розовое
Желтовато-розовое
Желтовато-красное
Ярко-красное
менее 0, 05
от 0, 05до 0, 1
от 0, 1 до 0, 5
от 0, 5 до 1, 0
от 1, 0 до 2, 5
более 2, 5
Определение.
К 10мл исследуемой воды прибавляют 1-2 капли HCl и 0, 2 мл (4 капли) 50%-го раствора KNCS. Перемешивают и наблюдают за развитием окраски. Примерное содержание железа находят по таблице2. Метод чувствителен, можно определить до 0, 02 мг/л.
Fe 3+ + 3NCS= Fe(NCS) 3
5. Определение сульфатов (качественное определение с приближённой количественной оценкой.)
Оборудование и реактивы
Штатив лабораторный с пробирками, пипетки 5 и 10 см3 с делениями на 0, 1 см3, колбы мерные вместимостью 100, 500 и 1000 см3, пробирки колориметрические с притертой пробкой и отметкой на 10 см3, палочки стеклянные, воронки стеклянные, HCl(1:5), BaCl2. (5%), калий сернокислый, серебро азотнокислое, вода дистиллированная.
Приготовление основного стандартного раствора сернокислого калия
0, 9071 г K2SO4 растворяют в мерной колбе вместимостью 1 дм 3 в дистиллированной воде и доводят объем раствора дистиллированной водой до метки. 1 см 3 раствора содержит 0, 5 мг сульфат-иона.
Приготовление рабочего стандартного раствора сернокислого калия
Основной раствор разбавляют 1 : 10 дистиллированной водой. 1 см 3 раствора содержит 0, 05 мг сульфат-иона.
Приготовление 5 %-ного раствора хлористого бария
5 г ВаСl2 растворяют в дистиллированной воде и доводят объем до 100 см 3 .
Приготовление 1, 7 %-ного раствора азотнокислого серебра
8, 5 г AgNO3 растворяют в 500 см 3 дистиллированной воды и подкисляют 0, 5 см 3 концентрированной азотной кислоты.
В колориметрическую пробирку диаметром 14-15 мм наливают 10 см3 исследуемой воды, добавляют 0, 5 см3 соляной кислоты (1:5). Одновременно готовят стандартную шкалу. Для этого в такие же пробирки наливают 2, 4, 8 см 3 рабочего раствора сернокислого калия и 1, 6; 3, 2; 6, 4 см 3 основного раствора K2SO4 и доводят дистиллированной водой до 10 см 3 , получая таким образом стандартную шкалу с содержанием: 10, 20, 40, 80, 160, 320 мг/дм 3 сульфат-иона. Прибавляют в каждую пробирку по 0, 5 см 3 соляной кислоты (1:5), затем в исследуемую воду и образцовые растворы по 2 см3 5 %-ного раствора хлористого бария, закрывают пробками, перемешивают и сравнивают со стандартной шкалой.
6. Определение иона свинца (качественное)
Иод калий дает в растворе с ионами свинца характерный осадок PbI2: Исследования производятся следующим образом. К испытуемому раствору прибавить немного KI, после чего, добавив CH3COOH, нагреть содержимое пробирки до полного растворения первоначально выпавшего мало характерного желтого осадка PbI2. Охладить полученный раствор под краном, при этом PbI2 выпадет снова, но уже в виде красивых золотистых кристаллов Pb 2+ +2I. = PbI2
7. Определение ионов меди (качественное)
В фарфоровую чашку поместить 3-5мл исследуемой воды, выпарить досуха, затем прибавить 1каплю конц. раствора аммиака. Появление интенсивно синего цвета свидетельствует о появлении меди
8. Определение хлорида натрия в воде(приближенная оценка)
Оборудование и реактивы: Пипетка объемом 10мл, бюретка, три конические колбы, белая кафельная плитка, проба воды, дистиллированная вода, калий хроматный индикатор, 50мл раствора AgNO3 (2, 73г на 10мл)
Определение. Наливают 10мл исследуемой воды в коническую колбу и добавляют 2капли калий-хроматного индикатора. Из бюретки оттитровывают хлорид-ион раствором AgNO3, постоянно встряхивая коническую колбу.
В конечной точке титрования осадок AgCl окрашивается в красный цвет. Дважды повторить титрование с 10мл исследуемой воды.
Подсчитать среднее количество израсходованного AgNO3. Объем израсходованного AgNO3 приблизительно равен содержанию хлоридов в пробе воды (в г/л).
9. Определение органических веществ в воде
Оборудование и реактивы: пробирки, пипетка на 2мл, HCl (1:3), KMnO4
Определение: Наливают в пробирки 2 мл фильтрата пробы, добавляют несколько капель соляной кислоты. Затем готовят розовый раствор KMnO4 и приливают его к каждой пробе по каплям. В присутствии органических веществ KMnO4 будет обесцвечиваться. Можно считать что органические вещества полностью окислены, если красная окраска сохраняется в течение одной минуты. Посчитав количество капель, которое потребуется для окисления всех органических веществ, узнаем загрязненность пробы
10. Определение нитратов (риванольная реакция)
Оборудование и реактивы: пробирки, пипетка на 5мл, 2мл, физиологический раствор (0, 9%р-р NaCl), риванол солянокислый (0, 25г риванола растворяют в 200мл 8%HCl), порошок цинка
К 1мл исследуемой воды прибавляют 2, 2мл физиологического раствора. Затем отбирают 2мл приготовленного раствора, добавляют 1мл солянокислого раствора риванола и немного порошка цинка (на кончике ножа). Если в течении 3-5минут желтая окраска риванола исчезнет и раствор окрасится в бледно-розовой цвет, то содержание нитратов в воде превышает ПДК.
Все эти вышеперечисленные методы анализа качества воды может самостоятельно провести студент 3-го курса химического ВУЗа в условиях химической (аналитической) лаборатории. Для более полного анализа качества воды существуют специальнве лаборатории Санэпидемнадзора, оснащенные современным оборудованием с применением высококачественных реактивов, что обеспечивает высокую точность и достоверность анализа воды.
7 августа 2009 24 июня 2016
Здравствуйте! Попал на ваш сайт, немного ознакомился с информацией, очень интересно, т.к. её очень много. Конечно, некоторые моменты (как например структура воды, «память» и пр. – особо сложны и дискуссионны). Мой вопрос будет очень коротким:
в статье (вопросе) Методы экспресс-анализа качества питьевой воды вы пишете «. При этом измеряются физические (значение рН, жёсткость воды). характеристики воды». С каких пор рН и жесткость стали физическими характеристиками (свойствами) воды?
Спасибо за Ваше замечание. Авторы люди и они иногда также делают опечатки. Имелись в виду такие физичекие параметры воды, как плотность ее и вязкость. Вместе со значением рН, ОВП, Eh они объеденены в группу физико-химических параметров.
Здравствуйте!
Скажите, пожалуйста, как можно проверить воду на остаточное серебро (имеется ввиду вода, проходящая через фильтры, содержащие серебро)?
Здравствуйте!
Подскажите, пожалуйста, какой набор лабораторного оборудования необходим для проведения постоянного производственного контроля качества питьевой воды , поступающей от городского Водоканала в резервуары запаса питьевой воды завода и далее в заводскую сеть питьевого водоснабжения. Городской Водоканал гарантирует качество СанПиН 2.1.4.1074-01, за исключением остаточного хлора из-за большой протяженности водоводов.
Заранее благодарю за ответ. 25.04.2016г
как провести экспресс анализ воды на содержание в ней ионов аммония?
источник
Проведение лабораторных исследований воды уже стало хорошим тоном для собственников частных домов. Наличие собственного источника водоснабжения на участке требует регулярного изучения физических параметров, а также выполнения химанализа — для получения точной информации о составе и качестве жидкости. Кроме колодезного и скважинного водоснабжения, получать точные данные о составе текущей в трубах среды нужно представителям промышленного сектора. Но где сделать химический анализ воды можно быстро, эффективно и качественно? Лаборатория нашей санэпидемслужбы предлагает четкий прайс и широкий перечень параметров для проверки. Получать результаты мы предлагаем в строго установленные сроки и на официальных бланках, соответствующих требованиям Роспотребнадзора.
Куда обращаться, если у вас возникли сомнения в качестве и чистоте жидкости, используемой в питьевых целях? Наша СЭС проведет все исследования с учетом особенностей проблемы. В первую очередь, нужно учесть, что водопроводные среды проверяются на уровень качества по стандартам СанПиН еще на стадии прохождения через станцию, централизованно. В них должны отсутствовать фекальные примеси, тяжелые металлы. Бактериологические показатели также должны соответствовать норме. Особенно важно качество питьевого сырья. Его показатели зависят от способов используемой очистки. Микробиологические пробы обычно проводятся в природных водоемах. Санобработка для водопровода подавляет развитие патогенной флоры в трубах и водных массивах.
В Москве и Московской области, несмотря на все прилагаемые усилия, сохраняется недостаточно благоприятная санитарная обстановка. Компании, предприятия, организации используют жидкости в промышленных целях и часто экономят на их очистке, выбирая самые дешевые системы. Кроме того, на состав воды сильно влияет уровень грунтовых вод, сезонные факторы. Испытательная лаборатория отмечает, что любые изменения физических характеристик должны подвергаться проверке. Если источник загрязнен, сдавать пробы в центр для исследования нужно немедленно. Но даже когда визуальных изменений нет, физико-химическая экспертиза и анализ воды, проведенный специалистами, может показать негативные изменения, связанные с содержанием примесей органического и неорганического типа.
Содержание микроэлементов минерального и металлического происхождения в каждом источнике водоснабжения абсолютно уникально. Однако существуют определенные нормативы, устанавливающие уровень их безопасного потребления организмом человека. Если он превышен, то последствия могут быть самыми негативными. При проверке хим. состава жидкостей исследуются как содержащиеся внутри них компоненты, так и органолептические показатели, способные стать достаточно информативным дополнением ко всему, что касается составления полного отчета о проведенной проверке. Изменения запаха, цвета, уровня прозрачности, вкуса — все эти факторы являются следствием наличия посторонних примесей. И если они выявляются при детальной или экспресс-проверке, следует проявить бдительность.
При изучении представленных образцов и проб специалисты лаборатории в первую очередь обращают внимание на следующие показатели:
- содержание органических примесей — окисляемых и выявляемых при помощи кислородного воздействия, кроме простого наличия, можно выявить точные наименования веществ;
- органолептические характеристики — они определяют основные показатели, влияющие на потребительские свойства жидкости;
- обобщенные или физические — плотность, жесткость, кислотность среды;
- наличие неорганических примесей — металлы, черные, цветные, тяжелые.
Современные технические средства и химические реагенты позволяют специалистам нашей лаборатории получать максимально точные и достоверные результаты исследований в короткие сроки.
Установленная на хим анализ воды из скважины стоимость для населения в нашей лаборатории всегда остается максимально доступной. Законодательно обязанность по проверке качества текущей из крана, скважины, колодца жидкости на частных собственников не возлагается. Но многие владельцы домов и квартир предпочитают контролировать эти параметры в соответствии с рекомендациями Роспотребнадзора не реже 1 раз в полугодие. Причинами для выполнения проверки могут быть следующие факторы:
- контроль за качеством применяемого для приготовления пищи и питья сырья;
- подбор системы водоподготовки с учетом состава жидкости;
- определение возможностей для целевого назначения жидкости (для аквариумистики, полива комнатных растений).
Выполнять химический анализ водопроводной воды в Москве должны представители ресурсоснабжающих организаций. В частности, на Водоканале исследование после очистки проводится сразу по 130 параметрам. Но если на выходе со станции жидкость является безопасной, нет гарантии, что она останется таковой до момента попадания в кран. Некачественное обслуживание труб приводит к развитию внутри них патогенной микрофлоры, попаданию органических или неорганических примесей. При их поступлении в организм человека — во время купания, при чистке зубов или при употреблении жидкости без кипячения, может происходить бактериальное заражение, поражение органов и тканей тяжелыми металлами. Анализ в этом случае поможет уточнить опасные компоненты.
Химический анализ воды из колодца, родника не является обязательным. Но собственники таких источников водоснабжения, как правило, предпочитают следить за тем, что они пьют. Тем более, что именно здесь чаще всего наблюдаются случаи употребления жидкостей в некипяченом виде. Распознать наличие опасных примесей по неприятному привкусу, запаху, изменению цвета можно только в 3% всех случаев загрязнения. Помимо распространенных бактерий, вроде кишечной палочки, в составе могут находиться такие компоненты, как яйца глистов, а также возбудители и споры гораздо более опасных инфекций. Так, при отсутствии данных о предыдущем использовании участка, вырытый на его территории колодец может оказаться вблизи от скотомогильника.
Химический анализ воды из скважины и стоимость его проведения — важный вопрос для обладателей собственных, автономных источников водоснабжения глубокого залегания. Если на участке присутствует подобное дополнение уже при покупке, анализ стоит сделать обязательно. Кроме того, рекомендуется выполнять проверку недавно выкопанного источника спустя 3-4 месяца, после естественного осаживания поднятых взвесей. При использовании скважины для розлива бутилированной продукции, промышленном или лечебном применении сырья, поступающего из нее, обязательно оформление установленного требованиями органов по сертификации подтверждающего документа. Именно он подтверждает соответствие уровня санитарии нормативным требованиям.
Химический анализ воды в Москве, цена которого зависит от перечня исследуемых характеристик, для бутилированной продукции обязателен. Но и здесь есть свои тонкости. К примеру, многие поставщики бутылей для кулеров заправляют их чуть ли не из водопроводной сети, без дополнительной фильтрации и обработки. Обращение в лабораторию позволяет исследовать уровень качества и безопасности жидкости. Кроме того, можно проверить микробиологические характеристики — в самой бутыли и после выхода воды из крана. Они покажут, насколько чистым и безопасным с санитарно-гигиенической точки зрения является источник питьевого сырья. Для минеральной и артезианской продукции существуют отдельные стандарты и нормативы.
В рамках применения исследований химсостава продукции может применяться целый комплекс различных методов контроля. Среди наиболее часто используемых вариантов можно отметить:
- спектрофотометрический — исследует наличие посторонних включений органического и неорганического характера в составе;
- потенциометрический — обеспечивает контроль за содержанием фторидов, водорода;
- хроматографический — обеспечивает выявление органики в составе образцов;
- гравиметрический — обеспечивает оценку сульфатных характеристик, минерализации воды;
- органолептический — основан на объективной оценке вкуса, цвета, запаха, визуальных характеристик жидкости;
- капиллярный электрофорез — позволяет выявлять экзотоксические вещества, катионы и анионы.
Аналитическая проверка воды подразумевает использование современных и эффективных средств, методов и технологий для выполнения исследований. Порядок действий зависит от того, выполняется забор проб лаборантами или самим заказчиком. Как только образцы оказываются доставлены к месту назначения, их тщательно проверяют на все заданные параметры (15 базовых, 22 или 33 вида показателей). По результатам выполненных испытаний производится составление отчетной документации.
Проводящие химический анализ воды независимые лаборатории сегодня являются одним из базовых инструментов, при помощи которых Роспотребнадзор контролирует качество питьевого сырья в регионе. Профессиональный подход в этом случае обеспечивает возможности для оптимального достижения заявленных результатов. Наша санэпидемстанция располагает собственным сертифицированным исследовательским центром, на базе которого обеспечивается выполнение контрольных мероприятий по изучению уровня безопасности предоставляемых образцов. Все работы проводятся экспертами высокого класса, способными с высокой точностью проконтролировать все значимые характеристики.
источник
Качество воды играет важную роль, оказывая непосредственное влияние на здоровье человека. Речь как о питьевой воде, так и жидкости, используемой для бытовых целей. Даже если она остается кристально чистой визуально, в ней могут содержаться опасные для организма человека микробиологические или химические компоненты, увеличивающие риск возникновения различных заболеваний.
Своевременный лабораторный анализ воды позволит убедиться в том, что химические и биологические показатели воды в норме, или же предпринять необходимые шаги по исправлению ситуации, если были обнаружены определенные нарушения. Обратившись к услугам испытательного центра «НОРТЕСТ», вы получите точный и подробный отчёт от аккредитованной лаборатории.
Наш центр проводит анализ воды в Москве из открытых водоемов, скважин, колодцев, родников, подземных источников, а также водопроводных и сточных вод. Комплексное исследование включает в себя следующие возможности:
- Оценку уровня загрязнения воды с учетом требования нормативных документов;
- Оценку качества воды из централизованных источников с помощью забора проб из открытых водоемов, а также скважин с точки зрения пригодности для питья или использования в хозяйственных целях;
- Оценку влияния воды на строительные конструкции, бетон и другие стройматериалы;
- Разработку мер и проведение мероприятий по реабилитации водоемов;
Также наша лаборатория предлагает решения по очистке воды, оценивая эффективность работы фильтров и систем водоподготовки. Полный перечень услуг зависит от задания, переданного нам заказчиком, но мы всегда готовы предложить свой вариант, учитывая многолетний опыт исследований в области.
Для исследований с высокой точностью получаемых данных используются специальные химические реактивы, с помощью которых возможные примеси и другие вредные источники определяются быстро и эффективно. Для оперативного реагирования наши специалисты выезжают на место забора проб с необходимым оборудованием для первичной оценки.
Комплексное исследование – оптимальный вариант, который гарантирует получение максимально полной картины, обнаружение всех источников опасности, а также оценку возможных вариантов по реагированию. Точечная проверка снизит эффективность результата, поэтому при первичном обращении к услугам нашей лаборатории рекомендуем провести полный анализ воды. В дальнейшем будет проще ориентироваться на имеющиеся данные.
Своевременное исследование воды позволит выстроить стратегию по исправлению ситуации — «НОРТЕСТ» составит рекомендации по эффективным мерам, которые необходимы для улучшения качества жидкости, поступающей как на промышленные предприятия, так и в дома или квартиры.
Нести опасность для потребителя может не только вода из крана – часто люди недооценивают влияние вредных веществ на колодцы, родники и скважины. Если вблизи дома или жилого сектора расположены очистные сооружения, свалки или проезжая часть, без анализа воды также не обойтись. Проверка профессиональной лабораторией с квалифицированной командой и новейшим оборудованием позволит сделать выводы о качестве воды, а также, при необходимости, принять незамедлительные меры по ее очистке.
Перечень определяемых показателей зависит от целей и задач, стоящих перед заказчиком. Мы всегда готовы порекомендовать нашим заказчикам оптимальный комплекс необходимых исследований.
источник
Требования, предъявляемые к качеству воды, могут быть самыми различными и определяются её целевым назначением. Для оценки качества пластовых, природных и сточных вод их образцы подвергают анализу. На основании результатов анализа делаются выводы о пригодности воды для конкретного вида потребления, возможности применения тех или иных методов очистки. Анализы подземных вод позволяют прогнозировать сопутствующие месторождения полезных ископаемых. При анализе вод для характеристики их свойств определяют химические, физические и бактериологические показатели. Основными показателями, определяющими пригодность воды для определенной отрасли народного хозяйства, являются химические, так как физические (содержание взвешенных частиц, температура, цвет, запах, плотность, сжимаемость, вязкость, поверхностное натяжение) и бактериологические (наличие бактерий) показатели зависят от химического состава воды.
К химическим показателям качества воды относятся:
состав растворенных газов.
Общее солесодержание характеризует присутствие в воде минеральных и органических примесей, количество этих примесей в виде общей минерализации, сухого и плотного остатков. Общая минерализация представляет собой сумму всех найденных в воде анализом катионов и анионов. Минерализацию выражают в миллиграмм-эквивалентах солей, находящихся в I л воды, или в процентах, то есть числом граммов растворенных веществ, содержащихся в 100 г раствора. Сухим остатком называется суммарное количество нелетучих веществ, присутствующих в воде во взвешенном, коллоидном и растворенном состоянии, выраженное в мг/л. Сухой остаток определяют путем выпаривания пробы воды, последующего высушивания при 105 о С и взвешивания. Плотный остаток – это сухой остаток, определенный из профильтрованной пробы воды. Следовательно, разница двух показателей соответствует содержанию взвешенных веществ пробы. Если сухой остаток прокалить при температуре 500-600 о С, то масса его уменьшится и получится остаток, называемый золой. Уменьшение массы происходит за счет сгорания органических веществ, удаления кристаллизационной воды, разложения карбонатов. Потери при прокаливании приближенно относят за счет органических примесей.
Жесткость воды обусловливается наличием в ней ионов Са 2+ и Mg 2+ . Для большинства производств жесткость воды является основным показателем её качества. В жесткой воде плохо пенится мыло. При нагревании и испарении жесткой воды образуется накипь на стенках паровых котлов, труб, теплообменных аппаратов, что ведет к перерасходу топлива, коррозии металлов и авариям.
Жесткость количественно выражается числом миллиграмм-эквивалентов ионов кальция и магния в 1 л воды (мг-экв/л); 1 мг-экв/л жесткости соответствует содержанию в воде 20,04 мг/л ионов Са 2+ или
12,16 мг/л ионов Mg 2 + . Различают жесткость общую, карбонатную и некарбонатную.
Карбонатная жесткость связана с присутствием в воде в основном гидрокарбонатов и карбонатов кальция и магния, которые при кипячении воды переходят в нерастворимые средние или основные соли и выпадают в виде плотного осадка:
Таким образом, при кипячении карбонатная жесткость устраняется. Поэтому она называется также временной жесткостью. Следует сказать, что при переходе HCO3 – в CO32 – и при выпадении карбонатов кальция и магния в воде остается некоторое количество ионов Са 2+ , Mg 2+ , CO32 – , соответствующее произведению растворимости СаСО3 и (MgOH)2CO3. В присутствии посторонних ионов растворимость этих соединений повышается.
Некарбонатная (постоянная) жесткость не разрушается кипячением. Она обусловливается присутствием в воде кальциевых и магниевых солей сильных кислот, главным образом сульфатов и хлоридов.
Общаяжесткость воды представляет собой сумму карбонатной и некарбонатной жесткости и обусловливается суммарным содержанием в воде растворенных солей кальция и магния. По величине общей жесткости принята следующая классификация природных вод:
Если известны концентрации (мг/л) в воде Ca 2+ , Mg 2+ и HCO3 – , то жесткость рассчитывается по следующим формулам:
Общая жесткость
Карбонатная жесткость равна концентрации (мг/л) [HCO3– ]; в случае, если содержание ионов кальция и магния в воде выше, чем количество гидрокарбонатов:
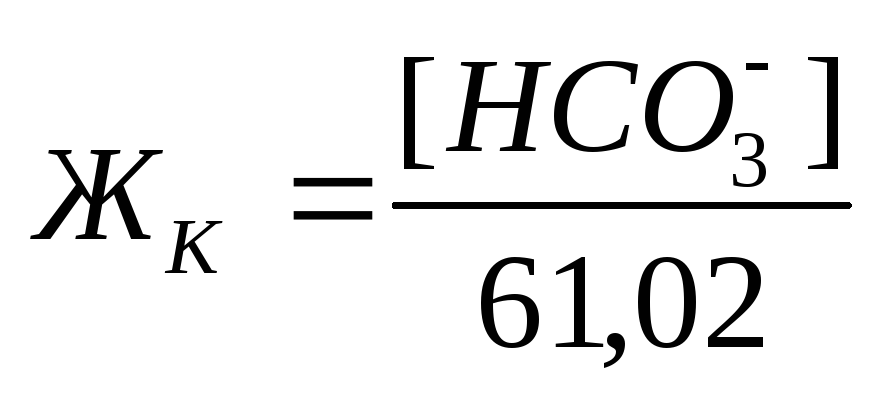
Если же количество гидрокарбонатов в воде превышает содержание ионов кальция и магния, то карбонатная жесткость соответствует общей жесткости. Разность между общей и карбонатной жесткостью составляет некарбонатную жесткость: ЖНК= ЖО– ЖК . Следовательно, ЖНК – это содержание Ca 2+ и Mg 2 + , эквивалентное концентрации всех остальных анионов, в том числе и некомпенсированных гидрокарбонатов.
Окисляемость характеризует содержание в воде восстановителей, к которым относятся органические и некоторые неорганические (сероводород, сульфиты, соединения двухвалентного железа и др.) вещества. Величина окисляемости определяется количеством затраченного окислителя и выражается числом миллиграммов кислорода, необходимого для окисления веществ, содержащихся в 1 л воды. Различают общую и частичную окисляемость. Общую окисляемость определяют обработкой воды сильным окислителем – бихроматом калия K2Cr2O7 или йодатом калия KIO3. Частичную окисляемость определяют по реакции с менее сильным окислителем – перманганатом калия КMnO4. По этой реакции окисляются только сравнительно легко окисляющиеся вещества.
Для полного окисления содержащихся в воде органических веществ, при котором происходят превращения по схеме
требуется количество кислорода (или окислителя в расчете на кислород), называемое химическим потреблением кислорода (ХПК) и выражаемое в мг/л.
При любом методе определения ХПК вместе с органическими веществами окисляются и неорганические восстановители, содержащиеся в пробе. Тогда содержание неорганических восстановителей в пробе определяют отдельно специальными методами и результаты этих определений вычитают из найденного значения ХПК.
Реакция среды характеризует степень кислотности или щелочности воды. Концентрация водородных ионов природных вод зависит главным образом от гидролиза солей, растворенных в воде, количества растворенных угольной кислоты и сероводорода, содержания различных органических кислот. Обычно для большинства природных вод величина рН изменяется в пределах 5,5-8,5. Постоянство рН природных вод обеспечивается наличием в ней буферных смесей. Изменение значения рН свидетельствует о загрязнении природной воды сточными водами.
Определение иона Cl – . В основу определения иона хлора положен аргентометрический метод Мора. Принцип анализа заключается в том, что при прибавлении к воде раствора AgNO3 образуется белый осадок хлорида серебра:
Определение хлорид-ионов ведут в интервале рН = 6,5 ÷ 10, чтобы одновременно с AgCl не выпадал осадок Ag2CO3. Проведению определения Сl – мешает наличие в воде ионов брома, йода, сероводорода, от которых освобождаются предварительной обработкой воды.
Определение иона SO42– . Метод определения сульфат-ионов основан на малой растворимости сульфата бария, количественно выпадающего в кислой среде при добавлении к воде раствора хлорида бария: Ba 2+ + SO42– = BaSO4↓
По массе образовавшегося осадка рассчитывают содержание иона SO42– .
Определение ионов CO32– и HCO3– . Эти ионы определяют титрованием пробы воды растворами серной или соляной кислот последовательно с индикаторами фенолфталеином и метилоранжем. Реакция нейтрализации протекает в две стадии.
Первые порции кислоты вступают в реакции с карбонат-ионом, образуя гидрокарбонат-ион:
Окраска фенолфталеина при рН = 8,4 переходит из розовой в бесцветную, что совпадает с таким состоянием раствора, когда в нем остаются лишь гидрокарбонаты. По количеству кислоты, пошедшей на титрование, рассчитывают содержание карбонат-иона. Расход кислот на титрование с фенолфталеином эквивалентен содержанию половины карбонатов, т.к. последние нейтрализуются только наполовину до HCO3 – . Поэтому общее количество CO32 – эквивалентно удвоенному количеству кислоты, затраченной на титрование. При дальнейшем титровании в присутствии метилоранжа происходит реакция нейтрализации гидрокарбонатов:
Метилоранж меняет окраску при pH = 4,3, т.е. в момент, когда в растворе остается только свободный диоксид углерода.
При расчете содержания ионов HCO3 – в воде следует из количества кислоты, пошедшей на титрование с метилоранжем, вычесть количество кислоты, идущей на титрование с фенолфталеином. Общее количество кислоты, затраченной на нейтрализацию ионов ОН – , СО32– и НСО3– , характеризует общую щелочность воды. Если рН воды ниже 4,3, то её щелочность равна нулю.
Определение ионов Ca 2+ , Mg 2+ . Имеется несколько методов обнаружения и определения содержания ионов Са 2+ и Mg 2+ . При добавлении в воду оксалата аммония (NH4)2C2O4 в случае присутствия ионов кальция образуется белый осадок оксалата кальция:
После отделения осадка оксалата кальция в воде можно определить ионы Mg 2+ с помощью раствора гидрофосфата натрия Na2HPO4 и аммиака. При наличии иона Mg 2 + образуется мелкокристаллический осадок соли магния:
Полученные осадки прокаливают и взвешивают. На основании полученных результатов вычисляется величина кальциевой и магниевой жесткости.
Наиболее быстрым и точным методом определения Са 2 + и Mg 2 + является комплексонометрический метод, основанный на способности двунатриевой соли этилендиаминотетрауксусной кислоты (трилон Б)
N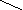
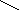
образовывать с ионами кальция и магния прочные комплексные соединения.
При титровании пробы воды трилоном Б происходит последовательное связывание в комплекс сначала ионов кальция, а затем ионов магния. Содержание ионов кальция определяют, титруя воду в присутствии индикатора — мурексида. Мурексид образует с ионами кальция малодиссоциированное комплексное соединение, окрашенное в малиновый цвет.
Ионы магния не дают комплекса с мурексидом. Трилон Б извлекает Са 2+ из его растворимого комплекса с мурексидом, вследствие чего окраска раствора, изменяется на сиреневую:
По количеству трилона Б, расходуемого на титрование, определяют содержание Са 2 + . Титрованием пробы воды трилоном Б в присутствии индикатора хромогена черного определяют суммарное содержание Са 2 + и Mg 2 + , то есть общую жесткость воды. Вода, содержащая Са 2 + и Mg 2 + , в присутствии хромогена черного окрашивается в красный цвет вследствие образования комплекса с Mg 2 + . При титровании воды в точке эквивалентности происходит изменение цвета на синий вследствие протекания следующей реакции:
Содержание Mg 2+ вычисляют по разности между общим содержанием (Са 2+ + Mg 2+ ) и содержанием Са 2 + . Трилонометрическое определение каждого иона производится при том значении рН, при котором этот ион образует с трилоном Б соединение более прочное, чем с индикатором. Для поддержания заданного значения рН к титруемому раствору добавляют буферные растворы. Кроме того, поддержание заданной величины рН обеспечивает определенную окраску индикатора. Общую жесткость воды определяют при рН > 9, кальциевую – при рН = 12.
Определение ионов Na + , K + . Производится вычислением по разности между суммой мг-экв найденных анионов и катионов, поскольку вода электронейтральна:
С достаточно высокой точностью все присутствующие в воде катионы можно определить эмиссионной спектроскопией сухого остатка.
Растворенные в воде газы определяют химическими методами или газовой хроматографией.
Определение диоксида углерода производят титрованием пробы воды щелочью в присутствии индикатора–фенолфталеина:
Определение растворенного кислорода производится йодометрическим методом.
Для анализа в пробу воды поcледовательно добавляют раствор хлорида марганца и щелочной раствор йодида калия. Метод основан на окислении свежеполученного гидроксида двухвалентного марганца содержащимся в воде кислородом:
Количество образовавшегося в воде бурого осадка гидроксида четырехвалентного марганца эквивалентно количеству растворенного кислорода. При последующем добавлении к пробе соляной или серной кислоты четырехвалентный марганец вновь восстанавливается до двухвалентного, окисляя при этом йодид калия. Это приводит к выделению свободного йода, эквивалентного содержанию четырехвалентного марганца, или, что то же самое, растворенного кислорода в пробе:
Выделившийся свободный йод определяется количественно путем титрования раствором тиосульфата натрия:
I2+ 2Na2S2O3
Йодометрический метод определения растворенного кислорода неприменим для вод, содержащих сероводород, так как сероводород вступает во взаимодействие с йодом и занижает результат. Во избежание этой ошибки предварительно связывают содержащийся в пробе сероводород в соединение, не препятствующее нормальному течению реакции. Для этой цели обычно используют хлорид ртути (II):
Определение H2S. Прежде чем приступить к количественному определению сероводорода, определяют его качественное присутствие по характерному запаху. Более объективным качественным показателем служат свинцовые индикаторные бумажки (фильтровальная бумага, пропитанная раствором ацетата свинца). При опускании в воду, содержащую сероводород, свинцовая бумага темнеет, принимая желтую (малое содержание), бурую (среднее содержание) или темно-коричневую (высокое содержание) окраску.
В водных растворах сероводород присутствует в трех формах: недиссоциированный H2S, в виде ионов HS – и S 2 – . Относительные концентрации этих форм в воде зависят от рН этой воды и в меньшей степени от температуры и общего солесодержания.
Если анализируемая вода не содержит веществ, реагирующих с иодом, то сероводород и его ионы можно определить следующим образом.
В основе количественного метода определения H2S лежит реакция окисления сероводорода йодом:
К точно отмеренному подкисленному раствору йода, взятого в избытке по отношению к ожидаемому содержанию сероводорода, прибавляют определенное количество воды. Количество йода, израсходованное на окисление сероводорода, определяется обратным титрованием остатка йода тиосульфатом. Разница между количеством раствора тиосульфата, соответствующим всему количеству взятого для анализа йода, и количеством этого же раствора, затраченного на титрование остатка йода в пробе, эквивалентна содержанию сероводорода в исследуемой пробе.
источник