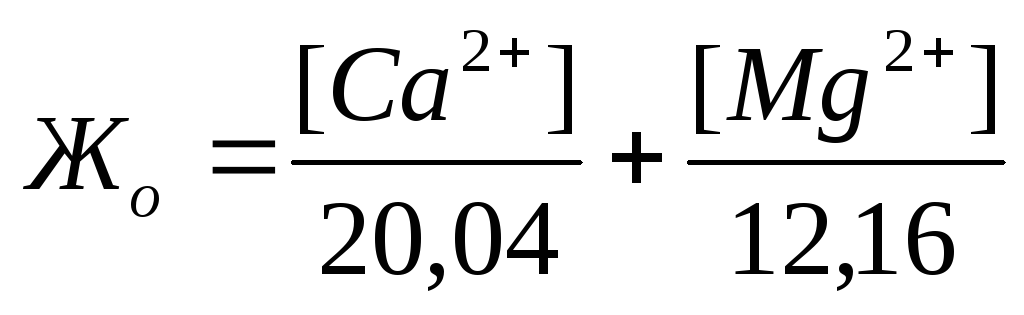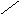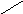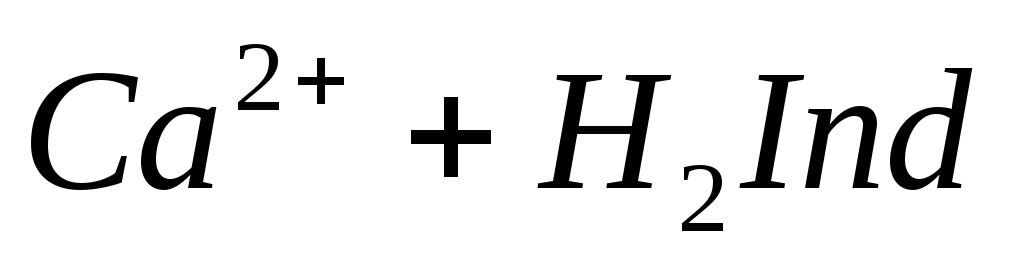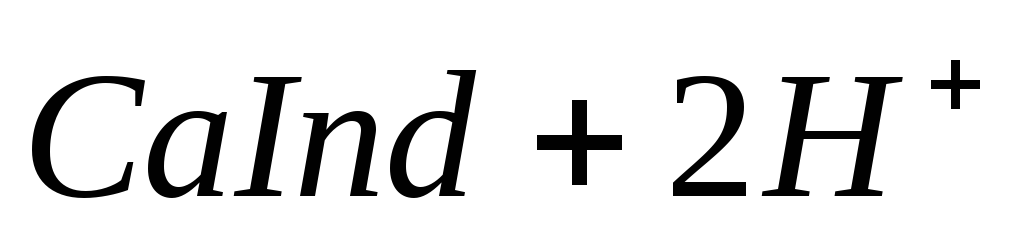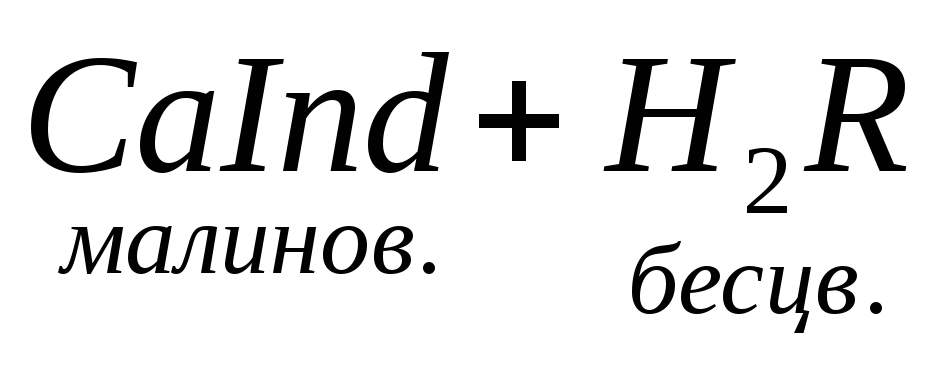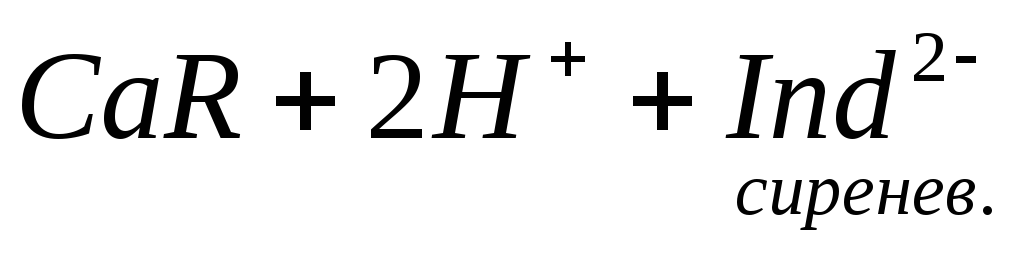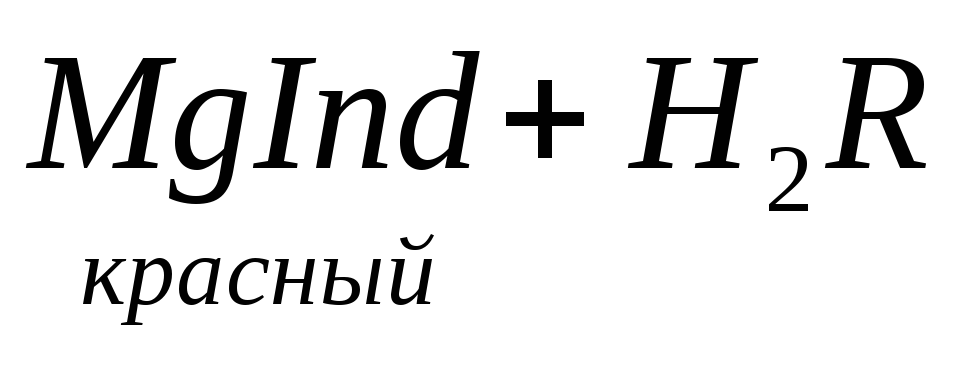Метод определения химического потребления кислорода
Water. Method for determination of chemical oxygen demand
МКС 13.060.50
ТН ВЭД 220100000
220110000
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены».
Сведения о стандарте
1 ПОДГОТОВЛЕН Обществом с ограниченной ответственностью «Протектор» совместно с группой компаний «Люмэкс»
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (Техническим комитетом по стандартизации ТК 343 «Качество воды»)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 15 ноября 2012 г. N 42)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97
Сокращенное наименование национального органа по стандартизации
Госстандарт Республики Казахстан
Госстандарт Республики Беларусь
4 Настоящий стандарт соответствует международному стандарту ISO 15705:2002* Water quality — Determination of the chemical oxygen demand index (ST-COD) — Small-scale sealed-tube method (Качество воды. Определение индекса химического потребления кислорода. Маломасштабный метод герметичных пробирок)
________________
* Доступ к международным и зарубежным документам, упомянутым здесь и далее по тексту, можно получить, перейдя по ссылке на сайт http://shop.cntd.ru. — Примечание изготовителя базы данных.
Степень соответствия — неэквивалентная (NEQ).
Настоящий стандарт подготовлен на основе применения ГОСТ Р 52708-2007 «Вода. Метод определения химического потребления кислорода»
5 Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2012 года N 1618-ст межгосударственный стандарт ГОСТ 31859-2012 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2014 года.
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
Настоящий стандарт устанавливает метод определения химического потребления кислорода (далее — ХПК) в воде с использованием фотометрии. Метод распространяется на все типы воды (питьевые, природные, сточные) в диапазоне значений ХПК от 10 до 800 мгО/дм . Метод может быть использован для анализа проб воды с более высокими значениями ХПК при условии их разбавления, но не более чем в 100 раз.
К мешающим факторам при проведении определения относят наличие в пробе воды хлоридов при их содержании свыше 1000 мг/дм и марганца (II) при его содержании свыше 50 мг/дм . Мешающие факторы устраняют разбавлением пробы воды.
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 4220-75 Реактивы. Калий двухромовокислый. Технические условия
ГОСТ ИСО 5725-6-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике*
________________
* В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике».
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ ИСО/МЭК 17025-2009 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ 24104-2001 Весы лабораторные. Общие технические требования*
________________
* В Российской Федерации действует ГОСТ Р 53228-2008 «Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания».
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 29169-91 (ИСО 648-77) Посуда лабораторная стеклянная. Пипетки с одной отметкой
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 30813-2002 Вода и водоподготовка. Термины и определения
ГОСТ 31861-2012 Вода. Общие требования к отбору проб
ГОСТ 31862-2012 Вода питьевая. Отбор проб
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
В настоящем стандарте применены термины по ГОСТ 30813 и следующий термин с соответствующим определением:
химическое потребление кислорода; ХПК: Количество кислорода, потребляемое при химическом окислении содержащихся в воде органических и неорганических веществ под действием различных окислителей.
[ГОСТ 27065-86, статья 29]Фотометр, спектрофотометр или фотометрический анализатор (далее — анализатор), снабженный адаптером для измерений оптической плотности воды и водных растворов, непосредственно находящихся в реакционных сосудах, в диапазоне длин волн от 400 до 700 нм.
Реакционные сосуды из термостойкого стекла (пробирки с завинчивающимися крышками вместимостью от 10 до 15 см ), предназначенные для обработки проб воды и измерений оптической плотности воды и водных растворов.
Нагревательный блок (термореактор), предназначенный для нагревания реакционных сосудов, обеспечивающий поддержание температуры содержимого реакционных сосудов (150±5) °С.
Перемешивающее устройство, например магнитная мешалка, эксикатор или ультразвуковая ванна.
Весы лабораторные по ГОСТ 24104 высокого или специального класса точности с ценой деления (дискретностью отсчета) 0,1 мг и наибольшим пределом взвешивания 220 г.
Колбы мерные по ГОСТ 1770 2-го класса точности вместимостью 25, 50, 1000 см .
Цилиндры мерные по ГОСТ 1770 2-го класса точности.
Стаканы химические термостойкие по ГОСТ 25336 вместимостью 1000 см .
Пипетки градуированные 2-го класса точности по ГОСТ 29227 или пипетки с одной отметкой 2-го класса точности по ГОСТ 29169, или дозаторы пипеточные с допускаемой предельной погрешностью дозирования ±5%.
Государственный (межгосударственный) стандартный образец (ГСО) бихроматной окисляемости с погрешностью аттестованного значения не более ±2%.
Вода дистиллированная по ГОСТ 6709.
Кислота серная по ГОСТ 4204, х.ч.
Сульфат ртути (II), х.ч. или ч.д.а.
Сульфат серебра, х.ч. или ч.д.а.
Калий двухромовокислый (бихромат калия) по ГОСТ 4220, х.ч. или стандарт-титр (фиксанал).
Бумага фильтровальная лабораторная по ГОСТ 12026.
Пробы воды отбирают по ГОСТ 31861, ГОСТ 31862, ГОСТ 17.1.5.05.
Для отбора, транспортирования и хранения проб воды используют емкости из стекла или полимерных материалов с навинчивающейся или пришлифованной пробкой. Емкости из полимерных материалов используют только для хранения замороженных проб воды при температуре минус 20 °С. Объем отбираемой пробы воды — не менее 100 см .
Отбор проб проводят в день выполнения анализа. Если пробы воды хранят до проведения анализа, то их подкисляют до рН меньше 2 разбавленной серной кислотой (см. 7.3.3), добавляя 10 см кислоты в расчете на 1000 см пробы. При этом пробы воды хранят при температуре от 2 °С до 8 °С не более 5 сут в защищенном от света месте.
Срок хранения замороженных до минус 20 °С проб воды — не более 1 мес.
Если проба содержит осадок, видимый невооруженным глазом, взвесь или нерастворенные органические вещества, например жиры, то перед отбором аликвотной порции пробы воды для обеспечения однородности, пробу интенсивно перемешивают, используя любое перемешивающее устройство (например магнитную мешалку, экстрактор или ультразвуковую ванну).
7.1 Подготовку анализатора к работе проводят в соответствии с руководством (инструкцией) по эксплуатации.
7.2 Подготовка реакционных сосудов
Из новой партии реакционных сосудов отбирают методом случайной выборки от 5% до 10% всего количества реакционных сосудов, но не менее трех штук. В каждый сосуд помещают по 5 см дистиллированной воды. Реакционный сосуд закрывают крышкой и проверяют на отсутствие видимых невооруженным глазом пузырьков воздуха в дистиллированной воде. При наличии пузырьков их удаляют легким постукиванием по стенке реакционного сосуда. Измеряют оптическую плотность дистиллированной воды в реакционном сосуде при длине волны 440 или 600 нм в зависимости от предполагаемого диапазона измерения значений ХПК (см. раздел 4).
Если измеренные значения оптической плотности дистиллированной воды в каждом реакционном сосуде отличаются не более чем на 0,01 единицы оптической плотности, то всю партию реакционных сосудов используют для проведения измерений ХПК.
Если измеренные значения оптической плотности дистиллированной воды в реакционных сосудах отличаются более чем на 0,01 единицы оптической плотности, то проводят сплошной контроль всей партии реакционных сосудов, отбирая для проведения измерений ХПК те из них, которые по значению оптической плотности отличаются друг от друга не более чем на 0,01 единицы оптической плотности.
Последующие проверки пригодности реакционных сосудов для измерений проводят с периодичностью не реже одного раза в месяц аналогично проверке новой партии реакционных сосудов.
7.3 Приготовление вспомогательных растворов
7.3.1 Раствор бихромата калия для измерения значений ХПК в диапазоне от 10 до 160 мгО/дм
Бихромат калия высушивают при (105±5) °С в течение 2 ч. Навеску 4,90 г высушенного бихромата калия растворяют в дистиллированной воде в мерной колбе вместимостью 1000 см и доводят объем раствора в колбе дистиллированной водой до метки. Молярная концентрация эквивалента бихромата калия составляет 0,1 моль/дм .
Допускается готовить раствор бихромата калия из стандарт-титра по прилагаемой к нему инструкции.
Срок хранения раствора — не более 6 мес.
7.3.2 Раствор бихромата калия для измерения значений ХПК в диапазоне от 80 до 800 мгО/дм
Бихромат калия высушивают при (105±5) °С в течение 2 ч. Навеску 24,52 г высушенного бихромата калия, растворяют в дистиллированной воде в мерной колбе вместимостью 1000 см и доводят объем раствора в колбе дистиллированной водой до метки. Молярная концентрация эквивалента бихромата калия составляет 0,5 моль/дм .
Допускается готовить раствор бихромата калия из стандарт-титра по прилагаемой к нему инструкции.
Срок хранения раствора — не более 6 мес.
7.3.3 Раствор серной кислоты молярной концентрации 4 моль/дм
В стеклянный стакан вместимостью 1000 см помещают около 700 см дистиллированной воды, осторожно добавляют при перемешивании 220 см концентрированной серной кислоты, охлаждают и доводят объем раствора в стакане дистиллированной водой до метки.
Срок хранения раствора — не более 12 мес.
7.3.4 Раствор серной кислоты молярной концентрации 1,8 моль/дм
В стеклянный стакан вместимостью 1000 см помещают 180 см дистиллированной воды, осторожно добавляют при перемешивании 20 см концентрированной серной кислоты.
Срок хранения раствора — не более 12 мес.
7.3.6 Раствор сульфата серебра в серной кислоте
Растворяют в стеклянной емкости 3,25 г сульфата серебра в 250 см концентрированной серной кислоты. Раствор перемешивают и оставляют в защищенном от света месте на 12 ч при комнатной температуре. Затем раствор вновь интенсивно перемешивают до полного растворения сульфата серебра.
Раствор хранят в емкости из темного стекла в условиях, исключающих воздействие прямых солнечных лучей, не более 12 мес.
7.3.7 Реагент для заполнения реакционных сосудов при измерении значений ХПК в диапазоне от 10 до 160 мгО/дм
Перед началом работы в реакционный сосуд пипеткой или дозатором вносят 0,5 см раствора бихромата калия (см. 7.3.1), осторожно добавляют 2,5 см раствора сульфата серебра (см. 7.3.6), затем 0,2 см раствора сульфата ртути (II) (см. 7.3.5). Допускается добавлять 0,05 г сухой соли сульфата ртути (II) вместо раствора сульфата ртути (II). Смесь осторожно перемешивают вращательными движениями или с использованием любого перемешивающего устройства, затем закрывают сосуд крышкой. Реакционные сосуды, заполненные реагентом, хранят в светонепроницаемой таре в защищенном от света месте при температуре от 2 °С до 8 °С.
Срок хранения заполненного реагентом реакционного сосуда — не более 12 мес. Содержимое реакционного сосуда перед применением перемешивают.
7.3.8 Реагент для заполнения реакционных сосудов при измерении значений ХПК в диапазоне от 80 до 800 мгО/дм
Реагент готовят по 7.3.7, используя раствор бихромата калия (см. 7.3.2).
Условия и срок хранения заполненного реагентом реакционного сосуда по 7.3.7. Содержимое реакционного сосуда перед применением перемешивают.
7.4 Приготовление градуировочных растворов
7.4.1 Приготовление основного раствора со значением ХПК 1000 мгО/дм
Основной раствор для измерения ХПК готовят из ГСО бихроматной окисляемости в соответствии с инструкцией по применению. Например при использовании ГСО бихроматной окисляемости с аттестованным значением ХПК 10000 мгО/дм , в мерную колбу вместимостью 50 см вносят мерной пипеткой 5 см ГСО бихроматной окисляемости и доводят объем в колбе дистиллированной водой до метки. Раствор стабилен в течение 1 мес при хранении в колбе с притертой пробкой при температуре от 2 °С до 8 °С.
7.4.2 Приготовление градуировочных растворов для диапазона значений ХПК от 10 до 160 мгО/дм
В мерные колбы вместимостью 50 см мерными пипетками вносят 0,5; 1,0; 2,0; 3,5; 5,0; 8,0 см основного раствора (см. 7.4.1) и доводят объемы в колбах дистиллированной водой до метки. Значения ХПК приготовленных растворов составляют соответственно 10; 20; 40; 70; 100; 160 мгО/дм . Растворы используют в день приготовления.
7.4.3 Приготовление градуировочных растворов для диапазона значений ХПК от 80 до 800 мгО/дм
В мерные колбы вместимостью 25 см мерными пипетками вносят 2; 5; 10; 20 см основного раствора (см. 7.4.1) и доводят объемы в колбах дистиллированной водой до метки. Значения ХПК приготовленных растворов составляют соответственно 80; 200; 400; 800 мгО/дм .
Растворы используют в день приготовления.
7.5 Градуировка анализатора
Градуировку анализатора проводят в соответствии с руководством (инструкцией) по эксплуатации с использованием градуировочных растворов (см. 7.4.2 и 7.4.3) в зависимости от диапазона измеряемых значений ХПК. В качестве нулевой пробы используют дистиллированную воду. Градуировочные растворы и нулевую пробу воды подготавливают к измерениям аналогично анализируемым пробам (см. 8.5-8.7), измеряют значения оптической плотности растворов в реакционных сосудах при длинах волн (см. раздел 4) и устанавливают градуировочную зависимость оптической плотности растворов от значения ХПК (градуировочная характеристика), используя программное обеспечение к анализатору и/или программное обеспечение, предназначенное для обработки градуировочных зависимостей. Градуировочную характеристику признают стабильной, если абсолютное значение коэффициента корреляции, установленное программным обеспечением, не менее 0,98. Если коэффициент корреляции менее 0,98, градуировку анализатора повторяют.
Контроль стабильности градуировочной характеристики проводят не реже одного раза в три месяца в соответствии с периодичностью, установленной в Руководстве по качеству лаборатории*, с использованием не менее двух заново приготовленных градуировочных растворов с различными значениями ХПК (см. 7.4.2 и 7.4.3). Контроль стабильности градуировочной характеристики проводят также при смене партии реагента.
* Документ не приводится. За дополнительной информацией обратитесь по ссылке. — Примечание изготовителя базы данных.
8.3 Проводят визуальный осмотр реакционных сосудов и их содержимого. При обнаружении в сосуде трещин, повреждений любого типа или признаков зеленой окраски раствора, реакционный сосуд не используют.
8.4 Включают нагревательный блок, нагревают его до 150 °С и выдерживают при этой температуре не менее 10 мин.
8.6 На реакционный сосуд плотно навинчивают крышку и перемешивают его содержимое, осторожно переворачивая несколько раз. Вытирают внешнюю поверхность реакционного сосуда фильтровальной бумагой. Помещают реакционный сосуд в нагревательный блок и выдерживают в течение (120±10) мин.
8.7 Осторожно, например специальными захватами, вынимают реакционные сосуды из нагревательного блока и охлаждают при комнатной температуре до температуры не выше 60 °С. Перемешивают содержимое, переворачивая реакционные сосуды. Затем охлаждают реакционные сосуды до комнатной температуры. Реакционные сосуды, в которых произошло визуально заметное уменьшение объема содержимого, для измерений не используют. Анализ пробы воды в этом случае повторяют (см. 8.1-8.6).
8.8 Если раствор после охлаждения прозрачен, то измеряют оптическую плотность пробы воды при рабочей длине волны 440 нм, используя реагент (см. 7.3.7), или при 600 нм, используя реагент (см. 7.3.8).
Если раствор мутный, то ему дают отстояться, затем измеряют его оптическую плотность как описано выше. Если после отстаивания раствор остается мутным, то анализ пробы воды повторяют, предварительно разбавив ее дистиллированной водой.
где — объем пробы воды после разбавления, см ;
— объем аликвотной порции пробы воды до разбавления (см. 8.1), см .
где — максимальное значение ХПК из двух параллельных определений (см. 9.1), мгО/дм ;
— минимальное значение ХПК из двух параллельных определений (см. 9.1), мгО/дм ;
— относительное значение предела повторяемости по таблице 1, %.
Таблица 1
источник
ПНД Ф 14.1:2.100-97
Количественный химический анализ вод. Методика выполнения измерений химического потребления кислорода в пробах природных и очищенных сточных вод титриметрическим методом
Купить ПНД Ф 14.1:2.100-97 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО «ЦНТИ Нормоконтроль».
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Документ устанавливает методику количественного химического анализа проб природных и очищенных сточных вод для определения в них величины химического потребления кислорода (ХПК) при содержании органических веществ, эквивалентном потреблению молекулярного кислорода в диапазоне от 4,0 до 80,0 мг/дм3 титриметрическим методом без концентрации пробы.
Методика допущена для целей государственного экологического контроля
3. Приписанные характеристики погрешности измерений и ее составляющих
4. Средства измерений, вспомогательные устройства, материалы, реактивы
5. Требования безопасности
6. Требования к квалификации операторов
9. Подготовка к выполнению измерений
10. Устранение мешающих влияний
12. Обработка результатов измерений
13. Оформление результатов анализа
14. Контроль качества результатов анализа при реализации методики в лаборатории
×
| Дата введения: | 01.12.2016 |
|---|---|
| Добавлен в базу: | 01.09.2013 |
| Заверение срока действия: | 01.12.2016 |
| Актуализация: | 01.01.2019 |
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:
ГОСУДАРСТВЕННЫЙ КОМИТЕТ РОССИЙСКОЙ
ФЕДЕРАЦИИ ПО ОХРАНЕ ОКРУЖАЮЩЕЙ СРЕДЫ
Государственного комитета РФ
по охране окружающей среды
_____________ А.А. Соловьянов
КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ ВОД
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ
ХИМИЧЕСКОГО ПОТРЕБЛЕНИЯ КИСЛОРОДА
В ПРОБАХ ПРИРОДНЫХ И ОЧИЩЕННЫХ СТОЧНЫХ ВОД
ТИТРИМЕТРИЧЕСКИМ МЕТОДОМ
Методика допущена для целей государственного экологического контроля
МОСКВА 1997 г.
(издание 2004 г.)
Настоящий документ устанавливает методику количественного химического анализа проб природных и очищенных сточных вод для определения в них величины химического потребления кислорода (ХПК) при содержании органических веществ, эквивалентном потреблению молекулярного кислорода в диапазоне от 4,0 до 80,0 мг/дм 3 титриметрическим методом без концентрирования пробы.
При величине ХПК > 50 мг/дм 3 определение следует проводить при соответствующем разбавлении пробы дистиллированной водой.
Определению мешают хлориды, сульфиды, соединения железа(II), нитриты и другие неорганические вещества, способные окисляться бихроматом в кислой среде.
Мешающие влияния устраняют в соответствии с п. 10.
Титриметрический метод определения ХПК основан на окислении органических веществ избытком бихромата калия в растворе серной кислоты при нагревании в присутствии катализатора — сульфата серебра. Остаток бихромата калия находят титрованием раствором соли Мора и по разности определяют количество K2Cr2O7, израсходованное на окисление органических веществ.
Настоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведённых в таблице 1.
Диапазон измерений, значения показателей точности, повторяемости, воспроизводимости
Диапазон измерений величины ХПК, мг/дм 3
Показатель точности (границы относительной погрешности при вероятности Р = 0,95),
±d, %
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости),
sr, %
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости),
sR, %
Значения показателя точности методики используют при:
— оформлении результатов анализа, выдаваемых лабораторией;
— оценке деятельности лабораторий на качество проведения испытаний;
— оценке возможности использования результатов анализа при реализации методики в конкретной лаборатории.
Весы лабораторные общего назначения с наибольшим пределом
взвешивания 200 г и ценой наименьшего деления 0,1 мг любого типа
Весы лабораторные общего назначения с наибольшим пределом
взвешивания 200 г и ценой наименьшего деления 10 мг любого типа
СО с аттестованным содержанием ХПК с погрешностью не более 1 % при Р = 0,95
Цилиндры мерные или мензурки
4.2. Вспомогательные устройства
Плитки электрические с закрытой спиралью и регулируемой
мощностью нагрева
Шкаф сушильный лабораторный с температурой нагрева до 130 °С
Стаканчики для взвешивания (бюксы)
Установки для определения ХПК в составе:
Колба К-1-250-29/32 ТС или колба Гр-250-29/32
Обратный холодильник ХПТ-2-400-29/32 ХС
Прибор вакуумного фильтрования ПВФ-35 или ПВФ-47
Средства измерений должны быть поверены в установленные сроки.
Допускается использование других, в том числе импортных, средств измерений и вспомогательных устройств с характеристиками не хуже, чем у приведенных в п.п. 4.1 и 4.2.
Бихромат калия (калий двухромовокислый)
N-фенилантраниловая кислота или
Бумага индикаторная универсальная
Фильтры мембранные Владипор типа МФАС-МА или МФАС-ОС-2 (0,45 мкм)
или фильтры бумажные обеззоленные «синяя лента»
Все реактивы, используемые для анализа, должны быть квалификации ч.д.а. или х.ч.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже ч.д.а.
5.1. При выполнении анализов необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
5.2. Электробезопасность при работе с электроустановками обеспечивается по ГОСТ 12.1.019.
5.3. Организация обучения работающих безопасности труда проводится по ГОСТ 12.0.004.
5.4. Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
Выполнение измерений может производить химик-аналитик, владеющий техникой титриметрического метода анализа.
При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
· температура окружающего воздуха (22 ± 6) °С;
· атмосферное давление (84 — 106) кПа;
· относительная влажность не более 80 % при температуре 25 °С;
· частота переменного тока (50 ± 1) Гц;
· напряжение в сети (220 ± 22) В.
8.1. Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб».
8.2. Посуду, предназначенную для отбора и хранения проб, моют хромовой смесью, затем тщательно (не менее 10 раз) промывают водопроводной и ополаскивают дистиллированной водой.
8.3. Пробы воды отбирают в стеклянную посуду с пробками, не загрязняющими пробу органическими соединениями.
В зависимости от целей анализа определение ХПК можно проводить в нефильтрованной или фильтрованной пробе. В последнем случае пробу предварительно фильтруют через мембранный фильтр 0,45 мкм, очищенный двухкратным кипячением в дистиллированной воде. Допустимо использование бумажных фильтров «синяя лента», промытых дистиллированной водой. При фильтровании через любой фильтр первые порции фильтрата отбрасывают.
Объем отбираемой пробы должен быть не менее 100 см 3 .
8.4. Определение ХПК, особенно в загрязненных водах, следует проводить как можно скорее после отбора пробы. Допускается хранение пробы при температуре не выше 4 °С не более суток при консервации добавлением раствора серной кислоты (1:2) из расчета 2 см 3 на каждые 100 см 3 пробы воды.
8.5. При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указывается:
— цель анализа, предполагаемые загрязнители;
— должность, фамилия отбирающего пробу, дата.
9.1. Приготовление растворов и реактивов
9.1.1. Раствор бихромата калия с концентрацией 0,25 моль/дм 3 эквивалента.
6,129 г бихромата калия, предварительно высушенного в течение 2 ч при 105 °С, количественно переносят его в мерную колбу вместимостью 500 см 3 , растворяют в дистиллированной воде, доводят до метки и перемешивают. Раствор устойчив при хранении в плотно закрытой темной склянке в течение 6 мес.
9.1.2. Раствор бихромата калия с концентрацией 0,025 моль/дм 3 эквивалента.
50 см 3 раствора бихромата калия с концентрацией 0,25 моль/дм 3 эквивалента помещают в мерную колбу вместимостью 500 см 3 и доводят объем раствора до метки дистиллированной водой. Хранят в склянке с притертой пробкой в темном месте не более 6 мес.
9.1.3. Раствор соли Мора с концентрацией 0,25 моль/дм 3 эквивалента.
49,0 г соли Мора переносят в мерную колбу вместимостью 500 см 3 , растворяют в дистиллированной воде, осторожно добавляют 10 см 3 концентрированной серной кислоты и после охлаждения доводят объем раствора до метки дистиллированной водой. Хранят в плотно закрытой посуде не более 6 мес.
9.1.4. Раствор соли Мора с концентрацией 0,025 моль/дм 3 эквивалента.
50 см 3 раствора соли Мора с концентрацией 0,25 моль/дм 3 эквивалента помещают в мерную колбу вместимостью 500 см 3 и доводят объем раствора до метки дистиллированной водой. Хранят в плотно закрытой посуде не более 3 мес.
Точную концентрацию раствора устанавливают ежедневно или перед серией определений в соответствии с п. 10.2.
В качестве индикатора используют раствор N-фенилантраниловой кислоты или ферроина (комплекс сульфата железа(II) с 1,10-фенантролином).
Для приготовления раствора N-фенилантраниловой кислоты 0,25 г реактива растворяют в 12 см 3 раствора гидрооксида натрия (для ускорения процесса раствор можно слегка подогреть) и разбавляют дистиллированной водой до 250 см 3 .
Для приготовления раствора ферроина 2,43 г индикатора растворяют в 100 см 3 дистиллированной воды.
При приготовлении раствора ферроина на основе 1,10-фенантролина растворяют 0,980 г соли Мора (NH4)2Fe(SO4)2 · 6H2O в 100 см 3 дистиллированной воды, добавляют 2,085 г 1,10-фенантролина моногидрата или 2,93 г сульфата и перемешивают до растворения последнего.
Раствор индикатора хранят в плотно закрытой склянке из темного стекла не более 3 мес.
9.1.6. Раствор гидроксида натрия, 0,4 %.
0,4 г NaOH растворяют в 100 см 3 дистиллированной воды. Раствор устойчив при хранении в плотно закрытой полиэтиленовой посуде не более 2 мес.
9.1.7. Раствор сульфата серебра.
5,0 г Ag2SO4 растворяют в 1 дм 3 концентрированной серной кислоты. Раствор устойчив в склянке из темного стекла в течение 6 мес.
9.2. Установление точной концентрации раствора соли Мора
Пипеткой вместимостью 10 см 3 отбирают 10 см 3 раствора бихромата калия с концентрацией 0,025 моль/дм 3 эквивалента (п. 9.1.2), переносят в коническую колбу, добавляют 180 см 3 дистиллированной воды и 20 см 3 концентрированной серной кислоты. После охлаждения добавляют в пробу 3 — 4 капли индикатора ферроина или 10 капель раствора N-фенилантраниловой кислоты и титруют раствором соли Мора с концентрацией 0,025 моль/дм 3 эквивалента (п. 9.1.4) до перехода окраски из синевато-зеленой в красно-коричневую при использовании в качестве индикатора ферроина и из красно-фиолетовой в синевато-зеленую при использовании N-фенилантраниловой кислоты.
Титрование повторяют и при отсутствии расхождения в объемах титранта более 0,05 см 3 за результат принимают среднее значение. В противном случае повторяют титрование до получения результатов, отличающихся не более, чем на 0,05 см 3 .
Точную концентрацию раствора соли Мора находят по формуле:
где См — концентрация раствора соли Мора, моль/дм 3 эквивалента;
Сб — концентрация раствора бихромата калия, моль/дм 3 эквивалента;
Vб — объем раствора бихромата калия, взятый для титрования, см 3 ;
Vм — объем раствора соли Мора, пошедший на титрование см 3 .
Мешающее влияние хлоридов при концентрациях менее 300 мг/дм 3 устраняется за счет присутствия в пробе катализатора (сульфата серебра). При больших содержаниях хлоридов к пробе добавляют сульфат ртути (II) из расчета 100 мг на 10 мг хлоридов.
Мешающее влияние сульфидов и соединений железа (II) устраняют предварительной продувкой пробы воды воздухом, если она не содержит летучих органических соединений, или учитывают при расчете ХПК. В последнем случае определяют их концентрации и пересчитывают на величины ХПК, исходя из того, что 1 мг H2S и 1 мг Fe 2+ эквивалентны соответственно 0,47 и 0,14 мг O2. Таким же образом учитывают влияние нитритов (1 мг NО2 эквивалентен 0,35 мг O2).
11.1. Выполнение измерений в водах с низкой концентрацией хлоридов
Если концентрация хлоридов в пробе анализируемой воды составляет менее 300 мг/дм 3 , в колбу со шлифом установки для определения ХПК вносят с помощью пипетки 20 см 3 воды (или аликвоту, доведенную дистиллированной водой до 20 см 3 ), добавляют 10,0 см 3 раствора бихромата калия с концентрацией 0,025 моль/дм 3 эквивалента (п. 9.1.2) и 30 см 3 раствора сульфата серебра в концентрированной серной кислоте. Для равномерного кипения в колбу бросают 2 — 3 капилляра, присоединяют к ней обратный холодильник и кипятят содержимое на песчаной бане в течение 2 ч.
После охлаждения установки промывают холодильник дистиллированной водой (около 50 см 3 ), отсоединяют его, добавляют в колбу, обмывая ее стенки, еще 50 см 3 дистиллированной воды, вновь охлаждают, переносят пробу в коническую колбу, дважды споласкивая колбу, где кипятилась проба, дистиллированной водой (по 20 — 30 см 3 ). Добавляют 3 — 4 капли раствора ферроина (или 10 капель раствора фенилантраниловой кислоты) и титруют избыток непрореагировавшего бихромата калия раствором соли Мора (п. 9.1.4) до перехода окраски индикатора из синевато-зеленой в красно-коричневую при использовании в качестве индикатора ферроина и из красно-фиолетовой в синевато-зеленую при использовании N-фенилантраниловой кислоты.
Аналогичным образом проводят холостой опыт с 20 см 3 дистиллированной воды.
11.2. Выполнение измерений в водах с высокой концентрацией хлоридов
Если концентрация хлоридов в воде превышает 300 мг/дм 3 , к отобранной для анализа пробе (20 см 3 или меньшей аликвоте, доведенной до 20 см 3 дистиллированной водой) добавляют сульфат ртути из расчета 100 мг на каждые 10 мг содержащихся в пробе хлоридов и тщательно перемешивают. Далее выполняют определение, как описано в п. 11.1. Наличие небольшого количества осадка, образовавшегося после добавления сульфата ртути, не мешает определению.
12.1. Величину ХПК (бихроматной окисляемости) анализируемой пробы воды X находят по формуле:
где Vмх — объем раствора соли Мора, израсходованный на титрование в холостом опыте, см 3 ;
Vм — объем раствора соли Мора, израсходованный на титрование в пробы воды, см 3 ;
См — концентрация раствора соли Мора, моль/дм 3 эквивалента;
V — объем пробы воды, взятый для определения, см 3 ;
8,0 — масса миллиграмм-эквивалента кислорода, мг.
Если величина ХПК в анализируемой пробе превышает верхнюю границу диапазона (80 мг/дм 3 ), разбавляют пробу с таким расчетом, чтобы величина ХПК входила в регламентированный диапазон, и выполняют определение в соответствии с п. 11.2.
В этом случае величину ХПК в анализируемой пробе воды X находят по формуле:
где ХV — величина ХПК в разбавленной пробе воды, мг/дм 3 ;
VV— объем пробы воды после разбавления, см 3 ;
v — объем аликвоты пробы воды, взятой для разбавления, см 3 .
12.2. Расхождение между результатами анализа, полученными в двух лабораториях, не должно превышать предела воспроизводимости. При выполнении этого условия приемлемы оба результата анализа, и в качестве окончательного может быть использовано их среднее арифметическое значение. Значения предела воспроизводимости приведены в таблице 2.
Значения предела воспроизводимости при вероятности Р = 0,95
Диапазон измерений величины ХПК, мг/дм 3
Предел воспроизводимости (относительное значение допускаемого расхождения
между двумя результатами измерений, полученными в разных лабораториях), R, %
При превышении предела воспроизводимости могут быть использованы методы оценки приемлемости результатов анализа согласно раздела 5 ГОСТ Р ИСО 5725-6.
Результат анализа X в документах, предусматривающих его использование, может быть представлен в виде:
где D — показатель точности методики.
Значение D рассчитывают по формуле:
Значение d приведено в таблице 1.
Если проводилось разбавление пробы воды из-за превышения величины ХПК верхней границы диапазона, значение d выбирают из таблицы 1 для величины ХПК в разбавленной пробе воды ХV.
Допустимо результат анализа в документах, выдаваемых лабораторией, представлять в виде:
источник
Химический, микробиологический анализы воды из скважин, и центрального водоснабжения, с примером допустимых показателей
Исследования помогают установить химический состав и свойства воды и выявить концентрацию всех вредных примесей. Это необходимо для обеспечения любого объекта строительства качественной питьевой водой, а также для расчетов и выбора подходящего очистительного и распределительного оборудования. От состава и свойств воды зависит расчетный срок службы прокладываемых коммуникаций и здоровье людей, использующих ее для питьевых или бытовых нужд. Именно по этой причине одним из основных этапов геоизысканий является обязательное проведение различных анализов воды из скважины, которое назначается застройщиками любых объектов, в том числе и промышленных.
Емкости, используемые для анализа воды
При этом стоит учесть, что подобные лабораторные исследования рекомендуется проводить систематически, так как химический состав воды подвержен изменениям под действием внешней среды.
Выделяют 3 основных вида показателей:
- Физические показатели, которые позволяют оценить основные свойства воды, а именно ее вкус, цвет, мутность, температурные данные, запах и информацию о взвешенных частицах в составе.
- Химические показатели. Они позволяют охарактеризовать состав воды за счет оценки концентрации основных ионов. Также в процессе исследования определяют основные показатели жесткости, уровень pH, число общей минерализации и содержание отдельных ионов, отвечающих за качество воды, фтора, железа, калия и т. д. Стоит отметить, что избыток железа влияет на цвет воды и вызывает образование осадка в трубах, который может негативно влиять на сантехническое оборудование и трубы. В то время как избыток меди влияет на вкусовые качества.
- Бактериологические показатели также отвечают за качество воды и позволяют своевременно определить заражение различными микроорганизмами. Чаще всего бактерии попадают в жидкость под воздействием внешних факторов и человеческой жизнедеятельности. Например, заражение может произойти при попадании сточных вод, при контакте воды с животными и при загрязнении различными промышленными отходами.
Показатели качества воды определяются:
- химическим анализом;
- органолептическим исследованием, в результате которого определяется жесткость и наличие железа;
- токсическим анализом, направленным на определение наличия опасных веществ;
- микробиологическим исследованием, позволяющим определить содержание бактерий в скважине, водоеме или колодце.
Результаты проверки указывают на количество определенных веществ в разных единицах измерения. При знании норм можно самостоятельно оценить основные показатели. Если все в норме, то жидкость можно считать чистой и пригодной к использованию. В противном случае нужно проводить дополнительную фильтрацию. Обычно в результатах указывают предельно допустимую концентрацию (ПДК) примесей. Этот показатель говорит, что количество определенного вещества не несет негативного воздействия. ПДК прописываются в нормативных документах.
Исследование производят для установления точного химического состава воды, а также для оценки основных свойств. Характер исследования может отличаться в зависимости от поставленных задач. Химический анализ воды подразделяют на общий и специальный. Во время общего анализа воды определяется ее общая характеристика, необходимая для ее классификации, а также для получения информации о содержании отдельных солей и ионов. Данные результаты имеют широкое назначение.
Согласно СанПиН 2.1.4.559-96, на сегодняшний день в результате исследования воды обязательно устанавливают концентрацию ионов кальция, магния, натрия, которые наряду с другими составляют основу шестикомпонентного анализа, также позволяющего определить содержание железа и уровень pH. Исследование не включает в себя определение газового состава.
Краткое описание основных исследуемых в процессе химического анализа показателей:
- Водородный коэффициент (pH) зависит от концентрации ионов.
- Жесткость воды определяют исходя из концентрации в ней солей кальция и магния.
- Щелочность базируется содержанием гидроксидов, анионов слабых кислот, бикарбонатов и карбонатов.
- Хлориды связаны с присутствием в жидкости обычной соли. При наличии с хлоридами азотсодержащих веществ есть угроза загрязнения централизованного водоснабжения бытовыми отходами.
- Сульфаты могут вызывать проблемы пищеварительной системы.
- Элементы, содержащие азот, показывают присутствие в жидкости животной органики. К ним относится аммиак, нитриты, нитраты.
- Фтор и йод. Оба вещества несут негативные последствия как при избытке, так и при дефиците. Первое вещество может вызвать рахит, заболевания зубов и крови. Второе – проблемы щитовидной железы.
- Железо в составе воды может находиться в растворенном, нерастворенном, коллоидном состоянии, а также в виде органических примесей и бактерий.
- Марганец вместе с железом оставляют желтые потеки труб, аналогичные следы остаются и на чистом белье, а также вызывают характерный привкус. Это пагубно действует на печень.
- Сероводород можно встретить в подземных водах, проводя анализ колодезной воды. Вещество относится к ядам, серьезно влияющим на здоровье людей. В воде, используемой для бытовых и питьевых нужд, присутствие сероводорода крайне опасно и запрещено.
- Хлор – наиболее распространенное средство санитарной обработки водопроводной воды. Вещество оказывает пагубное воздействие на организм и является одной из причин генетических мутаций, тяжелых отравлений, онкологических болезней. Однако в воде часто наблюдается остаточный хлор, используемый для ее обеззараживания, в безопасной концентрации.
- Натрий и калий – следствие растворения коренных пород.
Среди специальных анализов подземных вод важное место занимают:
- Санитарный, направленный на определения уровня жесткости и кислотности, содержания солей и ионов NH4, NO2, NO3. Анализ выявляют в целях определения пригодности воды для питья и бытового использования и уровня ее загрязненности.
- Бальнеологический анализ – кроме главных ионов, позволяет выявить уровень газовых компонентов, радиоактивность, число сульфатов, железо, мышьяк, литий и ряд иных показателей качества. Он считается наиболее полным и применяется для нормирования целебных источников минеральной воды, установленных требованиям ГОСТ Р 54316-2011, расположенных , например, в Карловых Варах, Ессентуках, Железноводске, Трускавце.
- Технический анализ производят для того, чтобы оценить коррозионные и агрессивные свойства воды, а также определить ее пригодность для использования в нефтедобыче, для питания паровых котельных установок или в иной технической сфере.
- Поисковый анализ питьевой воды используют наряду с техническим анализом для поиска агрессивных примесей и оценки способов ее дальнейшего использования.
Анализы воды из скважины проводят как в стационарных лабораторных условиях, так и с использованием полевых лабораторных установок непосредственно на объекте строительства. В полевых условиях часто используют исследовательские лаборатории и передвижные конструкции для анализа, разработанные учеными А. А. Резниковым (ПЛАВ), И. Ю. Соколовой и другими. Данный вид оборудования обычно состоит из упакованных смонтированных комплектов оборудования, посуды и реактивов, которые предназначены для исследований объемным, колориметрическим и нефелометрическим методами.
Химическая экспертиза воды имеет широкий спектр действия и применяется для:
- анализа питьевой воды;
- определения чистоты промышленных источников;
- подбора фильтров на производстве.
Для точности результатов рекомендуют соблюдать следующие требования:
- Емкость для пробы воды на анализ должна быть стерильной. Объем тары – 500 гр. Простерилизовать посуду может лаборатория, проводящая исследование, но процедуру несложно провести и дома. Для этой цели пробирку необходимо простерилизовать кипятком или паром. Также можно подержать емкость 10-15 мин в духовке или над открытым огнем.
- Перед забором нужно продезинфицировать кран открытым пламенем и обтереть спиртом. После этих манипуляций нужно спустить воду на полной мощности в течение 5-7 мин. Запрещается притрагиваться к крышке и горловине тары.
- Жидкость необходимо оградить от тепла и прямых солнечных лучей, так как такое воздействие способно нарушить качество, и результаты будут недостоверными. Лучше во время перевозки поместить пробирку в холодное место.
- Образец нужно передать в лабораторию и приступить к определениям максимум через 3 часа после забора.
К образцу прилагают документацию, содержащую информацию о виде источника (колодец, скважина, природный водоем и т. д.), место пробы, правильную дату и время забора, а также точный юридический адрес источника.
Качество воды из скважины и ее состав можно определить несколькими методиками. Каждая из них устанавливает определенный показатель. Химический состав воды из скважины, водоема или колодца обычно изображают в ионной, процент-эквивалентной или эквивалентной форме. Ионная форма позволяет выразить химический состав питьевой воды в виде отдельных ионов, содержащихся в ней. Они выражаются в миллиграммах (мг) или же в граммах (гр), изредка данные могут быть предоставлены как отношение к массе и объему исследуемой жидкости.
Вода в процессе визуального исследования
Сегодня все сертифицированные лаборатории, куда доставляются пробы, предоставляют результаты гидрохимических исследований в ионной форме, которая является основным изображением состава воды. Ионная форма считается основной и используется для дальнейших переходов. Если надо выполнить перевод результатов, изображенных в виде отношения к единице объема, к составу, отнесенному к единице массы, количество отдельных ионов нужно поделить на плотность, а в случае обратного перехода — помножить.
Эквивалентная форма изображения результатов и получила значительное распространение. Она дает развернутое представление о свойствах воды, позволяет определить содержание ионов и установить происхождение вод. Форма используется в аналитических целях и позволяет контролировать результаты.
Чистая водопроводная вода
Эквивалент иона представляет собой частное от деления ионной массы на валентность иона. В качестве примера можно рассмотреть содержание иона натрия в эквивалентном виде иона: Na+ = 23/1, а эквивалент иона С = 35,5/1, из этого следует вывод, что на 23 единицы массы иона Na+ приходится 35,5 единицы иона, выраженных в эквивалентах. Исходя из этого, нужно отметить, что для перехода от ионной формы к эквивалентному изображению результатов нужно разделить количество иона, выраженное в миллиграммах (мг) или граммах (гр), на величину эквивалента иона.
Вода с избыточным содержанием железа и меди
Процент-эквивалентная форма позволяет более наглядно показать ионно-солевой состав, соотношение между ионами, а также определяет черты сходства вод с различной величиной минерализации, что делает данную форму наиболее распространенной. Но изображение содержания солей в составе исследуемых жидкостей только в одной из вышеперечисленных форм не дает возможности установить абсолютное содержание ионов в воде. По этой причине желательно предоставить результаты исследований, изобразив их в эквивалентной и ионной формах.
Многообразные химические соединения имеют разную степень токсичности и могут негативно влиять на работу органов человеческого организма, а в некоторых случаях становятся причиной летального исхода. Влияние на человеческий организм.
Образец готовых результатов лабораторного протокола анализа воды
В связи с этим фактом принимают еще один показатель вредности воды – колониеобразующие единицы КОЕ. Показатель КОЕ в воде выявляет единичные микроорганизмы, способные образовывать колонии.
Все предельно допустимые концентрации (ПДК) веществ, содержащихся в составе воды, нормируются по ГОСТ 2874-82 и СанПиН 2.1.4.1074-01. При этом для расшифровки результатов возможно использовать нормативные документы, одобренные Всемирной организации здравоохранения (ВОЗ). Результат анализа в обязательном порядке должен содержать информацию о классе опасности каждого из компонентов.
Широко используют метод микробиологического анализа. Он позволяет установить качество воды из скважины и водопроводной жидкости благодаря способу мембранной фильтрации. Вода пропускается через специальную мембрану с размером сетки 0,65 мкм. Все микроорганизмы остаются на фильтре.
Для каких источников может быть назначен данный вид исследования:
- Централизованный водопровод. Исследование проводят, если имеется информация о вероятном заражении воды.
- Автономные источники, такие как скважины или колодцы. Анализ необходим в обязательном порядке и требует регулярного проведения для своевременной очистки и дезинфекции.
- Жидкости, расфасованные в тару (бутилированная вода), проверяют микробиологическим исследованием для поддержания и повышения качества.
- Стоки рекомендуется исследовать для оценки воздействия человеческой деятельности на внешнюю среду.
Микробиологическое загрязнение обычно происходит из-за воздействия промышленности, фермерских хозяйств и канализационных стоков. Анализ дает возможность своевременно провести мероприятия по очистке и предотвратить негативное воздействие на человека.
При обустройстве новой скважины микробиологический анализ необходимо выполнить дважды. Первый забор производят сразу после бурения скважины – для определения типа очистного оборудования. После подбора и установки фильтра, а также настройки систем водоподготовки проверка воды на качество нужна для того, чтобы дать оценку эффективности используемого оборудования и определить качество очищенной воды.
В дальнейшем в течение первого года работы рекомендуется проводить исследования не реже чем один раз в квартал (3 месяца). В дальнейшем как минимум раз в 12 месяцев. Своевременный контроль качества позволяет снизить риск заболеваемости и смертности, так как состав воды постоянно меняется, просочившиеся загрязненные грунтовые воды могут содержать бактерии и иные вредные примеси. Воду из колодца необходимо проверять бактериологическим методом как минимум 1 раз в 10-12 месяцев.
Забор пробы на микробиологические исследования имеет ряд отличий от забора для проведения химического исследования. Для получения наиболее точного результата рекомендуется придерживаться следующих требований:
- Использовать для забора только стерильную емкость, такую же как для химического анализа. Обычно объем тары не превышает 0,5 литра. Оптимальным вариантом будет использование емкости, приобретенной в лаборатории, в которой будет проводиться исследование.
- При использовании собственной тары необходимо заранее ее подготовить. Для этого емкость стерилизуют при помощи пара, кипятка или духового шкафа.
- Перед тем как сдать воду на анализ водопроводный кран необходимо обеззаразить спиртом и огнем, так как состав водопроводной воды подвержен изменениям под действием внешних бактерий. Затем нужно спустить воду в течение 5-6 минут, чтобы избавиться от застоявшейся в трубах воды.
- После забора емкость плотно закрывают.
- Запрещено прикасаться к горловине и внутренней стороне крышки емкости.
Стандартный средний состав морской воды с солесодержанием 35 г/л
Необходимо как можно быстрее доставить образец в лабораторию, если нет возможности сделать анализ воды в течение двух часов, пробу помещают в холодильник, где она может сохранить свои свойства на протяжении одного дня. Так же как и образец для химического анализа, пробу для микробиологического исследования в обязательном порядке сопровождает соответствующая документация. Образец для исследования доставляют в лабораторию ближайшего отделения СЭС, где можно сделать развернутый анализ. Для наиболее быстрого получения результатов желательно заранее договориться с выбранной лабораторией.
Особое место в исследовании должно занимать качество воды, критерии качества воды должны соответствовать нормативным рамкам, установленным действующим ГОСТом. Согласно формулировке ГОСТ 27065-86, под критериями качества воды понимают один или группу характерных признаков, позволяющих дать оценку ее качества. Исходя из предполагаемого назначения скважины, водоема или колодца выделяют несколько критериев, согласно которым производят оценку качества воды, основными из них являются:
- Гигиенический критерий, согласно которому учитывают общую безопасность, в том числе с точки зрения токсикологии, эпидемиологии и радиологии. Также критерий позволяет оценить благоприятные свойства и влияние на организм человека.
- Экологический критерий позволяет оценить воздействие колодца или скважины на окружающую среду и рассчитать ориентировочный срок службы водного объекта.
- Экономический критерий оценивает финансовую прибыльность источника.
- Рыбохозяйственный – дает возможность оценить качество воды различных предприятий рыбного промысла или при выборе воды для аквариумов и рыбных вольеров, что позволяет оценить возможность развития рыб и других водных животных.
Основным критерием качества принято считать гигиенический. Показатели этого критерия качества оценивают на всех этапах строительства, а также для определения качества водопроводной и питьевой (в том числе бутилированной) воды.
Гигиенические требования к питьевой воде централизованного водоснабжения устанавливаются СанПиН 2.1.4.559-96. Согласно нормативному документу, вода должна иметь безвредный химический состав и отвечать всем критериям радиационной и эпидемической безопасности.
Все данные нормативов были приняты по требованиям ВОЗ.
источник
Требования, предъявляемые к качеству воды, могут быть самыми различными и определяются её целевым назначением. Для оценки качества пластовых, природных и сточных вод их образцы подвергают анализу. На основании результатов анализа делаются выводы о пригодности воды для конкретного вида потребления, возможности применения тех или иных методов очистки. Анализы подземных вод позволяют прогнозировать сопутствующие месторождения полезных ископаемых. При анализе вод для характеристики их свойств определяют химические, физические и бактериологические показатели. Основными показателями, определяющими пригодность воды для определенной отрасли народного хозяйства, являются химические, так как физические (содержание взвешенных частиц, температура, цвет, запах, плотность, сжимаемость, вязкость, поверхностное натяжение) и бактериологические (наличие бактерий) показатели зависят от химического состава воды.
К химическим показателям качества воды относятся:
состав растворенных газов.
Общее солесодержание характеризует присутствие в воде минеральных и органических примесей, количество этих примесей в виде общей минерализации, сухого и плотного остатков. Общая минерализация представляет собой сумму всех найденных в воде анализом катионов и анионов. Минерализацию выражают в миллиграмм-эквивалентах солей, находящихся в I л воды, или в процентах, то есть числом граммов растворенных веществ, содержащихся в 100 г раствора. Сухим остатком называется суммарное количество нелетучих веществ, присутствующих в воде во взвешенном, коллоидном и растворенном состоянии, выраженное в мг/л. Сухой остаток определяют путем выпаривания пробы воды, последующего высушивания при 105 о С и взвешивания. Плотный остаток – это сухой остаток, определенный из профильтрованной пробы воды. Следовательно, разница двух показателей соответствует содержанию взвешенных веществ пробы. Если сухой остаток прокалить при температуре 500-600 о С, то масса его уменьшится и получится остаток, называемый золой. Уменьшение массы происходит за счет сгорания органических веществ, удаления кристаллизационной воды, разложения карбонатов. Потери при прокаливании приближенно относят за счет органических примесей.
Жесткость воды обусловливается наличием в ней ионов Са 2+ и Mg 2+ . Для большинства производств жесткость воды является основным показателем её качества. В жесткой воде плохо пенится мыло. При нагревании и испарении жесткой воды образуется накипь на стенках паровых котлов, труб, теплообменных аппаратов, что ведет к перерасходу топлива, коррозии металлов и авариям.
Жесткость количественно выражается числом миллиграмм-эквивалентов ионов кальция и магния в 1 л воды (мг-экв/л); 1 мг-экв/л жесткости соответствует содержанию в воде 20,04 мг/л ионов Са 2+ или
12,16 мг/л ионов Mg 2 + . Различают жесткость общую, карбонатную и некарбонатную.
Карбонатная жесткость связана с присутствием в воде в основном гидрокарбонатов и карбонатов кальция и магния, которые при кипячении воды переходят в нерастворимые средние или основные соли и выпадают в виде плотного осадка:
Таким образом, при кипячении карбонатная жесткость устраняется. Поэтому она называется также временной жесткостью. Следует сказать, что при переходе HCO3 – в CO32 – и при выпадении карбонатов кальция и магния в воде остается некоторое количество ионов Са 2+ , Mg 2+ , CO32 – , соответствующее произведению растворимости СаСО3 и (MgOH)2CO3. В присутствии посторонних ионов растворимость этих соединений повышается.
Некарбонатная (постоянная) жесткость не разрушается кипячением. Она обусловливается присутствием в воде кальциевых и магниевых солей сильных кислот, главным образом сульфатов и хлоридов.
Общаяжесткость воды представляет собой сумму карбонатной и некарбонатной жесткости и обусловливается суммарным содержанием в воде растворенных солей кальция и магния. По величине общей жесткости принята следующая классификация природных вод:
Если известны концентрации (мг/л) в воде Ca 2+ , Mg 2+ и HCO3 – , то жесткость рассчитывается по следующим формулам:
Общая жесткость
Карбонатная жесткость равна концентрации (мг/л) [HCO3– ]; в случае, если содержание ионов кальция и магния в воде выше, чем количество гидрокарбонатов:
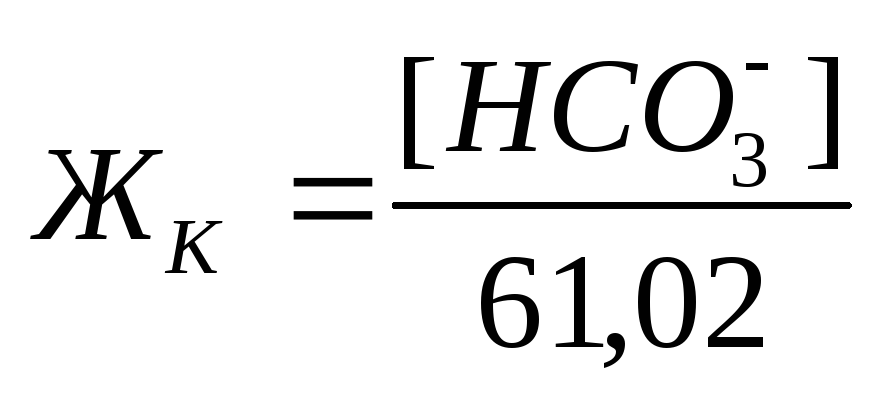
Если же количество гидрокарбонатов в воде превышает содержание ионов кальция и магния, то карбонатная жесткость соответствует общей жесткости. Разность между общей и карбонатной жесткостью составляет некарбонатную жесткость: ЖНК= ЖО– ЖК . Следовательно, ЖНК – это содержание Ca 2+ и Mg 2 + , эквивалентное концентрации всех остальных анионов, в том числе и некомпенсированных гидрокарбонатов.
Окисляемость характеризует содержание в воде восстановителей, к которым относятся органические и некоторые неорганические (сероводород, сульфиты, соединения двухвалентного железа и др.) вещества. Величина окисляемости определяется количеством затраченного окислителя и выражается числом миллиграммов кислорода, необходимого для окисления веществ, содержащихся в 1 л воды. Различают общую и частичную окисляемость. Общую окисляемость определяют обработкой воды сильным окислителем – бихроматом калия K2Cr2O7 или йодатом калия KIO3. Частичную окисляемость определяют по реакции с менее сильным окислителем – перманганатом калия КMnO4. По этой реакции окисляются только сравнительно легко окисляющиеся вещества.
Для полного окисления содержащихся в воде органических веществ, при котором происходят превращения по схеме
требуется количество кислорода (или окислителя в расчете на кислород), называемое химическим потреблением кислорода (ХПК) и выражаемое в мг/л.
При любом методе определения ХПК вместе с органическими веществами окисляются и неорганические восстановители, содержащиеся в пробе. Тогда содержание неорганических восстановителей в пробе определяют отдельно специальными методами и результаты этих определений вычитают из найденного значения ХПК.
Реакция среды характеризует степень кислотности или щелочности воды. Концентрация водородных ионов природных вод зависит главным образом от гидролиза солей, растворенных в воде, количества растворенных угольной кислоты и сероводорода, содержания различных органических кислот. Обычно для большинства природных вод величина рН изменяется в пределах 5,5-8,5. Постоянство рН природных вод обеспечивается наличием в ней буферных смесей. Изменение значения рН свидетельствует о загрязнении природной воды сточными водами.
Определение иона Cl – . В основу определения иона хлора положен аргентометрический метод Мора. Принцип анализа заключается в том, что при прибавлении к воде раствора AgNO3 образуется белый осадок хлорида серебра:
Определение хлорид-ионов ведут в интервале рН = 6,5 ÷ 10, чтобы одновременно с AgCl не выпадал осадок Ag2CO3. Проведению определения Сl – мешает наличие в воде ионов брома, йода, сероводорода, от которых освобождаются предварительной обработкой воды.
Определение иона SO42– . Метод определения сульфат-ионов основан на малой растворимости сульфата бария, количественно выпадающего в кислой среде при добавлении к воде раствора хлорида бария: Ba 2+ + SO42– = BaSO4↓
По массе образовавшегося осадка рассчитывают содержание иона SO42– .
Определение ионов CO32– и HCO3– . Эти ионы определяют титрованием пробы воды растворами серной или соляной кислот последовательно с индикаторами фенолфталеином и метилоранжем. Реакция нейтрализации протекает в две стадии.
Первые порции кислоты вступают в реакции с карбонат-ионом, образуя гидрокарбонат-ион:
Окраска фенолфталеина при рН = 8,4 переходит из розовой в бесцветную, что совпадает с таким состоянием раствора, когда в нем остаются лишь гидрокарбонаты. По количеству кислоты, пошедшей на титрование, рассчитывают содержание карбонат-иона. Расход кислот на титрование с фенолфталеином эквивалентен содержанию половины карбонатов, т.к. последние нейтрализуются только наполовину до HCO3 – . Поэтому общее количество CO32 – эквивалентно удвоенному количеству кислоты, затраченной на титрование. При дальнейшем титровании в присутствии метилоранжа происходит реакция нейтрализации гидрокарбонатов:
Метилоранж меняет окраску при pH = 4,3, т.е. в момент, когда в растворе остается только свободный диоксид углерода.
При расчете содержания ионов HCO3 – в воде следует из количества кислоты, пошедшей на титрование с метилоранжем, вычесть количество кислоты, идущей на титрование с фенолфталеином. Общее количество кислоты, затраченной на нейтрализацию ионов ОН – , СО32– и НСО3– , характеризует общую щелочность воды. Если рН воды ниже 4,3, то её щелочность равна нулю.
Определение ионов Ca 2+ , Mg 2+ . Имеется несколько методов обнаружения и определения содержания ионов Са 2+ и Mg 2+ . При добавлении в воду оксалата аммония (NH4)2C2O4 в случае присутствия ионов кальция образуется белый осадок оксалата кальция:
После отделения осадка оксалата кальция в воде можно определить ионы Mg 2+ с помощью раствора гидрофосфата натрия Na2HPO4 и аммиака. При наличии иона Mg 2 + образуется мелкокристаллический осадок соли магния:
Полученные осадки прокаливают и взвешивают. На основании полученных результатов вычисляется величина кальциевой и магниевой жесткости.
Наиболее быстрым и точным методом определения Са 2 + и Mg 2 + является комплексонометрический метод, основанный на способности двунатриевой соли этилендиаминотетрауксусной кислоты (трилон Б)
N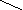
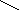
образовывать с ионами кальция и магния прочные комплексные соединения.
При титровании пробы воды трилоном Б происходит последовательное связывание в комплекс сначала ионов кальция, а затем ионов магния. Содержание ионов кальция определяют, титруя воду в присутствии индикатора — мурексида. Мурексид образует с ионами кальция малодиссоциированное комплексное соединение, окрашенное в малиновый цвет.
Ионы магния не дают комплекса с мурексидом. Трилон Б извлекает Са 2+ из его растворимого комплекса с мурексидом, вследствие чего окраска раствора, изменяется на сиреневую:
По количеству трилона Б, расходуемого на титрование, определяют содержание Са 2 + . Титрованием пробы воды трилоном Б в присутствии индикатора хромогена черного определяют суммарное содержание Са 2 + и Mg 2 + , то есть общую жесткость воды. Вода, содержащая Са 2 + и Mg 2 + , в присутствии хромогена черного окрашивается в красный цвет вследствие образования комплекса с Mg 2 + . При титровании воды в точке эквивалентности происходит изменение цвета на синий вследствие протекания следующей реакции:
Содержание Mg 2+ вычисляют по разности между общим содержанием (Са 2+ + Mg 2+ ) и содержанием Са 2 + . Трилонометрическое определение каждого иона производится при том значении рН, при котором этот ион образует с трилоном Б соединение более прочное, чем с индикатором. Для поддержания заданного значения рН к титруемому раствору добавляют буферные растворы. Кроме того, поддержание заданной величины рН обеспечивает определенную окраску индикатора. Общую жесткость воды определяют при рН > 9, кальциевую – при рН = 12.
Определение ионов Na + , K + . Производится вычислением по разности между суммой мг-экв найденных анионов и катионов, поскольку вода электронейтральна:
С достаточно высокой точностью все присутствующие в воде катионы можно определить эмиссионной спектроскопией сухого остатка.
Растворенные в воде газы определяют химическими методами или газовой хроматографией.
Определение диоксида углерода производят титрованием пробы воды щелочью в присутствии индикатора–фенолфталеина:
Определение растворенного кислорода производится йодометрическим методом.
Для анализа в пробу воды поcледовательно добавляют раствор хлорида марганца и щелочной раствор йодида калия. Метод основан на окислении свежеполученного гидроксида двухвалентного марганца содержащимся в воде кислородом:
Количество образовавшегося в воде бурого осадка гидроксида четырехвалентного марганца эквивалентно количеству растворенного кислорода. При последующем добавлении к пробе соляной или серной кислоты четырехвалентный марганец вновь восстанавливается до двухвалентного, окисляя при этом йодид калия. Это приводит к выделению свободного йода, эквивалентного содержанию четырехвалентного марганца, или, что то же самое, растворенного кислорода в пробе:
Выделившийся свободный йод определяется количественно путем титрования раствором тиосульфата натрия:
I2+ 2Na2S2O3
Йодометрический метод определения растворенного кислорода неприменим для вод, содержащих сероводород, так как сероводород вступает во взаимодействие с йодом и занижает результат. Во избежание этой ошибки предварительно связывают содержащийся в пробе сероводород в соединение, не препятствующее нормальному течению реакции. Для этой цели обычно используют хлорид ртути (II):
Определение H2S. Прежде чем приступить к количественному определению сероводорода, определяют его качественное присутствие по характерному запаху. Более объективным качественным показателем служат свинцовые индикаторные бумажки (фильтровальная бумага, пропитанная раствором ацетата свинца). При опускании в воду, содержащую сероводород, свинцовая бумага темнеет, принимая желтую (малое содержание), бурую (среднее содержание) или темно-коричневую (высокое содержание) окраску.
В водных растворах сероводород присутствует в трех формах: недиссоциированный H2S, в виде ионов HS – и S 2 – . Относительные концентрации этих форм в воде зависят от рН этой воды и в меньшей степени от температуры и общего солесодержания.
Если анализируемая вода не содержит веществ, реагирующих с иодом, то сероводород и его ионы можно определить следующим образом.
В основе количественного метода определения H2S лежит реакция окисления сероводорода йодом:
К точно отмеренному подкисленному раствору йода, взятого в избытке по отношению к ожидаемому содержанию сероводорода, прибавляют определенное количество воды. Количество йода, израсходованное на окисление сероводорода, определяется обратным титрованием остатка йода тиосульфатом. Разница между количеством раствора тиосульфата, соответствующим всему количеству взятого для анализа йода, и количеством этого же раствора, затраченного на титрование остатка йода в пробе, эквивалентна содержанию сероводорода в исследуемой пробе.
источник