Поиск и подбор лечения в России и за рубежом
Диагностические методы исследования включают пальцевое исследование прямой кишки, сигмоидо- и колоноскопию, исследование кала на скрытую кровь, радиографию с использованием бариевой клизмы, компьютерную и позитронно-эмиссионную томографию.
В последние годы всё чаще применяют определение в крови уровня карцино-эмбрионального антигена, который является индикатором метастатических процессов развития опухоли в толстом кишечнике.
Всем лицам в возрасте старше 40 лет ежегодно рекомендуется проходить пальцевое исследование прямой кишки и сдавать кал для анализа на скрытую кровь.
Во время пальцевого исследования доктор ощупывает прямую кишку изнутри пальцем в перчатке для обнаружения патологических образований. В это время можно производить забор кала для анализа на скрытую кровь. Кроме этого, у мужчин одновременно проводится обследование предстательной железы.
АНАЛИЗ КАЛА НА СКРЫТУЮ КРОВЬ
Важным скрининговым методом для обнаружения колоректального рака и полипов является анализ кала на скрытую кровь.
Для опухолей толстой и прямой кишки характерна кровоточивость с попаданием крови в кал. Небольшое количество крови, перемешанное с калом, обычно невооруженным взглядом не видно. Используемые анализы кала на скрытую кровь основаны на изменении цвета химических веществ, что позволяет обнаружить микроскопические количества крови. Данные тесты являются достоверными и недорогими.
При проведении анализа небольшое количество кала наносится на специальную карточку. Обычно забирается три последовательных образца кала. При положительном анализе кала на скрытую кровь вероятность наличия полипа толстой кишки равна 30-45%, а вероятность рака толстой кишки составляет 3-5%. Если рак толстой кишки обнаружен при подобных обстоятельствах, то диагностика считается ранней, а долгосрочный прогноз — благоприятным.
Важно помнить, что положительный результат анализа кала на скрытую кровь вовсе не обязательно означает наличие у человека рака толстой кишки. Кровь в кале может появляться при самых разных состояниях. Тем не менее, при обнаружении в кале скрытой крови необходимо провести дополнительное обследование, в том числе ирригоскопию, колоноскопию и другие тесты для исключения рака толстой кишки и выявления источника кровотечения. Кроме этого, важно понимать, что отрицательный результат анализа кала на скрытую кровь не означает отсутствие колоректального рака или полипов. Даже при идеальных условиях анализ кала на скрытую кровь упускает, по крайней мере, 20% случаев рака толстой кишки. У многих пациентов с толстокишечными полипами результат теста на скрытую кровь является отрицательным. При подозрении на опухоли толстого кишечника, а также при наличии высокого риска развития колоректальных полипов и рака гибкая сигмоидоскопия или колоноскопия проводится даже при отрицательных результатах теста на скрытую кровь.
Начиная с 50-летнего возраста, всем лицам, каждые 3-5 лет рекомендуется проведение гибкой сигмоидоскопии.
Гибкой сигмоидоскопией называется сокращенный вариант колоноскопии (обследование прямой кишки и нижних отделов толстой кишки с помощью специальной трубки).
Применение скрининговой сигмоидоскопии снижает летальность от рака толстой кишки. Это происходит в результате выявления у лиц с отсутствием симптомов полипов или рака на ранней стадии. При обнаружении полипа или опухоли рекомендуется проведение полной колоноскопии. При колоноскопии без открытого оперативного вмешательства можно полностью удалить большинство полипов. Врачи рекомендуют проводить скрининговую колоноскопию вместо гибкой сигмоидоскопии всем здоровым лицам, начиная с возраста 50-55 лет.
Пациенты с высоким риском развития колоректального рака могут проходить колоноскопию с возраста менее 50 лет. Например, пациентам с раком толстой кишки в семейном анамнезе рекомендуется начинать колоноскопию на 10 лет раньше, чем ближайшему родственнику был поставлен самый первый диагноз рака, или на 5 лет раньше, чем у ближайшего родственника был выявлен самый первый предопухолевый полип. Еще более ранняя колоноскопия рекомендуется пациентам с наследственными синдромами рака толстой кишки, такими как САП, АСАП, ННРТК и MYH-полипоз. Рекомендации зависят от генетического дефекта: например, при САП колоноскопию можно начинать с подросткового возраста для отслеживания развития полипов толстой кишки. Кроме этого, для исключения рецидива колоноскопию следует проводить пациентам, у которых полипы или рак толстой кишки отмечались ранее. У пациентов с длительным течением хронического язвенного колита (более 10 лет) риск развития рака толстой кишки повышен, а поэтому для обнаружения предраковых изменений в стенке кишечника им следует регулярно проходить колоноскопию.
Для проведения колоноскопии используется тонкий длинный зонд, который вставляется через прямую кишку для обследования внутренних поверхностей толстого кишечника. Колоноскопия считается более точным методом, чем рентгенологическое исследование.
При обнаружении полипов, обычно с помощью колоноскопа проводится их удаление, образец ткани отправляется на гистологическое исследование. Патоморфолог изучает полип под микроскопом для обнаружения признаков озлокачествления. Большинство удаляемых при колоноскопии полипов являются доброкачественными. Но у многих из них бывают признаки предопухолевого состояния. Удаление предраковых полипов предотвращает развитие из них в дальнейшем колоректального рака.
Если при проведении колоноскопии обнаруживается злокачественная опухоль, то производится биопсия (забор небольших образцов ткани) с последующим их исследованием под микроскопом. Если биопсия подтверждает диагноз рака, проводится определение стадии опухоли. Это позволяет выявить ее распространенность в другие органы. Для колоректального рака характерно распространение в легкие и печень. Поэтому при определении стадии опухоли обычно используется рентгенография органов грудной клетки, УЗИ или компьютерная томография легких, печени и органов брюшной полости.
При ирригоскопии — рентгенологическом исследовании толстой и прямой кишки пациент получает клизму с бариевой взвесью (белая жидкость, содержащая барий). Барий не проницаем для рентгеновских лучей и позволяет увидеть контуры толстого кишечника при рентгенографии.
В некоторых случаях проводится анализ крови на раково-эмбриональный (или карцино-эмбриональный) антиген (РЭА). РЭА — это вещество, которое образуется некоторыми раковыми клетками. Иногда высокое содержание РЭА обнаруживается у пациентов с колоректальным раком.
В настоящее время доступно генетическое исследование для обнаружения наследственных синдромов рака толстой кишки, таких как САП, АСАП, ННРТК и MYH-полипоз.
Генетическое консультирование с последующим генетическим тестированием необходимо проводить в тех семьях, члены которых страдают раком толстой кишки, множественными толстокишечными полипами или другими видами рака, например, мочеточников, матки, 12-перстной кишки и т.д., а также при возникновении рака в молодом возрасте.
Генетическое тестирование без предварительного консультирования не одобряется, поскольку требует дополнительного обучения членов семьи, а полученные результаты сложны для интерпретации.
Преимущества проведения генетической консультации с последующим генетическим тестированием включают:
Выявление членов семьи с высоким риском развития рака толстой кишки, которым требуется раннее проведение колоноскопии;
Выявление членов семьи с высоким риском развития других видов рака, которым может потребоваться профилактическое обследование, например, УЗИ для выявления рака матки, анализы мочи на рак мочеточника, эндоскопическое обследование верхних отделов желудочно-кишечного тракта на рак желудка и 12-перстной кишки;
Устранение беспокойства тех членов семьи, у которых наследственные генетические дефекты отсутствуют.
+7 495 66 44 315 — где и как вылечить рак
Сегодня в Израиле рак молочной железы поддается полному излечению. По данным израильского министерства здравоохранения, в настоящее время в Израиле достигнута 95% выживаемость при данном заболевании. Это — самый высокий показатель в мире. Для сравнения: по данным Национального Канцер Регистра заболеваемость в России в 2000г по сравнению с 1980г увеличилась на 72%, а выживаемость составляет 50%.
На сегодняшний день стандартом лечения клинически локализованного рака предстательной железы (т.е. ограниченного на простате), а значит излечимого, считается либо различные оперативные методы, либо лучевые терапевтические методы (брахитерапия). Стоимость диагностики и лечения рака предстательной железы в Германии составит от 15.000 € до 17.000 €
Данный вид оперативного лечения был разработан американским хирургом Фредериком Мосом и успешно применяется в Израиле на протяжении последних 20 лет. Определение и критерии операции по методу Моса разработаны Американским колледжем операции Моса (ACMS) совместно с Американской академией дерматологии (AAD).
Нано-Нож (Nano-Knife) — новейшая технология радикального лечения рака поджелудочной железы, печени, почек, легких, простаты, метастазов и рецидивов рака. Нано-Нож убивает опухоль мягких тканей электрическим током, сводя к минимуму риск повреждения близлежащих органов или кровеносных сосудов.
Технология Кибер-Нож была разработана группой врачей, физиков и инженеров Стендфордского Университета. Эта методика была одобрена FDA лечения внутричерепных опухолей в августе 1999 года, и для опухолей в остальных областях тела в августе 2001 года. На начало 2011г. действовали около 250 установок. Система активно распространяется по всему миру.
ПРОТОННАЯ ТЕРАПИЯ — радиохирургия протонного пучка или тяжело заряженных частиц. Свободно двигающиеся протоны извлекают из атомов водорода. Для этого служит специальный аппарат, который отделяет отрицательно заряженные электроны. Оставшиеся положительно заряженные частицы и есть протоны. В ускорителе частиц (циклотроне) протоны в сильном электромагнитном поле разгоняются по спиральной траектории до огромной скорости, равной 60% скорости света — 180 000км/сек.
источник
- повышенное потребление животных белков и жиров
- потребление рафинированных углеводов
- малое употребление клетчатки
- изменение секреции желчи и состава желчных кислот
- изменение кишечной флоры
- дефицит витаминов А и С
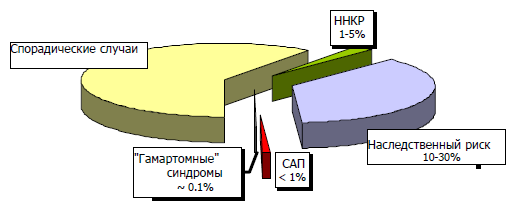
Роль наследственности в развитии рака ободочной кишки изучена недостаточно. Первичные генетические факторы являются значимыми у 5-10% больных.
- Полипозом толстой кишки
- Одиночными и групповыми полипами толстой кишки
- Язвенным колитом
- Болезнь Крона
- Предшествующая операция по поводу рака толстой кишки
- Предшествующая операция на молочной железе и яичниках
В настоящее время большинство исследователей выделяют 3 основные гистологические формы рака ободочной кишки: железистый рак, или аденокарциному (70-75% случаев), солидный рак (до 20%) и коллоидный или слизистый рак (8-17% случаев). В соответствии с классификацией ВОЗ по степени дифференцировки различают высоко дифференцированные (низкая степень злокачественности), среднюю степень дифференцировки и злокачественности и низко дифференцированные опухоли (высокая степень злокачественности).
Стадия 0 — Tis (рак in situ)
Стадия I — T1N0M0, T2N0M0
Стадия II — T3N0M0,T4N0M0
Стадия III — все значения T, N1-3M0
Стадия IV — все значения T и N, M1
Т1- опухоль прорастает слизистую оболочку и подслизистую основу кишки
Т2 — опухоль прорастает мышечный слой стенки кишки
Т3 — опухоль прорастает субсерозную ткань или неперитонезированные участки
кишки
Т4 — инвазия опухоли в периректальные ткани и соседние органы.
Тx — первичная опухоль не может быть оценена
N1 — один — три пораженных метастазами регионарных лимфатических узла
N2 — более трех пораженных лимфатических узла
N3 — поражение лимфатических узлов вдоль магистральных сосудов прямой кишки
M0 — отдаленных метастазов нет
M1 — есть отдаленные метастазы
Основным методом лечения рака ободочной кишки является хирургический . Он позволяет выполнить полное удаление опухоли в пределах здоровых тканей. Решить задачу подавления последующего опухолевого роста призваны лучевая , химио- , иммуномодулирующая терапии.
Хирургическое лечение
Хирургические операции в зависимости от распространенности опухоли и объема операции делятся на радикальные и паллиативные. Паллиативные операции могут выполняться в объеме радикальных резекций кишки или быть симптоматическими.
При радикальной операции удаляется пораженный опухолью отдел ободочной кишки одним блоком с регионарным лимфатическим аппаратом.
Паллиативные резекции выполняются при отдаленных метастазах рака и помогают предупредить в послеоперационном периоде такие осложнения, как выраженный болевой синдром, кровотечения из распадающейся опухоли, зловонные, раздражающие ткани кишечные выделения. Тем самым улучшается качество жизни запущенных онкологических больных.
Симптоматические операции без резекции кишки выполняются в объеме разгрузочных колостомий или обходных анастомозов у больных с далеко зашедшим опухолевым процессом по поводу осложнений рака.
По способу завершения различают операции с первичным восстановлением кишечной непрерывности и с наложением колостомы. Последние используются как первый этап в лечении рака, осложненного кишечной непроходимостью (с дальнейшим восстановлением) и при паллиативном лечении.
Химиотерапия
Одним из методов комбинированного лечения рака ободочной кишки является адьювантная (дополнительная) химиотерапия. Чувствительность рака ободочной кишки к ней выявлена у 25-30% больных. Адьювантная терапия проводится после операции при поражении опухолью регионарных лимфатических узлов.
Иммуномодулирующая терапия
В последнее время появляются сообщения о достоверном снижении количества рецидивов и отдаленных метастазов после проведения химиоиммунопрофилактики. Метод заключается в назначении пациентам после хирургического лечения при отсутствии метастазов в регионарных лимфоузлах в течение года еженедельно цитостатика и иммуномодулятора.
Лучевая терапия используется:
— Как предоперационный метод лечения рака прямой кишки (для уменьшения стадийности рака)
— Для послеоперационного облучения больных раком прямой кишки для сокращения частоты рецидивов
— Как основной метод лечения неоперабильного местнораспространенного рака прямой кишки.
Еще раз подчеркиваем, что только выявление колоректального рака на ранних стадиях позволяет максимально использовать весь спектр современных методов лечения и добиться хороших результатов. Рак на ранних стадиях может вызывать минимум жалоб и протекать под маской многих других проктологических и хирургических заболеваний. Поэтому своевременно обращайтесь к специалистам.
источник

Онкологический больной, согласно практике, попадает к врачам онкологам-колопроктологам уже с запущенными стадиями заболевания, вследствие чего до 50% таких пациентов умирают в первый год диагностики заболевания. Первым специалистом, к которому обращается больной с предопухолевым заболеванием или опухолью органов желудочно-кишечного тракта, является терапевт или гастроэнтеролог, затем врач-эндоскопист и лишь потом онколог; при раке прямой и ободочной кишки – соответственно врач-хирург или колопроктолог, эндоскопист и онколог.
Большинство (свыше 60%) больных колоректальным раком поступают в онкологические, хирургические и колопроктологические стационары, нередко на фоне развившихся таких тяжелых осложнений, как кишечная непроходимость, параканцерозные инфильтраты, абсцессы, кровотечения, перфорация стенки толстой кишки. Это не только существенно ухудшает непосредственные и отдаленные результаты хирургического лечения, но и является причиной увеличения удельного веса больных со стомами. Даже в специализированных стационарах формированием стом заканчивается каждая 3-4-я операция на толстой кишке; 12-20% больных являются неоперабельными.
По причине поздней диагностики заболевания летальность больных раком ободочной кишки в течение года составляет 41,8%, прямой кишки – 32,9%. К сожалению, заболевание в преобладающем количестве случаев выявляют на III-IV стадии, что не позволяет выполнять щадящие радикальные вмешательства, в частности, трансанальные микрохирургические резекции. Показатель 5-летней выживаемости составляет 83% при локализации опухоли в пределах кишечной стенки, 64% — при распространении опухоли на всю толщину кишечной стенки. При наличии метастазов в лимфатических узлах этот показатель составляет в среднем 38%, а при наличии отдаленных метастазов (чаще всего в печени) – не превышает 3%.
Важным резервом снижения заболеваемости и распространенности рака органов желудочно-кишечного тракта, его своевременной диагностики и лечения на ранних стадиях является формирование врачами групп риска развития опухолей (пациенты, имеющие предопухолевые заболевания, неблагоприятные в плане онкологии, отягощенный семейный анамнез и др.) и активное наблюдение за такими больными.
— полипы: диффузный семейный полипоз, аденоматозные полипы;
— неспецифический язвенный колит;
— болезнь Крона;
— дивертикулез;
— другие доброкачественные и воспалительные заболевания прямой кишки.
Именно предраковые заболевания являются своеобразным водоразделом между терапией, гастроэнтерологией и онкологией. Учитывая, что прогрессирование и рост опухоли через стадию дисплазии – рака in situ – до стадии метастазирования происходят в течение года, это терапевтическое и диагностическое окно должны активно использовать именно врачи общего профиля для проведения первичной и вторичной профилактики рака данной локализации. В связи с этим становится актуальным своевременное обследование толстой кишки у практически здоровых людей для выявления у них бессимптомных заболеваний (полипов, раннего рака толстой кишки и др.).
Количество заболевших и умерших от колоректального рака может быть существенно уменьшено за счет полноценного скрининга – тестирования бессимптомных пациентов, имеющих предраковые заболевания или колоректальный рак на ранних стадиях. Наиболее частой находкой при проведении скрининга являются аденоматозные полипы, распространенность которых, по данным скрининговых колоноскопий, составляет 18-36%.
Согласно рекомендациям Американского общества рака, для своевременной диагностики рака в бессимптомной популяции в естественных (обычных) условиях риска показано проведение следующих методов обследования:
— пальцевое исследование прямой кишки – ежегодно у лиц старше 40 лет;
— исследование кала на скрытую кровь – ежегодно у лиц ≥ 50 лет;
— фиброколоноскопия – каждые 3-5 лет у лиц старше 50 лет (в нашей стране с учетом радиоэкологической ситуации – каждые 2 года).
— наличия хронических воспалительных заболеваний кишечника, аденоматозных полипов, рака другой локализации и др.;
— семейного анамнеза (наличие одного или двух родственников первой линии родства с колоректальным раком или семейным диффузным полипозом кишечника);
— возраст старше 50 лет (более 90% больных колоректальным раком – лица данной возрастной категории; средняя степень риска).
Превентивная колопроктологическая программа должна включать активное выявление бессимптомных полипов и рака толстой кишки на ранней стадии, их адекватное и своевременное хирургическое лечение. Эффективное наблюдение за выявленными больными позволяет предотвратить возникновение новообразований в толстой кишке у 94,4% больных, предупредить прогрессирование онкологической патологии в 94,7-99,5% случаев.
Возраст является важным фактором риска колоректального рака как у мужчин, так и у женщин. После 50 лет заболеваемости колоректальным раком увеличивается с 8 до 160 и более случаев на 100000 населения. Количество аденоматозных полипов толстой кишки у лиц в возрасте 50-75 лет увеличиваетс на 20-25%. Таким образом, люди, которым исполнилось 50 лет, даже при отсутствии симптоматики составляют группу умеренного риска колоректального рака. Вторую категорию – группу повышенного риска колоректального рака (20%) – составляют лица с генетической и семейной предрасположенностью, страдающие хроническими воспалительными заболеваниями кишечника и диффузным семейным полипозом.
Группа высокого риска колоректального рака определена в соответствии с Амстердамскими критериями (наличие злокачественных опухолей в двух поколениях, наличие рака у родственника первой линии в возрасте до 50 лет). В этом случае скрининг колоректального рака определяется врачом перед началом скрининга для выбора объема исследований и частоты их проведения.
- Выявлялись ли у пациента в прошлом аденоматозные полипы или колоректальный рак?
- Имеет ли пациент хронические воспалительные заболевания кишечника (язвенный колит, болезнь Крона и др.), предрасполагающие к развитию колоректального рака?
- Отягощен ли семейный анамнез в отношении колоректального рака или аденоматозного полипа толстой кишки? Если да, то как часто среди родственников первой степени родства и в каком возрасте рак или полип были впервие диагностированы?
Положительный ответ на любой из этих вопросов должен расцениваться как фактор риска развития колоректального рака.
Скрининг колоректального рака является комплексным обследованием и включает проведение теста на скрытую кровь в кале, выполнение сигмоскопии, колоноскопии, рентгеноконтрастных иследований, определение поврежденной ДНК в кале и др. Условием успешности скрининговой программы является соблюдение множества условий, важнейшими из которых представляются осведомленность и активность врачей первичного звена, готовность пациента к проведению скрининговых тестов, своевременность их выполнения и проведения необходимого лечения, последующего активного наблюдения за пациентами и т.д.
Причина поздней диагностики рака данной локализации и госпитализации больных заключается в отсутствии государственной программы по профилактике и ранней диагностике хронических заболеваний толстой кишки (полипов толстой кишки, колоректального рака, неспецифического язвенного колита, болезни Крона и др.), а также в снижении доступности населению, особенно жителям сельской местности, специализированных видов медицинской помощи, в том числе проктологической и онкологической.
Широкая информативность врачей-хирургов, терапевтов, гастроэнтерологов, колопроктологов о современных требованиях к проведению скрининга колоректального рака способствует своевременной диагностике и лечению этой патологии на начальном этапе и снижению показателей заболеваемости населения колоректальным раком.
Таким образом, объединение усилий основных звеньев в области здравоохранения и утверждение целевых государственных программ будут способствовать решению проблемы успешной профилактики и лечения рака толстой кишки, которая остается актуальной и требует принятия незамедлительных мер.
Уже на ранних доклинических стадиях развития колоректального рака в содержимом кишечника могут быть выявлены кровь и другие элементы тканей толстой кишки, что можно установить при исследовании кала на скрытую кровь. Как свидетельствуют результаты проведенных рандомизированных испытаний, использование данного исследования в качестве скринингового позволяет улучшить диагностику заболевания на ранних стадиях, снизить показатели смертности на 15-45% в зависимости от типа выполненного исследования и частоты его проведения.
В настоящее время одним из наиболее эффективных методов диагностики рака и предраковых состояний является быстрый иммунохроматографический экспресс-тест (ИХА-тест). К его преимуществам относятся отсутствие необходимости в подготовке больного к исследованию или соблюдении им определенного режима питания, выявление только неповрежденного человеческого гемоглобина, что исключает возможность ложноположительных реакций, высокая чувствительность (более 95%) и специфичность. Метод ИХА – CITO TEST FOB – быстрый, удобный в применении, высокочувствительный, не требует специального оборудования и реактивов, подготовленного медицинского персонала и значительных материальных затрат (стоимость эквивалентна 4-5 долларам США).
Колоректальный канцерогенез сопровождается рядом приобретенных генетических мутаций, которые могут обуславливать изменения нормальной слизистой оболочки толстой кишки вплоть до неизлечимых стадий рака. Сегодня появилась возможность получения человеческой ДНК из кала и ее тестирования на наличие генетических и других повреждений. Проведенные исследования подтверждают чувствительность этого метода на уровне 91% для рака и 82% для аденом толстой кишки со специфичностью 93%. В будущем следует ожидать стремительного развития этого скринингового метода.
Использование сигмоскопического исследованияпозволяет на две трети уменьшить смертность от колоректального рака, локализованного в пределах досягаемости сигмоскопа. С помощью гибкой сигмоскопии можно проводить визуальный осмотр внутренней поверхности толстой кишки на расстоянии до 60 см от анального отверстия. Эта методика не только позволяет выявлять колоректальные полипы и рак, но и используется для удаления полипов и взятия биопсии для патоморфологического исследования. К преимуществам гибкой сигмоскопии относится возможность проведения ее неэндоскопистом; процедура требует меньше времени, чем колоноскопия; подготовка толстой кишки проходит легче и быстрее; нет необходимости в проведении седации. Исследование по типу «случай-контроль» показали, что скрининговая сигмоскопия снижает смертность от колоректального рака на 60-70%. Опасные для жизни пациента осложнения встречаются в 1 случае на 10000 исследований.
Это один из наиболее информативных методов исследования толстой кишки, позволяющий не только выявить полипы, взять биоптат с любого участка толстой кишки или в зоне выявленного новообразования, но и провести оперативное вмешательство – полипэктомию в любом отделе толстой кишки. Имеются доказательства того, что проведение скринингового колоноскопического исследования позволяет существенно снизить показатели заболеваемости колоректальным раком, особенно у больных с аденоматозными полипами, уменьшить смертность пациентов с колоректальным раком. Однако сложность выполнения, высокая стоимость и неудобство для пациента существенно ограничивает использование колоноскопического исследования в качестве скрининга. 5-летний интервал между скрининговыми исследованиями для лиц со средней степенью риска развития колорктального рака (если предыдущее исследование было отрицательным) оправдан, так как среднее время развития аденоматозного полипа с трансформацией в рак составляет по меньшей мере 7-10 лет. Однако, в нашей стране, учитывая радиоэкологическую ситуацию, этот срок должен быть сокращен до 2-3 лет. в обнаружении дисплазии слизистой оболочки и опухолей толстой кишки существенную помощь оказывает хромоэндоскопическое исследование с использованием метиленового синего или индигокармина.
Спиральная компьютерная томография с последующей компьютерной обработкой дает трехмерное изображение толстой кишки с высоким разрешением. Исследование является неинвазивным и не сопровождается развитием серьезных осложнений. Выполняется после стандартной подготовки толстой кишки и инсуффляции в нее воздуха, что неудобно для пациента и сопровождается лучевой нагрузкой. Поскольку данный метод не может визуализировать плоские аденомы, его экономическая целесообразность (стоимость процедуры эквивалентна 80-100 долларам США) недостаточна, чтобы причислить его к категории широко распространенных скрининговых тестов.
В настоящее время нет рандомизированных исследований, подтверждающих снижение смертности или заболеваемости колоректальным раком в результате проведения скринингового ирригоскоического исследования у лиц со средней степенью риска развития заболевания.
источник
Колоректальный рак – патология онкологического происхождения, характеризующаяся возникновением злокачественного новообразования в толстом кишечнике. Заболеванию свойственно быстрое течение, поэтому оно нуждается в своевременном лечебном воздействии. Образованию опухоли подвержены больше люди в возрасте свыше 40 лет.
Колоректальный рак – это такое онкозаболевание, появляющееся в толстой и прямой кишке, и находится на втором месте по после поражения бронхо-легочной системы. Специалисты считают данный недуг очень опасным, поскольку долгое время он себя никак не проявляет, это ведет к позднему диагностированию, а впоследствии – к неблагоприятному исходу.
Симптоматика колоректального рака возникает на 3-4 стадии его развития, и признаки достаточно размыты и схожи с многими проктологическими либо гастроэнтерологическими патологиями. Диагностика подразумевает скрининг колоректального рака, а также инструментальные, лабораторные исследования.
Терапия требует оперативного вмешательства в совмещении с приемом лекарственных средств, химиотерапией, облучением.
Прогноз колоректального рака будет зависеть от этапа, при котором начались терапевтические мероприятия. Если недуг обнаружен на первой стадии, результат – положительный. Но поскольку онкозаболевание скоротечно метастазирует, излечение возможно лишь при своевременном хирургическом вмешательстве.
Определенной причины образования колоректального рака не имеется. Но к способствующим развитию заболевания факторам относят следующее:
- сидячий образ жизни;
- генетический фактор;
- злоупотребление вредными привычками;
- болезнь Крона, диабет;
- полипоз;
- присутствие у человека иных онкологических недугов;
- малое потребление продуктов с наличием растительной клетчатки;
- трещины прямой кишки;
- ожирение;
- иммунодефицитные состояния;
- воспалительные патологии в кишечнике;
- язвенный колит.
Онкологическое заболевание возникает при мутации клеток кишечника с последующим их перерождением в злокачественные. Обычно болезнетворный процесс начинается с появления полипов. При различных вызывающих факторах (слабый иммунитет, кишечные расстройства) отмечается быстрое развитие онкологии.
Ранняя симптоматика колоректального рака такова:
- чувство боли в нижней области живота, усиливающаяся после приема пищи;
- в момент опорожнения кишечника отмечается боль, чувство дискомфорта;
- понос;
- признаки анемии;
- в фекалиях наблюдается слизь, кровяные вкрапления;
- ощущение не до конца опорожненного кишечника;
- ложное желание к дефекации.
Когда уже перешли метастазы в иные внутренние органы, симптомы колоректального рака у женщин, мужчин следующие:
- недомогание, слабость;
- тошнота, рвота, не доставляющая облегчения;
- кровотечение из заднего прохода;
- вероятность к инфекционным патологиям, с трудом, вылечивающимся;
- бессонница;
- увеличение температуры тела, почти всегда держится в пределах 37-38°С;
- сухость во рту, чувство жажды;
- головокружение, болит голова;
- астения;
- потеря аппетита, резкое похудание.
Из-за всего этого у человека начинаются психоэмоциональные проявления: раздражительность, депрессия, апатия.
Важно посетить специалиста при начальных признаках недуга. Так как болезнь будет вовремя диагностирована, что в несколько раз увеличивает шансы на успешное излечение.
Врачи различают такие виды опухолей:
- Аденокарцинома – наиболее распространенная форма рака, опухоль происходит из железистых тканей.
- Плоскоклеточная – метастазы возникают очень рано, прогнозы обычно неблагоприятные.
- Солидная – основывается из клеток железы, является классом низкодифференцированной формы новообразования.
- Скиррозная – очень редкая стадия, складывается из межклеточной жидкости обычно с малым числом клеточных элементов.
- Перстневидная – новообразование похоже на перстень с камнем. Самая страшная форма недуга, зачастую ведет к летальному исходу пациента причем в первые годы течения патологического процесса.
- Меланома – новообразование состоит из пигментных тканей, располагается в районе прямого кишечника.
От степени поражения, диаметра опухоли, присутствия метастаз различают стадии колоректального рака:
- Нулевая – онкологический процесс не развивается за участками слизистой, не простирается по всему организму. Когда заболевание выявлено на этом этапе – 5-летняя выживаемость гарантирована почти в 99% заболевших случаев.
- Первая стадия – в ткани, вовлеченные в онкопроцесс, присоединяется мышечный слой, новообразование способно дотягиваться до подслизистых клеток. Метастаз здесь еще нет, если определить диагноз на этом этапе 5-летняя выживаемость будет в 90% случаев.
- Вторая – увеличение опухоли отмечается за пределы кишки, переходит на висцеральную брюшину, а также ближайшие органы. Прогноз здесь составляет 60-70%.
- Третья – разрушаются лимфатические узлы, брыжейки, образование большого размера. При таком диагнозе 5-летняя выживаемость составляет в меньшей – 20%, а в большей степени – 50% случаев.
- Четвертая – отмечается широкое метастазирование. Поражению поддаются дальние лимфоузлы, внутренние органы (пищевод, печень). Производить операцию уже нет смысла, выживаемость – 5%.
По характеру развития симптоматики выделяют следующие формы:
- Токсико-анемическая – основные признаки колоректального рака: повышенная утомляемость, недомогание, слабость, небольшое увеличение температуры тела.
- Диспепсическая – тошнота, рвота, ощущение боли в животе, снижение аппетита и массы тела, отрыжка.
- Энтероколитическая – характеризуется кишечными расстройствами.
- Обтурационная – присутствуют признаки кишечной непроходимости.
Метастатический колоректальный рак зачастую ведет к сложным усугублениям болезни – инвалидности, образованию иных патологий, становится рецидивом первостепенного фактора.
Диагностические мероприятия включают обязательный способ скрининга колоректального рака пациентов, у которых предрасположенность и риск развития КРР, либо есть похожие признаки. Метод является комплексом действий, помогающим правильно провести онкологическое обследование на начальном этапе, когда симптомов практически еще нет.
Человек без каких-либо проявлений к специалисту не пойдет, в связи с этим, у кого есть склонность к недугу проходят диспансеризацию в обязательном порядке.
В качестве диагностики колоректального рака применяется:
- пальпационное исследование – в момент прощупывания врач способен обнаружить опухоль в отделе прямой кишки; данный метод выявляет 70% карцином;
- эндоскопия (колоноскопия, ректоскопия) – изучает внутренний слой кишечника;
- гемоккультный тест – диагностикой этого метода является кровотечение, его выявление.
Когда имеются все схожие на онкозаболевание признаки, производится:
- анализ на колоректальный рак мочи, крови;
- рентгенография с добавлением контрастного вещества;
- КТ, МРТ;
- УЗИ;
- колоноскопия, ирригоскопия;
- биохимический анализ крови;
- иммунохимический тест.
Комплексный скрининг колоректального рака поможет установить правильный диагноз, после которого начинаются соответствующие лечебные действия.
Терапия онкологии у мужчин, женщин состоит в полном иссечении болезненного участка, а также в предупреждении метастаз, рецидива после операции. С этой целью лучевая терапия используется, химиотерапия.
Хирургическое лечение колоректального рака – это более эффективный способ, при котором возможно добиться лучшего результата. Метод, техника выполняется исходя от месторасположения новообразования. Перед вмешательством проктолог-гастроэнтеролог определяет характер роста, стадию опухоли.
В процессе операции производится резекция патологической области, кишки. Кроме этого, при наличии удаленных метастаз доктор иссекает клетчатку около пораженного участка, включая регионарные лимфоузлы.
Когда образование уже на позднем этапе, удаляются близкорасположенные ткани, втянутые в процесс. После такого обычно необходимо восстановление кишки, установление колостомы.
Локальная химиотерапия при колоректальном раке способствует устранению самой опухоли, но только, если она обладает невысокой стадией. Посредством системного химического лечения возможно исправить метастатические нарушения.
Такой метод лечения колоректального рака с помощью лекарственных средств осуществляется перед хирургическим вмешательством, разрешает уменьшить размер новообразования, соответственно, и уровень самой процедуры. После резекции химиотерапия становится профилактическим мероприятием метастазирования, рецидива.
Предварительно перед операцией выполняется облучение. Оно помогает торможению роста новообразования, нормализуя резектабельность.
По окончании хирургического вмешательства лучевое лечение в комплексе с химиотерапией, способствует снижению вероятности рецидива патологии, образованию метастаз.
Метастазирование в случае колоректального новообразования способно переходить гематогенным способом, то есть, если отмечается повреждение легких, печени, включая кости, и лимфогенным методом, когда нарушаются лимфоузлы.
Если стенки толстого кишечника становятся метастатическими – это значит, что недуг приобрел последнюю стадию патологии. Кроме этого, он бывает первичным (определяется на этой стадии) либо вторичным (а именно терапевтические действия не оказали положенного результата). У половины заболевших раком выявляется первичная форма метастатической опухоли, из-за чего прогноз обычно негативный.
Если колоректальный рак обнаружился своевременно, не на поздней стадии его развития, прогноз на излечение и выживаемость – благоприятный. Но он заметно снижается при наличии уже 2 стадии течения недуга. На 4 этапе болезни выживает 1 человек из 10 заболевших.
Поскольку нестабильность при колоректальном раке, то есть длительное отсутствие симптоматики, важны профилактические меры.
Основой профилактики колоректального рака является:
- своевременная терапия доброкачественных образований;
- отказ от вредных привычек (курения, спиртного);
- упрочнение иммунитета;
- употребление витаминов, минералов;
- прием кисломолочных изделий, растительного масла;
- недопущение ожирения;
- употребление достаточного количества воды (примерно 2 л в день);
- обязательное вылечивание кишечных патологий;
- устранение запоров;
- здоровый образ жизни (плавание, физкультура, прогулки на свежем воздухе).
Людям с синдромом Линча (или по-другому, наследственным неполипозным колоректальным раком) рекомендуется употреблять обезболивающие лекарства, Аспирин. Они уменьшают риск появления злокачественных опухолей в прямой кишке. Однако любые медикаменты должны быть назначены доктором.
Информация на нашем сайте предоставлена квалифицированными врачами и носит исключительно ознакомительный характер. Не занимайтесь самолечением! Обязательно обратитесь к специалисту!
Автор: Румянцев В. Г. Стаж 34 года.
Гастроэнтеролог, профессор, доктор медицинских наук. Назначает диагностику и проводит лечение. Эксперт группы по изучению воспалительных заболеваний. Автор более 300 научных работ.
источник
Рассматриваемая онкопатология занимает третье место по шкале распространенности раковых заболеваний в мире. Кроме того, уровень смертности от указанного недуга, особенно в западных странах, достаточно высок. Чтобы исправить сложившуюся ситуацию, специалисты рекомендуют проводить скрининг колоректального рака лицам со средним и высоким уровнем риска.
Указанная процедура предусматривает две основных стратегии: исследование кала и эндоскопические методики. Такие мероприятия способствуют выявлению предраковых изменений у практически здоровых людей.
Показания к выполнению тестов на рак прямой кишки и толстой кишки – кому необходимо пройти колоректальный скрининг прямо сейчас?
Рассматриваемая процедура показана лицам с высоким риском развития колоректального рака.
- Пациенты, у которых в истории болезни имеются сведения о наличии аденоматозных полипов.
- Те, кто перенес полноценное хирургическое лечение раковой опухоли тонкого/толстого кишечника.
- Семейный анамнез колоректальных новообразований (опухоли, аденоматозные полипы) у родственников 1-й линии родства если указанная онкопатология была диагностирована у них до пересечения 60-летнего рубежа. К повышенной группе риска также относят лиц, у которых у двоих и более родственников первой линии не зависимо от их возраста был диагностирован КРР.
- Воспалительные заболевания кишечника: болезнь Крона и неспецифический язвенный колит.
- Наследственные синдромы. В первую очередь, это касается:
— Семейного аденоматозного полипоза.
— Синдрома Пейтца-Егерса. Помимо полипоза органов жкт, диагностируется также пигментация кожных покровов и слизистых оболочек.
— Наследственного неполипозного колоректального рака.
— Синдрома множественных гамартом. Указанные новообразования являются доброкачественными, и они могут располагаться в отделах жкт, щитовидке, головном мозге, органах мочевыделительной и репродуктивной системы.
Семейный анамнез и колоректальный рак
Противопоказания к колоноскопии, входящей в программу колоректального скрининга — кому не назначат это исследование?
Рассматриваемая процедура применяется только по отношению к здоровым людям. Если же у пациента недуг кишечника уже выявлен, надобности в проведении колоректального скрининга у него нет.
- Период вынашивания ребенка.
- Аллергические реакции, либо плохая переносимость анестетических средств.
- Патологии жкт, при которых у пациента наблюдается резкое беспричинное снижение веса за последние полгода, наличие крови в каловых массах согласно проведенным тестам, а также железодефицитная анемия.
- Болезни крови, что связанны с ее свертываемостью.
- Диагностирование у пациента сопутствующих недугов, при которых колоноскопия представляет опасность для здоровья и даже жизни. К подобным заболеваниям относят:
— Сахарный диабет, что сопровождается сосудистыми обострениями.
— Злоупотребления алкогольными напитками.
— Серьезные сбои в работе сердца и/или печени.
— Нарушение мозгового кровообращения, на фоне которого развивается кислородное голодание ГМ.
Кроме того, колоноскопию не назначают, если в течение года был сделан анализ кала на скрытую кровь, либо проводились следующие диагностические мероприятия:
Начало проведения скрининга, если речь идет о наследственном факторе, будет определяться возрастом самого пациента, а также возрастом родственников, у которых была выявлена та или иная патология кишечника:
- После 40-летнего возраста назначают колоноскопию, которую в дальнейшем повторяют раз в 5 лет при диагностировании колоректального рака у родителей, братьев/сестер, детей пациента до достижения ими 60 лет. Этот же принцип распространяется на тот случай, если указанная онкопатология была диагностирована у двух и более родственников первой степени не зависимо от их возраста. Доктор также может назначить прохождение скрининга пациенту на 10 лет раньше возраста, при котором колоректальный рак/аденоматозные полипы были выявлены у первого ближайшего родственника.
- После достижения 10-12 лет ежегодно рекомендуется проводить сигмоскопию при диагностировании — либо при повышенном риске развития — семейного аденоматозного полипоза.
- Начиная с 20-летнего возраста, каждые 2 года следует проводить колоноскопию в случае повышенного риска появления либо при генетическом/клиническом диагностировании наследственного неполипозного колоректального рака. Допускается также начинать проводить скрининг на 10 лет раньше возраста, при котором рассматриваемый тип онкопатологии был диагностирован у самого первого родственника.
- После пересечения 50-летнего рубежа при отсутствии отягощающего семейного анамнеза и иных факторов, что могут привести к увеличению степени риска развития КРР, колоноскопию проводят единожды в жизни. При наличии противопоказаний к указанной процедуре, выбор делают в пользу гибкой сигмоскопии (1 раз на протяжении жизни, если в ходе обследования не выявлено каких-либо дегенеративных изменений). Если же сигмоскопия также нежелательна, такой группе пациентов проводят ежегодное тестирование кала на скрытую кровь.
- Каждые 1-2 года в специализированных медицинских центрах проводят колоноскопию пациентам, у которых диагностирована болезнь Крона, либо неспецифический язвенный колит. Начинать скрининг рекомендуется через 8-10 лет после начала развития указанных патологий.
Периодичность проведения скрининговой колоноскопии у пациентов с колоректальными полипами будет зависеть от типа новообразования:
- Каждые 10 лет в случае выявления гиперпластического полипа. Начинать скрининг рекомендуется через 3-6 лет после полипэктомии. Исключением является гиперпластический полипозный синдром в анамнезе, — скрининг в подобных ситуациях проводят намного чаще.
- Каждые 5-10 лет при выявлении максимум двух тубулярных аденом, параметр которых не превышает 10 мм, и которые имеют низкую степень дисплазии. Периодичность проведения колоноскопии определяется доктором на основании предыдущих результатов диагностики. Первый скрининг следует проводить не позже, чем через 3 года после удаления аденомы.
- Раз в пять лет при наличии от 3 до 10 аденом, либо при наличии одного большого аденоматозного полипа (от 1 см в диаметре). При этом, первая колоноскопия проводится не позже чем через 3 года после хирургического удаления всех аденом.
- Каждые 3 года в случае выявления более 10 колоректальных полипов. В этом случае пациенту в обязательном порядке необходимо пройти генетическое тестирование на семейный аденоматозный полипоз!
В случае резекции толстого кишечника по поводу лечения КРР, первая колоноскопия проводится в течение года после хирургической манипуляции.
Этапы колоректального скрининга – все тесты, анализы и диагностические мероприятия на выявление рака прямой и толской кишки
Скрининговые тесты на предупреждение колоректального рака включают:
- Определение скрытой крови в кале. Дает возможность выявить указанную онкопатологию у бессимптомных пациентов. Зачастую прибегают к гваяковой пробе Вебера. Достоверность результатов данного теста повышается при его проведение каждые 1-2 года в течение длительного периода. Но в этом и заключается вся загвоздка: далеко не все лица согласны активно участвовать в проведении повторных анализов на протяжении длительного времени учитывая тот момент, что к обследованию нужно готовиться. Кроме того, данный анализ может давать как ложноположительные, так и ложноотрицательные результаты. В первом случае пациентов посылают на весьма инвазивную для организма колоноскопию, которая в конечном счете оказывается ненужной. Альтернативной гваяковой пробы является иммунохимический метод определения крови в кале (FIT). Положительная сторона таких тестов – отсутствие необходимости соблюдать диету при подготовке к обследованию. Как и предыдущий анализ FIT нужно повторять каждый год, а для большей информативности его следует сочетать с инструментальными методами диагностики.
- Анализ кала на содержание ДНК.
- Гибкая сигмоскопия. Исследуемая площадь составляет 60 см, начиная от анального отверстия и до толстого кишечника. С ее помощью доктор может осмотреть левую часть толстой кишки, прямую кишку, и при необходимости взять образец патологического элемента для лабораторного исследования. Подготовка к данной манипуляции несложная, а длится она меньше, чем колоноскопия.
- Колоноскопия. Является золотым стандартом в выявлении колоректального рака. Однако такая процедура требует тщательной и длительной подготовки, а риск развития осложнений после ее проведения значительно выше, чем при гибкой сигмоскопии.
- Ирригоскопия с двойным контрастированием (ИДК). К ней прибегают при невозможности применения более информативных методик исследования толстой кишки. Минусом данной процедуры является большое количество ложноположительных результатов: артефакты кишечника могут определяться как аденомы. Однако, в половине случаев посредством рассматриваемой манипуляции удается обнаружить большие полипы.
- Компьютерно-томографическая колонография (КТК). Дает возможность получения двух- и трехмерного изображения просвета толстого кишечника. Данная скрининговая процедура нечувствительна в отношении плоских новообразований. Ее эффективность также снижается при наличии в толстой кишке нескольких полипов, что отличаются по своим параметрам. Не самой лучшей перспективой является также получение пациентом в ходе КТК определенной дозы ионизирующего излучения. С целью минимизации радиоактивного излучения европейскими странами изучается возможность использования магнитнорезонансной колонографии.
- Гваяковая смола, что используется, как основной ингредиент при тестировании каловых масс на скрытую кровь, может реагировать на некоторые овощи, фрукты, красное мясо, что может спровоцировать ложноположительные результаты. В связи с этим, за несколько дней до анализа пациентам нужно придерживаться определенной диеты.
- Женской части населения иммунохимический тест кала на скрытую кровь следует проходить после завершения менструации.
- Также за несколько дней до тестирования следует отказаться от приема препаратов, способствующих разжижению крови: варфарина, аспирина и пр.
- Перед колоноскопией и компьютерно-томографической колонографией пациенту нужно принимать слабительные средства и ставить очистительные клизмы: требуется полная подготовка кишечника.

источник
Колоректальный рак кишечника – онкологическое заболевание, которое поражает толстую и прямую кишку, которое составляет примерно 9-11% от общего числа раковых опухолей 
Статистика гласит, что он является третьей по распространенности причиной летального исхода, а эпидемиология включает практически все развитые страны, в особенности Европу.
Статистика колоректального рака в России свидетельствует о том, что заболеваемость данным видом онкологии постоянно растет.
Симптомы, по которым диагностируется рак, включают:
-
Боли, неприятные ощущения в животе;
- Частые вздутия живота;
- Нарушения дефекации (запоры, поносы);
- Недержание стула;
- Чувство неполного опорожнения после дефекации или ощущение переполненного кишечника;
- Кал с примесями крови, гноя или слизи;
- Тошнота и рвота;
- Общие признаки: снижение аппетита, чувство слабости, утомляемости, снижение массы тела, частые лихорадки.
Так, в первом случае в число признаков заболевания входят зуд в промежности, нарушения месячного цикла и появление геморроидальных узлов, а во втором – эректильная дисфункция.
Обычно данная онкология представляют собой аденокарциномы, но встречаются и другие гистологические варианты новообразований (базальноклеточные, плоскоклеточные, солидные опухоли и т.д.)
Патанатомия колоректального рака неодинакова:
- в 50% случаев он локализируется в прямой кишке,
- в 20% – в сигмовидной,
- в 15% – в толстой кишке,
- в 6-8% – в поперечной и нисходящей.
Согласно международной классификации выделяют следующие стадии опухолей кишечника:
- Стадия 0. Новообразование первично, лимфоузлы не поражены, метастазы не наблюдаются;
- Первая стадия. Опухоль прорастает сквозь стенки кишечника, лимфоузлы поражены, но метастазы колоректального рака отсутствуют;
-
Вторая стадия. Новообразование прорастает в соседние ткани и органы, метастаз также нет, как и поражений лимфоузлов;
- Третья стадия. Опухоль достигает близлежащих органов и тканей, выходит за пределы слизистой оболочки, метастазы присутствуют в 1-3 лимфоузлах, в некоторых случаях – в 4.
- Четвертая стадия. Колоректальный рак 4 стадии наиболее сложен для лечения, так как он дает множественные осложнения и затрагивает практически весь организм. В данном случае наблюдаются метастазы в мозг, легкие, печень и другие органы.
к содержанию ↑
Точная этиология и патогенез колоректального рака не выяснены, но существуют причины и факторы риска, провоцирующие развитие заболевания, которые делятся на модифицируемые (те, на которые человек может повлиять) и немодифицируемые.
Наиболее частая причина заболевания – возраст, то есть изменения, которые происходят в организме человека с течением времени (большинство пациентов с данным диагнозом – люди старше 50 лет).
В число остальных факторов, которые вызывают рак кишечника, входят:
-
Неправильное питание.
- Вредное производство, курение, алкоголизм.
- Генные мутации, случаи онкологии ЖКТ в семье – наследственный колоректальный рак наблюдается в 5-10% случаев.
- Гиподинамия.
- Кишечные воспаления (например, язвенный колит).
- Различные инфекции и новообразования.
- Иммунодефицит.
к содержанию ↑
Наиболее важную роль в терапии онкологии толстой кишки играет ранняя диагностика – метастатический колоректальный рак, который провоцирует метастазы в легких, печени, мозге и других органах, имеет очень плохой прогноз.
Диагностика включает скрининг колоректального рака (анализ кала, методы визуализации, КТ), анализ крови на онкомаркеры, внешний осмотр, позволяющий пальпировать опухоль и близлежащие лимфоузлы.
При подозрении на опухоль пациента отправляют на дальнейшие обследования – анализ на маркеры рака (антиген СА 242, СА 19-9, РЭА), тест на С-реактивный белок и ХГЧ, а также УЗИ, КТ, МРТ, биопсия, лучевая диагностика.
Если в крови присутствуют вышеуказанные антигены, повышается С-реактивный белог, ХГЧ растет, это может указывать на рост опухоли, метастазы колоректального рака в печень (чаще всего), почки и другие органы, а КТ характеристика помогает определить местоположение опухоли, ее размеры и другие особенности.
Не менее важную роль играет и определение микросателлитной нестабильности при колоректальном раке, то есть склонности клеток ДНК к мутации. Микросателлитная нестабильность определяется путем исследования срезов опухоли, которые берут во время биопсии.

Наиболее распространенными методами диагностики заболевания являются колоноскопия и анализ на скрытую кровь в кале.
Эти исследования входят в понятие скрининг – норма подразумевает отсутствие новообразований и следов крови.
Лечение колоректального рака включает разные методы, в зависимости от особенностей течения болезни:
-
Современные малоинвазивные технологии – разрушение тканей опухоли радиочастотами, ультразвуковыми волнами, лазером.
- Лучевая терапия.
- Химиотерапия первой линии, второй при прогрессировании опухоли.
- Иммунотерапия.
- Хирургическое вмешательство.
Один из новейших методов лечения заболевания – таргетная терапия колоректального рака, то есть адресное воздействие на клетки опухоли медицинскими препаратами. Чтобы подобрать таргетные препараты и оценить эффективность терапии проводится исследование гена KRAS (мутация KRAS ведет к неконтролируемому росту клеток и появлению метастазов).

Помимо вышеперечисленных методик, терапия заболевания включает другие клинические рекомендации: диета при колоректальном раке должна включать фрукты, овощи, крупы, яйца, морепродукты и исключать потребление жирного мяса, сахара, жареной, соленой и копченой пищи.
Лечение народными средствами в данном случае может проводиться только в качестве вспомогательного метода, которые будет дополнять назначенную врачом терапию.
Стандарты лечения колоректального рака за рубежом поставлены на более высокий уровень, поэтому многие пациенты с данным диагнозом выбирают клиники следующих стран:
-
Израиль;
- Германия;
- Великобритания;
- Швейцария;
- США;
- Южная Корея.
Стоимость лечения зависит от стадии заболевания, особенностей его течения и используемых методик, поэтому конечная цена определяется индивидуально.
Прогноз при данном виде онкологии зависит от стадии заболевания и других особенностей течения. На первой стадии выживаемость составляет 90%, а на четвертой стадии 
Также ухудшается прогноз выживаемости при kras мутации колоректального рака, так как в данном случае наблюдается быстрое увеличение опухоли и рост метастаз.
При метастазировании рака прогноз зависит от количества и характера метастазов – синхронные (возникают в течение 6 месяцев после постановки диагноза) и метахронные метастазы (возникают через 6 месяцев). Во втором случае прогноз для пациента более благоприятен, чем в первом.
Для прогноза результатов лечения и выживаемости используются модели прогнозирования, которые включают целый ряд аспектов (статистические данные, возраст и пол больного, характеристики опухоли и т.д.).
Профилактика колоректального рака заключается в следующем:
- В правильном, сбалансированном питании,
- Отказе от вредных привычек,
- Борьбе с гиподинамией,
- Своевременном лечении кишечных заболеваний,
- Прохождении обследований у гастроэнтеролога.
источник
 Боли, неприятные ощущения в животе;
Боли, неприятные ощущения в животе; Вторая стадия. Новообразование прорастает в соседние ткани и органы, метастаз также нет, как и поражений лимфоузлов;
Вторая стадия. Новообразование прорастает в соседние ткани и органы, метастаз также нет, как и поражений лимфоузлов; Неправильное питание.
Неправильное питание. Современные малоинвазивные технологии – разрушение тканей опухоли радиочастотами, ультразвуковыми волнами, лазером.
Современные малоинвазивные технологии – разрушение тканей опухоли радиочастотами, ультразвуковыми волнами, лазером. Израиль;
Израиль;