Данный урок — лабораторная работа разработан по предмету «Аналитическая химия» для обучающихся по профессии «Технология продукции общественного питания». В ходе лабораторной работы в основе определения общей жесткости воды используется один из методов титриметрического анализа — комплексонометрический.
Вода является универсальным растворителем на планете Земля. Как в загородных домах, так и в городе в квартирах с централизованным водопроводом существует проблема жесткой воды. Жесткость воды зависит от наличия в ней солей кальция и магния. Жесткость воды является характеристикой конкретного источника водоснабжения и не изменяется в процессе подготовки питьевой воды к централизованному водоснабжению. Как определить степень жесткости воды?
Цель: повторить основные понятия, используемые в титриметрическом анализе; научить определять общую жесткость воды комплексонометрическим методом; закрепить навыки работы с лабораторным оборудованием; развивать вычислительные навыки; воспитывать чувство ответственности и дисциплинированности при выполнении практической работы.
Оборудование: конические колбы, мерные круглодонные колбы, бюретки для титрования, реактивы: трилон Б, индикатор эриохром черный Т, водопроводная вода, аммиачно-буферная смесь; таблицы, инструкционные карты.
II. Актуализация знаний учащихся
Сегодня на уроке мы с Вами будем говорить о самом замечательном веществе на планете Земля — воде.
Вы, как будущие технологи общественного питания, будете использовать питьевую воду не только в быту, но и в своей профессиональной деятельности.
В Старом Осколе питьевая вода поступает в город из 14 водозаборов, расположенных в разных частях города и района.
1. Одинакова ли питьевая вода по своим свойствам? (нет)
2.Чем она отличается? (содержанием различных веществ — жесткостью)
Абсолютно чистой воды в природе не существует. Она всегда содержит различные примеси как в растворенном, так и во взвешенном состоянии. От концентрации и природы этих примесей зависит пригодность воды для бытовых и промышленных нужд.
3.Что такое жесткость воды?
Жесткость воды определяется содержанием в ней растворимых солей магния, кальция, гидрокарбонатов, сульфатов, хлоридов.
4. Какие виды жесткости воды Вы знаете?
Жесткость временная (карбонатная) обусловлена содержанием гидрокарбонатов кальция и магния.
Жесткость постоянной (некарбонатной) обусловленна присутствием в воде хлоридов, сульфатов и других солей магния и кальция.
Общая жесткость воды представляет сумму жесткости карбонатной и некарбонатной.
5. Почему нежелательно использовать жесткую воду в быту?
Жесткая вода образует плотные слои накипи на внутренних стенках паровых котлов и кипятильников, в ней плохо развариваются пищевые продукты, при стирке белья в жесткой воде расходуется больше мыла.
III. Изучение нового материала
Тема нашего урока «Определение общей жесткости воды комплексонометрическим методом». Запишем ее в тетради.
В ходе урока мы должны научиться практическим путем определять общую жесткость воды, используя титриметрический анализ, в частности комплексонометрический метод.
Вспомним основы комплексонометрического метода анализа.
1. В чем состоит сущность комплексонометрического метода?
Сущность комплексонометрического метода состоит в образовании комплексных соединений анализируемых катионов с органическими реагентами — комплексонами.
Титрование — постепенное добавление раствора известной концентрации до достижения точки эквивалентности.
3. Что такое точка эквивалентности?
Точка эквивалентности — момент окончания реакции, т.к. вещества реагируют между собой в эквивалентных количествах.
4. С помощью чего устанавливают точку эквивалентности? (индикатора)
Индикаторы — вещества, при помощи которых устанавливают момент эквивалентности между взаимодействующими растворами.
6. Что такое стандартный (рабочий) раствор?
Стандартный раствор — раствор с точно установленной концентрацией, используемый для титриметрических измерений.
7. Какие правила техники безопасности необходимо соблюдать при выполнении практической работы?
Правила техники безопасности при работе со стеклянной посудой; жидкостями и сыпучими, а также ядовитыми веществами.
Работу выполняем по парам. На столах имеются инструкционные карты.
IV. Выполнение практической работы
Работу выполняем по парам. На столах имеются инструкционные карты.
Цель работы: определить общую жесткость воды методом комплексонометрии.
Оборудование: бюретки, мерный цилиндр, мерные круглодонные колбы, конические колбы, цилиндры, воронки, шпатель; реактивы: раствор Трилона Б, эриохром черный Т (сухой), аммиачно-буферная смесь, водопроводная вода.
1. Мерной колбой отмерить 100 мл исследуемой Н2О и перелить ее в коническую колбу.
2. Добавить к воде 5 мл аммиачно-буферной смеси, затем 7-8 капель спиртового раствора индикатора эриохром черного Т или щепотку его смеси с NaCl или KCl (сухую).
3. Тщательно перемешать, раствор окрасится в винно-красный цвет.
4. Смесь оттитровать 0,05 Н раствором Трилона Б. К концу титрования раствор Трилона Б добавлять по каплям, встряхивая смесь в колбе после добавления каждой капли.
5.Титрование можно считать законченным если после добавления очередной капли окраска раствора приобретает синий цвет с зеленоватым оттенком и с добавлением лишней капли раствора комплексона не изменяется.
6. Определить объем трилона Б, израсходованного на титрование.
7.Титрование повторить 2-3 раза и для расчета взять среднее значение.
8. Произвести расчет общей жесткости воды.
Величину общей жесткости воды (Ж) в мг*экв/л вычисляют по формуле:
где N — нормальность раствора трилона Б, г-экв/л;
V — объем раствора трилона Б, мл;
9. Сделайте вывод о типе воды, пользуясь данными значениями жесткости воды.
Типы воды (по жесткости):
- Очень мягкие — 0-1,5 мг-экв/л;
- Мягкие — 1,5- 3,0 мг-экв/л;
- Среднежесткие — 3,0- 4,5 мг-экв/л;
- Довольно жесткие — 4,5 — 6,5 мг-экв/л;
- Жесткие — 6,5 — 11,0 мг-экв/л;
- Очень жесткие — свыше 11,0 мг-экв/л.
V. Подведение итогов работы
Сегодня на уроке мы практическим путем определили общую жесткость воды. Водопроводная вода, которую мы используем, является среднежесткой.
Какие способы устранения жесткости Вы знаете?
Способы устранения жесткости воды:
- Карбонатная (временная) жесткость — кипячение; добавление известкового молока или соды.
- Некарбонатная (постоянная) жесткость — добавление соды.
источник
Определение жесткости воды в современном мире – это обязательное условие для обеспечения работоспособности всей техники, работающей с ней. Тем не менее нельзя сказать, что такая жидкость действительно вредна для человека. Всего должно быть в меру, ведь излишне мягкая вода наносит не меньше ущерба здоровью, чем жесткая.
Начинать всегда следует с самых азов, чтобы было полное понимание проблемы. В нашем случае, прежде чем приступать к определению жесткости воды, сначала нужно понять, что она собой представляет. По результатам экспертизы, проведенной в 2011 на кафедре химии и экологии Новгородского университета им. Ярослава Мудрого, для природной натуральной воды жесткость является абсолютно нормальным явлением. Вплоть до момента появления современной техники этот вопрос вообще мало кого интересовал, тысячелетиями люди спокойно употребляли ее в том виде, в котором она есть. Придают воде жесткость растворенные в ней соли магния и кальция. Само понятие жесткости возникло по результатам ощущения людей, так как когда насыщенная этими солями и другими элементами вода вступает во взаимодействие с мылом, пена практически не образуется, затрудняя стирку или мытье.
Прежде чем понять, какую воду пить, следует учитывать тот факт, что жесткость не является однородной величиной. Есть как минимум две основные разновидности:
Зависят эти виды от типа растворенных солей, которые в любой жесткой воде присутствуют всегда вместе, составляя общую жесткость. Тем не менее разделять их можно и нужно. Временная жесткость напрямую зависит от наличия бикарбонатных и гидрокарбонатных анионов. Главная их особенность – разложение во время кипячения. В результате распада получается непосредственно сама вода, углекислый газ и карбонат кальция, который уже практически не растворяется. Получается, что от временной жесткости можно без особых проблем избавиться при помощи простого поднятия температуры воды до +100 градусов. В качестве примера можно привести любой чайник. После продолжительного использования можно обнаружить внутри осадок, который и является результатом описанного выше процесса распада. Все же, что не разлагается подобным образом, относится к постоянной жесткости, избавиться от которой без специальной обработки практически невозможно.
Это необходимо для того, чтобы понимать, какую воду пить можно без опаски, а также для того, чтобы любая техника, взаимодействующая с водой, не вышла из строя. Для человека излишне жесткая вода вредна. Но даже если этот параметр будет находиться на приемлемом для нашего организма уровне, все равно оборудование это не устроит. Аквариумы, кофейные, стиральные и посудомоечные машины, чайники, мультиварки и множество других вариантов техники требует воду строго определенной жесткости. Обычно справиться с этим помогают фильтры типа «Гейзер-3», однако зачастую такая мера может даже считаться излишней. Прежде чем тратить на них деньги, рекомендуется сначала провести тест на жесткость воды, ведь вполне возможно, что этот показатель и так на нормальном уровне.
Как уже было сказано выше, в первую очередь ущерб человеку наносит не какой-то определенный тип воды, а полное отсутствие баланса в организме.
- Плохое растворение пищевых продуктов (связано с катионами Ca 2 + и Mg 2 +).
- Кофе, чай и любые другие подобные напитки завариваются очень плохо.
- При длительном употреблении возможно расслабление желудка.
- Жесткая вода может стать причиной образования камней в почках.
- Насыщает организм требуемыми ему элементами.
- Улучшает состояние зубов, уменьшает вероятность возникновения кариеса.
- Жесткая вода является причиной поломки большинства видов техники.
- Выводит шлаки, но попутно вымывает полезные элементы (калий, магний и кальций). В результате кости становятся более хрупкими. Также не лучшим образом воздействует на сердечно-сосудистую систему.
- Негативно воздействует на гипофиз-адреналиновую систему.
- Оказывает плохое влияние на водно-солевой баланс организма.
Таким образом, определение жесткости воды должно производится не с целью избавиться от нее, а для того, чтобы свести негативное воздействие к минимуму и привести употребление такой жидкости к требуемому организмом балансу.
Согласно ГОСТу, питьевая вода должна проверяться на жесткость строго в лаборатории, посредством титриметрического анализа. Для этого сначала необходимо взять пробы, объем которых должен быть не менее 400 кубических сантиметров (0,4 литра). В качестве емкости, в которой будет производиться хранение, может использоваться любая тара, если она изготовлена из стекла или полимерного материала. Очень важно провести анализ не позднее чем через 24 часа после отбора пробы. В особых случаях, когда необходимо увеличить этот срок, производится подкисление жидкости посредством добавления соляной кислоты. В таком состоянии она может храниться уже около 1 месяца.
Среди всех методов определения жесткости воды данный вариант заслуженно считается самым достоверным и комплексным. В его основе лежит процесс образования соединений трилона вместе со щелочноземельными элементами ионов. Минимальный показатель жесткости, который поддается определению при помощи этого способа, – 0,1 о Ж (нормой считается 7-10 о Ж). В качестве пробы может быть использована обычная вода из-под крана. Лучшим выходом в ситуации с подозрением на повышенную жесткость является сразу же посетить соответствующую лабораторию, так как никакие домашние методы не смогут выдать точные данные. Но о них — ниже.
Полностью описывать весь процесс нет никакого смысла, так как воспроизвести его самостоятельно, без нужных навыков и химических элементов и оборудования невозможно. Тем не менее можно выделить несколько основных принципов реакции, которые сохраняются в любой ситуации и присущи абсолютно всем вариантам:
- Всегда должен быть способ, позволяющий зафиксировать эквивалентность реакции, которая и является основой для определения жесткости.
- Анализ проводится очень быстро.
- Должно выполняться требование стехиометричности процесса. Проще говоря, это значит, что в процессе проведения реакции не должны образовываться никакие побочные продукты.
- С момента начала реакции ее невозможно повернуть вспять или остановить.
Для определения жесткости воды в домашних условиях можно использовать специальные приспособления, купить которые не составит особого труда (они не запрещены и общедоступны). Выглядят они как стандартные тестовые полоски. Для использования достаточно погрузить одну из них в воду, требующую проверки, на указанный в инструкции период времени. В результате изделие изменит свой цвет. При использовании таких полосок для определения жесткости воды главной проблемой является определить, каков именно показатель жесткости. Чтобы это сделать, нужно сравнивать цвет на полосе и примеры с описанием на упаковке. К сожалению, далеко не всегда можно сразу же понять, что именно показывает приспособление, и даже в более четкой ситуации точность данных оставляет желать лучшего. В целом такие тест-полоски подходят только для общего понимания того, насколько жесткая или мягкая вода.
Проверить воду из-под крана на жесткость также можно при помощи подручных средств. Правда, это скорее занимательный опыт для детей, чем действительно вариант тестирования показаний жидкости.
- Банку емкостью 1 литр (или любую другую подобную емкость).
- Стакан в форме цилиндра.
- Любые весы (удобнее всего использовать электронные).
- Линейку.
- Мыло хозяйственное (72% или 60%).
- Дистиллированную воду.
Для проверки необходимо взять 1 грамм мыла, измельчить его и поместить в стакан. После этого следует подогреть дистиллированную воду, но не доводить до кипения. Ее следует налить в тот стакан, в котором уже лежит мыло. В итоге оно обязано растворится в воде. Следующий шаг – налить еще больше воды. После этого следует налить в банку обычной воды из-под крана и медленно вылить мыльную жидкость из стакана и перемешать (медленно). Если образуется пена, то это — показатель жесткости. К сожалению, более или менее четко сказать, каков именно ее уровень, при помощи такого метода практически невозможно.
Еще один вариант определения жесткости питьевой воды – воспользоваться специальным прибором – TDS-метром. В принципе, он предназначен для определения электропроводимости воды, на что влияют как непосредственно соли (создающие жесткость), так и множество других элементов, что не дает нужного уровня точности. Более того, показания прибора обычный человек, не умеющий их считывать, не поймет и скорее всего запутается. Попробуем упростить задачу. Подавляющее большинство таких устройств в качестве единиц измерения используется некие ppm. У нас же применяются другие варианты, основанные на эквиваленте миллиграмма на литр жидкости. В среднем, 1 наша единица (мг-экв/л) равняется 50,05 зарубежным ppm. По правилам, концентрация солей (т.е. жесткости) должна быть не более 350 ppm или же 7 мг-экв/л. На эти цифры и стоит ориентироваться. Если же прибор будет отечественным, все значительно облегчается. Хуже всего, когда подобное приспособление произведено где-то в Китае или другой подобной стране, где используются собственные единицы измерения. Тогда придется самостоятельно искать их эквивалент и переводить в привычные нам показания.
Из других приборов, способных определять жесткость воды, отдельно следует отметить уникальное устройство АКМС-1. Это достаточно большой стационарный агрегат, сходный по размерам с фильтрами «Гейзер-3». Просто так в домашних условиях с его помощью проверять жидкость не представляется возможным. Именно поэтому такие приспособления используются в первую очередь на производстве, где жесткость воды может повлиять на работу дорогостоящей техники или нанести другой подобный вред. В отличие от всех остальных аналогов, АКМС-1 действительно быстро и точно показывает текущий уровень жесткости, позволяя оператору своевременно реагировать. При помощи этого приспособления можно как пускать воду к рабочим агрегатам напрямую, если она не представляет для них угрозы, так и предварительно ее фильтровать. Это, конечно же, выльется в дополнительные затраты, но зато поможет сэкономить на ремонте техники, который обойдется значительно дороже.
Учитывая все указанное выше и требования ГОСТ, вода питьевая должна регулярно проверяться на уровень жесткости. Тем не менее принимать радикальные меры по ее умягчению не стоит, так как вредны оба состояния – слишком жесткая и слишком мягкая. Только в той ситуации, когда показатели действительно выше или ниже, стоит предпринимать какие-то действия. К слову, если с жесткостью регулярно борются, то про слишком мягкую воду практически не слышно, а ведь на это также нужно обращать не меньше внимания.
источник
Метод определения общей жесткости воды основан на том, что ионы кальция и магния связываются трилоном Б в комплексные соединения. О конце реакции судят по изменению цвета индикатора хромогена черного от розово-малинового до синевато-серого. Появление синевато-серого окрашивания свидетельствует об отсутствии ионов Са 2+ и Mg 2+ в растворе, т. е. о полном связывании их с трилоном Б.
В коническую колбу вместимостью 250 мл отмеривают 100 мл исследуемой воды, добавляют 5 мл аммиачного буферного раствора, индикатор хромоген (сухую смесь) и медленно титруют 0,1 н раствором трилона Б до перехода окраски в серовато-синюю.
Общую жесткость воды Жо, ммоль экв/л, вычисляют по формуле
где V1 – объем 0,1 н раствора трилона Б, израсходованный на титрование пробы, мл; К – коэффициент нормальности раствора трилона Б (К = Nфакт / 0,1); N1 – нормальность раствора трилона Б; V2 – объем исследуемой пробы воды, мл.
Определение карбонатной жесткости воды
Оттитровывают 100 мл воды 0,1 н раствором HCl в присутствии метилового оранжевого до перехода окраски от желтой к розовой. Карбонатную жесткость Жк, ммоль экв/л, вычисляют по формуле
где V3 – объем HCl, который пошел на титрование, мл; N2 – нормальность HCl, моль/л; V2 – объем воды, который взят для анализа, мл.
Некарбонатная жесткость определяется как разница между общей и карбонатной жесткостью
Определение количества диоксида углерода
В колбу поместите 200 мл исследуемой воды, добавьте 2 капли раствора фенолфталеина и взболтайте. Если вода окрасилась в интенсивный розовый цвет, это значит, что в ней нет растворенного диоксида углерода. Отсутствие окраски или очень слабая окраска свидетельствуют о присутствии растворенного диоксида углерода. В этом случае пробу титруют 0,1 н раствором NaOH до появления интенсивной окраски. Концентрацию диоксида углерода определяют по формуле
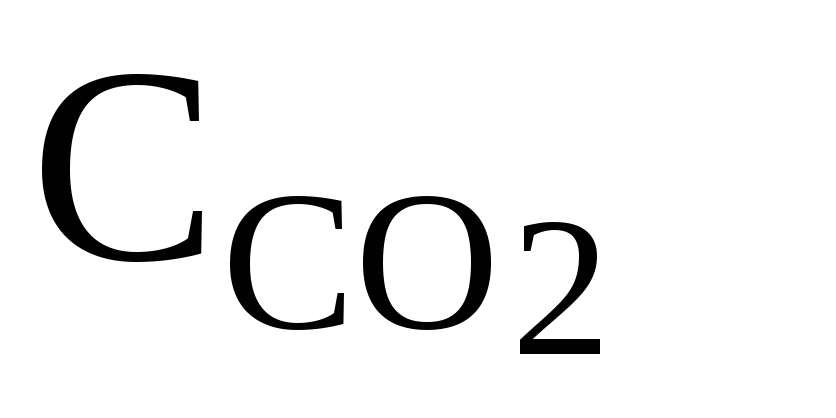
где N – нормальность NаОН, моль/л; V4 – его объем, мл.
Определение концентрации кальция и магния
К 100 мл воды добавляют 3 мл 10%-ного КОН до рН = 10–12, вносят примерно 0,2 г сухого индикатора мурексида, смешанного с сульфатом калия, и титруют трилоном Б до перехода окраски из розовой в фиолетовую.
Концентрацию кальция СК, ммоль экв/л, рассчитывают по формуле
где V5 – объем трилона Б, пошедший на титрование, мл.
Концентрацию магния См, ммоль экв/л, рассчитывают по формуле
После проведения полного обессоливания воды необходимо убедится в отсутствии в ней как катионов (Mg 2+ , Ca 2+ ), так и анионов (SO4 2– , NO3 – , Cl – ). Анализ на содержание указанных анионов в воде до ее обессоливания и после проводится качественно.
SO4 2– – раствор хлорида бария дает белый осадок сульфата бария;
Cl – – при добавлении раствора нитрата серебра образуется белый осадок хлорида серебра;
NO3 – – при добавлении раствора дифениламина в серной кислоте появляется характерное для ионов NO3 – синее окрашивание.
Определение содержания взвешенных частиц (мутность воды)
Мутность воды определяется фотоколориметрическим методом при длине волны 440 нм. Оптическую плотность измеряют в кюветах с толщиной поглощающего слоя 3 мм. Количество взвешенных частиц в воде находят по калибровочной кривой.
Регистрирующим прибором в фотоколориметре служит микроамперметр типа М907, оцифрованный в микроамперах и имеющий шкалу 0–100 делений, соответствующих шкале коэффициентов пропускания – и оптической плотности – D. При измерении со светофильтром 440 нм, отмеченным на лицевой панели колориметра черным цветом, ручку «Чувствительность» устанавливают в одно из положений 1, 2 или 3. Рабочие поверхности кювет перед каждым измерением необходимо тщательно протирать спирто-эфирной смесью, жидкость в кюветы наливать до метки на боковой поверхности кюветы. При установке кювет в кюветодержатель нельзя касаться пальцами участков поверхности кювет ниже уровня жидкости в них.
Колориметр включают в сеть за 15 мин до начала измерений. Во время прогрева кюветное отделение должно быть открыто (при этом шторка перед фотоприемником перекрывает световой пучок). В световой пучок помещают кювету со стандартным раствором, по отношению к которому производят измерения, и крышку кюветного отделения закрывают. Ручками «Чувствительность» и «Установка 100» устанавливают отсчет 100 по шкале колориметра. Затем поворотом ручки кювету со стандартным раствором заменяют кюветой с исследуемым раствором. После этого производят отсчет по шкале колориметра, соответствующий коэффициенту пропускания исследуемого раствора в процентах, или по шкале D в единицах оптической плотности. Измерения проводят 3–5 раз и окончательное значение измеряемой величины определяют как среднее арифметическое полученных значений.
источник
Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение
«Новгородский государственный университет имени Ярослава Мудрого»
Институт сельского хозяйства и природных ресурсов
Отделение естественных наук и природных ресурсов
Определение жесткости воды
Определение жесткости воды (титриметрический метод)
Методические указания к лабораторной работе
Великий Новгород, 2011 г.- 16 стр.
Важнейшим свойством природных вод является их жесткость. Жёсткость природных вод более всего обусловлена содержанием в них растворимых солей кальция и магния.
Если в воде находятся ионы металлов, образующие с мылом нерастворимые соли жирных кислот, то в такой воде затрудняется образование пены при стирке белья или мытье рук, вследствие чего возникает ощущение жёсткости. Отсюда и возникло понятие «жёсткой» воды.
В жёсткой воде плохо развариваются продукты питания, так как катионы Ca2+ и Мg2+ с белками пищи образуют нерастворимые соединения. В такой воде плохо завариваются чай, кофе. Постоянное употребление жёсткой воды может привести к расслаблению желудка и отложению солей в организме человека. В результате этого образуются камни в почках (мочекаменная болезнь).
Мягкая вода (дистиллированная вода), т. е. вода, с ничтожно малыми примесями инородных веществ и минеральных солей, используется в основном для медицинских или исследовательских целей в различных лечебно-оздоровительных программах и процедурах для вывода из организма шлаков.
Частое употребление мягкой воды может привести к тому, что из организма начнут вымываться и полезные микроэлементы: кальций, магний, калий. Прежде всего, это опасно для костей, крепость которых зависит от наличия кальция и микроэлементов, обеспечивающих нормальную работу нашего организма. Например, в регионах, где вода отличается мягкостью, т. е. пониженным содержанием минеральных примесей, ученые отмечают рост числа сердечно-сосудистых заболеваний. Там же где вода более жесткая, ситуация с заболеваниями сердца обстоит гораздо лучше – подобные случаи регистрируются нечасто. Кроме того, жесткость воды оказывает влияние и на уровень заболеваний кариесом – чем больше минеральных веществ, тем реже обращения к стоматологам.
Также установлено, что в связи с низким уровнем минерализации мягкая вода обладает неудовлетворительными органолептическими свойствами и оказывает неблагоприятное воздействие на водно-солевой обмен и функциональное состояние гипофиз-адреналиновой системы, регулирующей основные обменные процессы в организме.
При постоянном употреблении дистиллированной питьевой воды у пациентов отмечен также ряд изменений со стороны электролитного обмена – повышение концентрации хлоридов, калия и натрия в крови и усиленное их выведение с мочой. В связи с этим, для питьевой воды научно обоснована необходимость учета дополнительного критерия – физиологической полноценности.
В промышленности жёсткая вода, используемая для питания паросиловых установок, приносит особенно большой вред. При работе паровых котлов в жёсткой воде, содержащей Са(НСOз)2, Мg(НСO3)2 или CaS04, на внутренней поверхности стенок котла образуется слой накипи, уменьшающий их теплопроводность и тем самым понижающий коэффициент полезного действия установки. Замедленная теплопередача через стенки котла приводит к их перегреву и вследствие этого к ускоренной коррозии (окислению кислородом воздуха). В результате прочность стенок котла постепенно понижается, что может привести к его взрыву.
Образование осадка (накипи) при использовании воды, обладающей временной жёсткостью, связано с выпадением в осадок малорастворимых карбонатов — СаСO3 и MgCO3 . Если в воде присутствует сульфат кальция, то он выпадает в осадок из-за резкого понижения его растворимости при нагревании. Особенно прочная, но вместе с тем пористая, малотеплопроводная накипь образуется при одновременном содержании в воде гидрокарбонатов и сульфата кальция.
Соли магния (МqCI2 и МgSO4) и СаС12, содержащиеся в воде, не приводят к образованию в котлах накипи, так как они хорошо растворимы в воде, но вызывают коррозию стенок и металлической арматуры. Эти соли как электролиты способствуют протеканию электрохимических процессов на поверхности стали и тем самым ускоряет процесс её коррозии под действием воды и кислорода. Кроме того, MgCI2 и МgSO4 как соли слабого основания и сильных кислот гидролизуются, повышая концентрацию водородных ионов и создавая кислую среду, что также ускоряет процесс коррозии стали.
В химической промышленности использование жёсткой воды может оказаться недопустимым в тех случаях, когда соли, придающие ей жёсткость, препятствуют протеканию запланированных в данном производстве химические процессов или загрязняют получаемый продукт (например, полупроводниковое производство).
В строительной практике жёсткость воды должна учитываться, если гидротехническое сооружение или фундаментальные части зданий подвергаются действию грунтовых вод. Из солей, придающих воде жёсткость, вредное действие на бетон оказывают MgCI2, МgSO4 , СаSO4. Первая соль вызывает так называемую магнезиальную коррозию бетона, вторая — сульфатно-магнезиальную, третья ― сульфатную коррозию бетона. На стальные строительные конструкции, находящиеся в воде, вредное действие оказывают все соли, обусловливающие постоянную жёсткость. Причины ускорения коррозии стали те же, что и для паровых котлов.
Т. о. в каждом отдельном случае необходимо учитывать характер возможного воздействия природных вод. Для этого необходимо знать ее важнейшую характеристику — жёсткость.
В данных методических указаниях излагаются методики определения временной и постоянной жёсткости воды, а также способы её устранения.
Для количественного определения жёсткости воды применяют методы титриметрического анализа.
2. ОСНОВНЫЕ ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
2.1 Жёсткость природных вод
Жёсткость природных вод, в основном, обусловлена содержанием в них растворимых солей кальция и магния. Разумеется, жёсткость воды могут вызывать не только ионы Ca2+ и Мg2+, но и катионы других металлов, однако в естественных водах из катионов, образующих нерастворимые мыла, в значительных количествах прucутствуют только катионы кальция и магния. Эти ионы входят в состав гидрокарбонатов Са(НСО3)2, Mg(HCO3)2, сульфатов (СаSO4 и MgSO4) и хлоридов (СаСl2 и MgCl2). Содержание других растворимых солей кальция и магния в природных водах обычно очень мало.
Жёсткость, придаваемая воде гидрокарбонатами кальция и магния, называется карбонатной или временной жесткостью. В воде содержащей ионы HCO3-, устанавливается равновесие:
— разложения угольной кислоты H2CO3 ↔ СО2 + H2O (2)
— электролитическая диссоциация НСО3- ↔ Н++СО32- (3)
Равновесия в зтих процессах связаны между собой. При нагревании воды растворимость СO2 уменьшается, часть её улетучивается и равновесие (2) смещается вправо. Вследствие этого смещается вправо равновесие (I), создаётся избыток ионов ОН-, которые взаимодействуют с ионами Н, + вызывая смещение вправо равновесия (3).
В результате зтих реакций ионы НСО3- переходят в ионы СО32- no суммарному уравнению
Таким образом, при кипячении воды жёсткость, вызванная присутствием гидрокарбонатов кальция и магния, устраняется и поэтому называется временной жёсткостью.
Жёсткость, обусловленная хлоридами и сульфатами этих металлов, называется постоянной жёсткостью, она кипячением не устраняется..
Суммарная жёсткость воды носит название общей жесткости. Жесткость воды (степень жёсткости) принято выражать в ммллиэквивалентах ионов Са2+ и Mg2+ в I л воды (мэкв/л). I мэкв/л соответствует содержанию в I л воды 20,04 мг кальция или 12,16 мг магния. В зависимости от содержания ионов Са2+ и Mg2+ природные воды делятся на следующие группы:
Величина общей жесткости (мэкв/л)
2.2 Методы устранения жёсткости воды
Из сказанного выше следует, что использование для промышленных нужд природных вод возможно в ряде случаев только после предварительной очистки, которая состоит в устранении их жесткости, опреснении воды.
Применяемые на практике методы устранения жёсткости природной воды условно можно разделить на химические и физические. В первом случае уменьшение жёсткости связано с добавлением к воде различных химических веществ (реагентные методы). Физические методы понижения жёсткости воды основаны на использовании различного рода воздействия на воду (магнитное «электрическое поле, ультразвук и др.) и потому могут считаться безреагентными.
В данном методическом пособии рассматриваются только химические методы устранения жесткости воды.
В самом общем виде химические методы устранения жёсткости воды основаны на химических реакциях, в результате которых катионы кальция и магния, придающие жёсткость воде, переводятся в нерастворимые соединения (осадок). Таких методов несколько.
Если вода обладает только временной жёсткостью, то для её устранения применяют известковый способ, т. е. обрабатывают воду известью Са(OН)2:
Са(НСО3)2 + Са(OН)2 = 2СаСO3 + H2O
Mg(HCO3)2 + Са(ОН)2 = СаСO3 + MgCO3 + 2H2O
Так как ПР(MgCO3) больше, чем ПР(Mg(ОН)2), то окончательное удаление Mg2+ происходит не в виде карбоната, а в виде гидроксида:
MgCO3 + Са(ОН)2 = СаСO3 + Mg(ОН)2
Суммируя уравнения, относящиеся к гидрокарбонату магния, получим:
Mg(HCO3)2 +2Са(ОН)2 = 2СаСO3 + Mg(ОН)2 + 2H2O
Таким образом, при взаимодействии извести с гидрокарбонатами кальция и магния образуются осадки СаСO3 и Мg(OН)2.
При этом способе недопустим избыток извести, который может привести к повышению жёсткости. Поэтому количество вводимой извести должно точно соответствовать результатам анализа воды на жёсткость.
Для устранения как временной, так и постоянной жёсткости воды нередко применяют известково-содовый способ устранения жёсткости. Известь осаждает гидрокарбонаты кальция и магния, как указано выше, а сода — хлориды и сульфаты по реакциям:
CaCI2 + Nа2CO3 = CaCO3 + 2NaCI
СаSO4 + Nа2CO3 = CaCO3 + Nа2SO4
MgCI2 + Nа2CO3 = MgCO3 + 2NaCI
MgSO4 + Nа2CO3 = MgCO3 + Nа2SO4
MgCO3 также переосаждается в виде Мg(OН)2
Кроме указанных способов, основанных на добавлении к воде растворимых реактивов, широкое распространение получили способы устранения жёсткости, основанные на прохождении (фильтрации) воды через слой специальных веществ — ионообменных смол (ионитов).
Иониты представляют собой твёрдые электролиты, у которых один ион является поливалентным и нерастворимым, а ионы противоположного знака могут обмениваться на ионы, находящиеся в водном растворе. При этом, если обмениваются катионы, иониты называются катионитами, при обмене анионов — анионитами, а сам метод носит название метода ионного обмена. Этот метод может быть использован как для умягчения воды, так и для её обессоливания (деионизации).
Ионообменные свойства смолам придают имеющиеся в них активные группы. Для катионитов такими группами являются — SO3H, — SiOOH, — COOН, — ОН; для анионитов — — NH2, — NH2OH и другие. К ионитам относятся также и некоторые сложные неорганические соединения, в частности алюмосиликаты натрия (пермутиты).
В общем случае процесс диссоциации ионообменных смол можно представить в виде:
катионит: _R — СООН = RСOO — + H+
анионит: R-NH2.HOH = R-NH3 + + ОН —
Использование ионитов позволяет практически полностью удалить из воды растворенные в ней соли, являющиеся электролитами. Вода, прошедшая через такие ионообменники, близка к дистиллированной, но обходится в несколько раз дешевле воды, полученной перегонкой.
2.3 Сущность титриметрического анализа
Титриметрический анализ заключается в измерении объема титранта (раствора с точно известной концентрацией), затраченного на реакцию с определяемым веществом.
Процесс постепенного добавления титранта к анализируемой пробе называется титрованием, а момент завершения реакции – точкой эквивалентности.
Расчет в титриметрическом анализе основан на законе эквивалентов: количества вещества эквивалентов всех участвующих в реакции веществ равны.
Условимся в дальнейшем любое анализируемое вещество обозначать «Х», а любой титрант «Т», тогда закон эквивалентов можно записать следующей формулами:

С(1/z Х) или СН(Х) – молярная концентрация эквивалента анализируемого вещества, моль/л или ммоль/л (часто в аналитической химии мэкв/л количество моль-эквивалентов вещества в литре раствора);
V(Х) – объем раствора анализируемого вещества, л или мл;
С(1/z Т) или СН(Т) — молярная концентрация эквивалента титранта, моль/л или ммоль/л (часто в аналитической химии мэкв/л количество моль-эквивалентов вещества в литре раствора);
V(Т) — объем раствора титранта, л или мл;
m(X) — масса анализируемого вещества, г;
M(1/zX)- молярная масса эквивалента анализируемого вещества, г/моль;
M(1/zT) — молярная масса эквивалента титранта, г/моль.
(возможны комбинации между формулами 1 и 2)
Выделим три основных задачи, которые необходимо решить для успешного проведения титриметрического анализа.
1. Необходимо знать точную концентрацию титранта (понятие «точная концентрация» здесь условно: ясно, что оперируя экспериментальными данными, имеющими приблизительный характер, мы лишь оговариваем степень точности. Точной будем называть такую концентрацию, которая в числовом выражении имеет три значащих цифры, например: 1,38; 0, 0138; 0,400).
2. Необходимо знать точные объемы растворов реагирующих веществ, т. е. титранта и анализируемого вещества.
3. Необходимо правильно выбирать реакцию для определения и надежно фиксировать точку эквивалентности.
В титриметрическом анализе могут использоваться не все химические реакции, а только те, которые отвечают определенным требованиям. Перечислим основные:
1. реакция должна быть практически необратимой;
2. реакция должна протекать в строгом соответствии с уравнением химической реакции, без побочных продуктов (это требование часто формулируется как «стехеометричность процесса»);
3. реакция должна протекать достаточно быстро;
4. должен существовать способ фиксирования точки эквивалентности.
2.3.1 Кислотно-основные индикаторы
Многие кислотно-основные реакции удовлетворяют этим требованиям, которые были перечислены выше.
Использование в качестве титрантов только сильных кислот и сильных оснований обеспечивает практическую необратимость многих реакций.
Реакции между кислотами и основаниями не сопровождаются, как правило, какими-либо внешними эффектами, поэтому для фиксирования точки эквивалентности приходится использовать специальные вещества-индикаторы.
Кислотно-основные индикаторы – это слабые кислоты или основания, степень ионизации которых определяется концентрацией Н+-ионов в растворе.
Для индикатора-кислоты НInd существует равновесие:

Чем больше будет концентрация Н+-ионов, тем меньше будет степень ионизации индикатора. Молекулярная HInd и ионная Ind- -формы индикатора имеют разные окраски. Таким образом, концентрация ионов Н+ влияет на соотоношение концентраций HInd и ионная Ind-, что, в свою очередь, определяет характер или яркость окраски. Для характеристики растворов в химии широко пользуются водородным показателем, рН.
В первом приближении: рН = — lgс(Н+) (в дальнейшем определение будет уточнено).
В кислых растворах рН 7, в нейтральных рН=7.
Все индикаторы изменяют свою окраску не скачкообразно, а плавно, т. е. в определенном интервале значений рН, называемом интервалом перехода. Поскольку индикаторы как кислоты или основания отличаются друг от друга по силе, они имеют разные интервалы перехода (см. справочник).
Значение рН раствора в процессе титрования постоянно меняется, вблизи точки эквивалентности наблюдается так называемый скачок титрования – резкое изменение рН раствора при незначительном добавлении титранта.
Для надежного фиксирования точки эквивалентности надо подобрать такой индикатор, интервал перехода окраски которого попадал бы в скачок титрования.
В аналитической практике из индикаторов чаще других применяют метилоранж (МО, интервал перехода 3,1 – 4,4) и фенолфталеин (ФФ, интервал перехода 8,0 – 9,6). При титровании сильной кислоты сильным основанием скачок титрования находится в диапазоне рН от 4 до 10 (при концентрации реагирующих веществ, равной 0,1 моль·дм-3).
В данном случае могут использоваться метилоранж и фенолфталеин.
При титровании слабой кислоты сильным основанием точка эквивалентности смещается с линии нейтральности в щелочную область вследствие гидролиза образующейся в точке эквивалентности соли (рН>7). Скачок титрования сужается и будет тем уже, чем слабее титруемая кислота. В этом случае в качестве индикатора может быть использован из двух упомянутых индикаторов только фенолфталеин.
При титровании слабого основания сильной кислотой по завершении реакции образуется соль, гидролизирующаяся по катиону; точка эквивалентности смещается в кислую область. Для фиксирования точки эквивалентности можно использовать метилоранж, нельзя – фенолфталеин.
При уменьшении концентрации реагирующих веществ скачок титрования сужается, что усложняет проблему выбора индикатора. При титровании многоосновных кислот или солей могут наблюдаться два скачка титрования.
2.3.2 Титранты, применяемые в кислотно-основном титровании
Различают ацидиметрию – титрование с помощью кислот и алкалиметрию – титрование с помощью оснований. Ацидиметрически можно определять основания и соли, вступающие в необратимое взаимодействие с сильными кислотами (например, карбонаты – вследствие выделения газообразного продукта, бораты – вследствие образования слабой борной кислоты). Алкалиметрически можно определять кислоты и гидролизующие соли.
В ацидиметрии используется в основном раствор хлорводородной кислоты (соляная кислота), с концентрациями от 0,05 до 0,2 моль·дм-3.
Раствор НСl нельзя приготовить по точной массе исходного вещества из-за его летучести, поэтому титрант готовят приблизительной концентрации разбавлением концентрированного раствора, а затем его стандартизируют. Для этого нужно иметь первичный стандарт – вещество, раствор которого можно приготовить по точной массе и которое реагирует с титрантом. Для определения точной концентрации титранта используют вспомогательное титрование, которое и называют стандартизацией титранта.
В качестве первичных стандартов для раствора HCl используют декагидрат тетрабората натрия Na2B4O7·10H2O (бура) или декагидрат карбоната натрия Na2CO3·10H2O.
В основе стандартизации лежат следующие реакции:
В алкалиметрии титрантом является раствор гидроксида натрия. Этот раствор также нельзя приготовить по точной массе, т. к. исходное вещество вследствие его взаимодействия с углекислым газом всегда загрязнено примесью карбоната натрия.
Титрант готовят приблизительной концентрации, разбавляя водой 50%-ный раствор (т. к. растворимость карбоната натрия в концентрированном растворе NaОН мала, он из этого раствора выпадает в осадок).
Стандартизацию приготовленного титранта проводят по дигидрату щавелевой кислоты Н2С2О4·2Н2О:
2.3.3 Применение кислотно-основного титрования
Кислотно-основное титрование позволяет решать многие задачи, возникающие при клиническом анализе биологических жидкостей как при постановке диагноза, так и при лечении больных. Определение кислотности желудочного сока, буферной емкости крови, спинномозговой жидкости – примеры использования кислотно-основного титрования в повседневной практике.
С помощью этого метода можно анализировать лекарственные вещества, устанавливать доброкачественность продуктов питания (например, молока).
Большое значение имеет рассматриваемый метод и при санитарно-гигиенической оценке объектов окружающей среды, в частности определение жесткости воды.
Промышленные стоки могут содержать или кислые, или щелочные продукты. Закисление или защелачивание природных водоемов и почвы приводит порой к необратимым последствиям, в связи с чем контроль кислотно-основного баланса весьма важен.
2.3.4 Посуда, применяемая для измерения объемов растворов
Мерные колбы (рис. 1) представляют собой круглые плоскодонные стеклянные сосуды с длинной узкой шейкой (горлом) с кольцевой меткой.
Мерные колбы служат для измерения объемов растворов, приготовления растворов определенной концентрации. Объем жидкости, вмещаемой колбой, выражают в миллилитрах. На колбе указывают ее емкость и температуру, при которой эта емкость измерена. Мерные колбы имеют притёртые пробки. Обычно применяются колбы на 50, 100, 250, 500 и 1000 мл.
Рис. 1. Мер — Рис. 2. Пи — Рис. 3. Бюретки
Пипетки служат для точного отмеривания определенного объема жидкости и представляют собой стеклянные цилиндрические, оттянутые сверху и снизу узкие трубки (рис. 2,а). В верхней части пипетки имеется отметка, показывающая, до какого уровня нужно заполнить снизу пипетку, чтобы вылитая из нее жидкость имела объем, указанный на пипетке. Чаще всего пользуются пипеткой емкостью 10 или 20 мл. Существуют измерительные пипетки, имеющие вид узкой градуированной трубки (рис. 2,6).
Для наполнения пипетки на ее верхний конец надевают ( или прислоняют) резиновую грушу, а нижний опускают в сосуд с жидкостью. Сжиманием груши из пипетки осторожно вытесняют такой объем воздуха, который после разжимания груши будет замещен объемом жидкости. Жидкость набирают выше штриха желаемого объема, затем быстро снимают грушу, закрывают отверстие указательным пальцем, придерживая пипетку средним и большим пальцами.
Слегка ослабляя нажим указательного пальца на верхнее отверстие пипетки, позволяют жидкости медленно и по каплям вытекать из пипетки.
Когда нижний край мениска бесцветной жидкости опустится до нужной отметки, указательным пальцем сильно зажимают отверстие пипетки.
Вынимают пипетку из сосуда и переносят ее в колбу, куда требуется перелить жидкость. Отводят указательный палец от верхнего края пипетки и дают содержимому свободно вылиться из пипетки полностью или до нужной отметки. При выливании жидкости пипетку держат вертикально, прислоняя кончик к стенке сосуда.
Если жидкость из пипетки выливают полностью, то по окончании сливания прикасаются на мгновение нижним концом пипетки к внутренней стенке сосуда, а оставшуюся в носике пипетки жидкость оставляют в пипетке, не стряхивают и не выдувают ее (пипетка отградуирована с учетом остающейся в кончике жидкости).
Бюретки (рис. 3) предназначены для выливания из них строго определенных объемов жидкости. Они представляют собой длинные стеклянные трубки, на которые нанесена шкала c делениями. Чаще всего пользуются бюретками емкостью 25 или 50 мл, градуированными на десятые доли миллилитра. В нижней части бюретки имеется кран. Иногда в бюретках нет крана, тогда на конец ее надевают отрезок резиновой трубки со стеклянным шариком внутри и стеклянной оттянутой внизу трубкой. Оттягивая пальцами резиновую трубку от шарика, можно
спускать жидкость из бюретки. Необходимо следить за тем, чтобы оттянутый конец трубки был нацело заполнен сливаемой жидкостью.
Бюретку аккуратно заполняют жидкостью через воронку, которую слегка приподнимают. Затем (после каждого заполнения) воронку снимают с бюретки. Важно, чтобы в нижней части бюретки не оставалось пузырьков воздуха. Для этого у бюретки с носиком (капилляр) с резиновой трубкой достаточно загнуть носик бюретки вверх и, ослабив немного зажим, вытеснить воздух с небольшим количеством жидкости в стакан.
Показания уровня жидкости в бюретке следует снимать с максимально доступной вашему глазу точностью (глаз должен находиться на одной горизонтальной линии с нижним краем мениска, если жидкость бесцветна или на одной линии с верхним краем мениска, если жидкость окрашена). Необходимо пользоваться белым бумажным экраном.
На глаз всегда можно разделить самое малое деление на 3-4 части, а это значит объем жидкости может быть измерен с точностью до 2-3 сотых мл, т. е. например, 20,25 мл.
Титрование представляет собой постепенное приливание раствора известной концентрации (титранта) к анализируемому раствору точно заданного объема.
Приливание титранта производится при помощи бюретки и заканчивается в тот момент, когда количество титранта, определяемого объемом израсходованного раствора и его концентрацией, полностью прореагирует с веществом анализируемого (титруемого) раствора. Этот момент окончания титрования называется точкой эквивалентности, так как при этом количества вещества в титранте и в анализируемом растворе становятся эквивалентными. Конец титрования устанавливается визуально по изменению цвета раствора в связи с образованием или израсходованием какого-либо окрашенного вещества или с помощью индикатора, изменяющего свой цвет в присутствии (или в отсутствие) каких-либо веществ, участвующих в титровании.
Обратите внимание: изменение окраски раствора должно произойти от одной избыточной капли титранта и удерживаться не менее 1 минуты.
3. ТРЕБОВАНИЯ ТЕХНИКИ БЕЗОПАСНОСТИ
Выполняя опыты, нужно пользоваться растворами только указанной концентрации и соблюдать рекомендуемую дозировку. Не делать дополнительных опытов без разрешения преподавателя.
В работе нужно пользоваться только незагрязненными реактивами и чистой посудой. Следует аккуратно работать с реактивами: внимательно читать этикетки, не уносить реактивы общего пользования на свои рабочие столы, во избежание загрязнения реактивов держать склянки с растворами и сухими веществами закрытыми, не путать пробки, не высыпать и не выливать обратно в склянки неиспользованные или частично использованные реактивы.
Если во время работы будет пролита кислота или щёлочь, удалять их следует быстро, так как эти реактивы портят стол и другие предметы, и осторожно, чтобы не прожечь одежду и не повредить руки.
При нагревании растворов на электроплитке будьте внимательны: избегайте термических ожогов.
4 Экспериментальная часть
Цель работа — научиться определять временную, постоянную и общую жёсткость воды.
Опыт I. Определение временной жёсткости воды
Так как вода, содержащая гидрокарбонаты кальция и магния имеет щелочную реакцию (почему?), определение карбонатной жёсткости производятся непосредственным титрованием воды соляной кислотой в присутствии индикатора — метилового оранжевого.
Для анализа в коническую колбу отмерить с помощью мерного цилиндра 100 мл исследуемой воды. Добавить 2-3 капли индикатора метилового оранжевого.
В приготовленную заранее бюретку налить 0,1Н раствор соляной кислоты. Установить уровень на нулевое деление и по каплям приливать соляную кислоту в воду до изменения окраски раствора от жёлтой до оранжево-розовой. Определить объём израсходованной на титрование кислоты.
Титрование повторить ещё два раза, каждый раз доливая в бюретку кислоту до нулевого деления.
Результаты титрования записать в таблицу 1:
источник
Сокращенное обозначение молекулы трилона Б: Na2 Н2 Тр.
Это соединение легко образует прочные внутрикомплексные соли со многими катионами. Соли образуются, с одной стороны, за счет замещения металлом водорода карбоксильных групп, с другой – за счет образования координационных связей между ионами металла и атомами азота.
При комплексонометрическом титровании к раствору, содержащему определяемые ионы, добавляют постепенно титрованный раствор комплексона. По мере титрования определяемые ионы связываются в комплекс, и в точке эквивалентности они практически отсутствуют в растворе. Реакцию в общем виде можно записать так:
Чтобы реакция комплексообразования шла до конца, нужно связать выделяющиеся ионы водорода. Поэтому при титровании к анализируемому раствору добавляют смесь хлорида и гидроксида аммония – аммиачно-буферный раствор.
Для определения момента окончания титрования служат индикаторы – вещества, образующие окрашенные соединения с ионами кальция и магния или с одним из этих катионов. Такими индикаторами являются кислотный хром синий К, дающий переход от розовой к серо–голубой окраске при рН=10-11; магнезон и эриохром черный Т, называемый также хромом черным специальным ЕТ00, изменяющие окраску от вино–красной к синей; мурексид и др.
Индикаторы обладают различной чувствительностью, т.е. их окрашенные соединения с ионами кальция и магния возникают при различных, но определенных для данного индикатора и для выбранных условий концентрациях этих ионов (табл.1.1). Например, эриохром черный Т образует окрашенное соединение с кальцием при концентрации этого иона около 7 мкг – экв/л; по отношению к ионам магния этот индикатор более чувствителен, и окраска возникает уже при 4 – 5 мкг-экв/л.
Чувствительность индикатора при определении жесткости Трилоном Б
| Индикатор | Четкая окраска отмечается при концентрации, мкг-экв/л | Значение рН | |
| Са 2+ | Мg 2+ | ||
| Эриохром черный Т | 7 | 4 – 5 | 8 – 10 |
| Кислотный хром темно-синий | 2 | 1 | 9 – 10 |
| Кислотный хром синий К | 2 | 1 | 8 – 10 |
| Кислотный однохром синий | 4 | 1 | 9 – 10 |
| Мурексид | 1 | — | 10 |
В таблице 1.1 приведены концентрации ионов, при которых окраска изменяется достаточно четко и при титровании визуально хорошо отмечается.
В то же время, если взять ряд растворов с различной концентрацией магния, например 0; 0,2; 0,5; 0,7; 1,0; 1,5 мкг – экв/л, то при добавлении к таким растворам индикатора хром темно–синего или хром синего К визуально можно различить разницу в оттенках получающихся окрасок.
Таким способом можно определять визуальным колориметрированием малые величины жесткости. Для повышения чувствительности следует только предварительно превратить кальциевую жесткость в магниевую. Это можно выполнить, добавляя в анализируемую жидкость раствор трилоната магния. Поскольку комплекс с кальцием имеет большую прочность (табл.1.1), то будет протекать реакция:
Са 2+ + Na2 MgТр.→ Mg 2+ + Na2 СаТр.
и ионы кальция будут заменены в анализируемой воде ионами магния в эквивалентном отношении.
Устойчивость комплекса существенно зависит от рН раствора. Поэтому комплексонометрическое титрование ведут в заданном интервале рН, используя различные буферные растворы.
Методом комплексонометрии можно определить катионы магния, кальция, цинка, алюминия, бария, свинца и многие другие – более 40 различных катионов. Этот метод широко применяется для определения жесткости воды.
1.6 Методика определения жесткости воды комплексонометрическим методом
Метод основан на образовании при рН=10±0,2 прочного бесцветного комплексного соединения трилона Б с ионами кальция и магния. В эквивалентной точке титрования все ионы кальция и магния связываются в комплексное соединение трилоном Б, в результате чего происходит изменение окраски индикатора от красной до голубой.
Чувствительность метода составляет 0,5 мг – экв/л при титровании 0,1н
Отбор проб является важной частью анализа, необходимым условием правильности получаемых результатов.
Главные принципы, которые требуется соблюдать при отборе проб воды, состоят в следующем:
1. Проба воды, взятая для анализа, должна отражать условия и место ее отбора. При отборе поверхностных вод необходимо изучить окружающую местность и брать пробы воды выше и ниже спуска сточных вод. Пробы из трубопроводов при наличии штуцера отбирают так, чтобы скорость вытекания воды из трубопровода совпадала со скоростью отбора. Соответственно цели анализа отбирают разовые и смешанные (средние) пробы за определенный период, сливая разовые, взятые из одного и того же места, через равные промежутки времени. Иногда средние пробы отбирают одновременно из разных мест исследуемого объекта и сливают вместе. Окончательный объем средней пробы должен быть пропорционален расходу воды и определяется из условия заданного перечня определений.
2.Объем пробы должен быть достаточным и соответствовать применяемой методике анализа. Для неполного анализа, при котором определяют только несколько компонентов, достаточно отобрать 1 л воды. Для более подробного анализа следует брать 2 л воды.
3. Пробы воды отбирают в стеклянные или полиэтиленовые бутыли с хорошо подобранной пробкой, а при наличии крупных примесей – в жестяные бидоны или банки с широким горлом. Посуду, используемую для отбора проб, необходимо вымыть хромовой смесью и тщательно промыть водопроводной, а затем дистиллированной водой. Перед отбором пробы посуду ополаскивают несколько раз исследуемой водой.
4. Отбор пробы, условия транспортирования и сроки хранения определяются из условий отсутствия изменений в содержании определяемых компонентов или в свойствах воды. Необходимо учесть, что ни консервация, ни фиксация не обеспечивают постоянного состава пробы на продолжительное время.
Целью этих операций является сохранение содержания соответствующего компонента без изменения на время, необходимое для доставки и обработки пробы воды. К анализу следует приступать в кратчайший срок после отбора пробы.
1.6.3 Реактивы и оборудование
· трилон Б (фиксанал 0,1н) по ТУ 6-09-2540-87;
· серно – кислый магний MgSO4 (фиксанал 0,1н) ТУ 6-09-2540-87;
· аммиачный буферный раствор;
· индикатор эриохром черный Т или кислотный хром темно – синий ч.д.а. ТУ 6-09-3870-87Е;
· сернистый натрий 9 – водный ч.д.а., Na2 S ГОСТ 2053-77.
· Трилон Б 0,05н: раствор готовят из 0,1н трилона Б, приготовленного из фиксанала, разбавлением его в 20 раз. Для этого 50 мл трилона Б 0,1н переносят в мерную колбу на 100 мл и доводят до метки обессоленной воды. При отсутствии фиксанала берут навеску 18,613 г. трилона Б и растворяют в мерной колбе на 1000 мл. Устанавливают титр трилона Б по фиксаналу 0,1н MgSO4 . Пипеткой отбирают 10 мл 0,1н MgSO4 в коническую колбу, добавляют 90 мл обессоленной воды, 5 мл аммиачно – буферного раствора, 5 – 7 капель индикатора кислотного хром темно – синего (эриохром черного, хромогена) и титруют раствором трилона Б до голубого цвета. Должно пойти 20 мл трилона Б
· Аммиачный буферный раствор: 20 г NH4 Cl растворить в 500 мл воды, добавить 80 мл концентрированного аммиака NH4 OH и довести объем до 1000 мл.
· Индикаторы кислотный хром темно – синий или эриохром черный Т: 0,5 г индикатора растворяют в 20 мл аммиачно – буферного раствора и доводят объем до 100 мл этиловым спиртом.
Отобрав определенный объем анализируемой воды (обычно 100мл) в коническую колбу, вводят в нее 5 мл аммиачной буферной смеси, несколько капель индикатора и титруют окрашенную в розовый или фиолетово – розовый цвет жидкость раствором трилона Б. Титрование ведут медленно, по каплям, так как образование трилонатных комплексов происходит не мгновенно. Прибавление титранта, т.е. раствора трилона Б, ведут до наиболее четкого изменения цвета. Здесь необходима, как говорят, «ститровка» всего коллектива данной лаборатории. Дело в том, что резкое «от одной капли» изменение окраски титруемой жидкости происходит только при работе с 0,1н и 0,01н растворами трилона Б. Применение более разбавленных растворов создает не резкое, а постепенное изменение окраски; на это требуется, например, от трех до пяти капель 0,002н раствора трилона Б. Вследствии этого необходимо выработать по возможности единое мнение о той окраски, при которой следует считать титрование законченным. Для этого в ряд конических колб вливают по 100 мл дистиллированной обессоленной воды, добавляют в каждую колбу по 2 мл раствора сернокислого магния (MgSO4 ) конц
1 мг-экв/л и по 5 мл аммиачной буферной смеси. Затем в первую колбу вводят 0,95 мл 0,002н раствора трилона Б, т.е. с явным недостатком, а в каждую следующую на одну каплю больше, чем в предыдущую. Например, 0,95; 0,98; 1,01; 1,04; 1,07; 1,10 мл (если объем капли 0,03мл). Жидкость в последней колбе будет явно перетитрована, т.к. 1 мл 0,002н раствора трилона Б содержит 2 мкг – экв вещества, т.е. такое же количество, что и 2 мл магнезиального раствора. Составив все колбы в ряд, решают, где возникает наиболее четко визуально – определенная разница окрасок. До этого изменение цвета в дальнейшем и ведут титрование. Следует лишь иметь ввиду, что переход окраски отмечается несколько различно в зависимости от освещения. Наиболее четко этот переход заметен при естественном дневном освещении, менее отчетливо при обычном электрическом и хуже всего при лампах «дневного света». Из индикаторов четче всего переход окраски при работе с эриохром черным ЕТ00, но этот индикатор, к сожалению, и наименее чувствителен.
источник
Как выполняется контроль жёсткости воды. Понятие жёсткости, от чего она зависит. Анализ воды на жёсткость дома. Лабораторные методы контроля общей и временной жёсткости жидкости. Приборы для выполнения анализа. Методы борьбы с повышенной жёсткостью в быту. Контроль жёсткость воды или анализ воды на жёсткость нужен для определения концентрации солей в жидкости. Этот анализ можно проводить в лабораторных условиях и дома.
Жёсткость воды – термин, говорящий о процентном соотношении солевых частиц магния и калия в жидкости. Она подразделяется на две разновидности:
- Временная (такая жидкость называется карбонатная);
- Общая жёсткость (данная вода относится к некарбонатной).
Первый тип жёсткости характеризуется присутствием гидрокарбонатных солевых частиц магния и калия. Если такую воду закипятить, то элементы распадутся на карбонаты и гидроксиды и выпадут в осадок. Именно этот белый налёт часто покрывает наши чайники изнутри и собирается на других нагревательных элементах.
Для жидкости с общей жёсткостью характерно наличие других химических элементов (различных нитратов, хлоридов и тп.п). Обычно жёсткость питьевой воды связана с особенностями вашего региона, составом грунтов. Чем больше известковых пород находится в почве, тем выше жёсткость воды. Но важно не только понимать суть понятия, но и знать, как проверить жёсткость воды. Выполнить это легко как в быту, так и на заводе.
Для проверки жёсткости водопроводной воды дома можно использовать следующие способы:
- Постарайтесь обильно вспенить мыльный брусок или порошок для стирки. Если у вас образуется мало пены, то ваша вода имеет повышенную жёсткость. Это возникает по той причине, что солевые частицы калия и магния не позволяют мылу пениться. При обильной пышной пене от любого моющего средства можно утверждать, что вода нежёсткая. Но этот метод не позволят точно определить степень жёсткости.
- На вкус также можно отличить жёсткую воду от мягкой. Она более горькая. Но не все могут точно уловить горьковатый привкус солей магния и калия.
- Белый осадок в чайниках, накипь на нагревательных элементах других бытовых приборов – признак жёсткой воды. Осадок возникает из-за распада солей и выпадения их на дно. Данная особенность жёсткой воды очень вредит бытовым приборам и отопительному трубопроводу.
- От жёсткости воды зависит скорость заваривания чайного напитка. При мягкой воде на эту процедуру уйдёт от 3 до 6 мин., в жёсткой воде чай будет завариваться от 8 до 12 мин. Кстати, на вкус оба напитка будут существенно отличаться.
- Благодаря нехитрому компактному измерительному прибору можно очень легко определить жёсткость любой жидкости. Он называется TDS-метр. Агрегат измерят электропроводность жидкости. Чем выше показатель, тем больше уровень солесодержания жидкости. Обычно его ещё называют солемер. Чаще такой анализ воды на жёсткость делают владельцы аквариумов и цветоводы.
- Проверить жёсткость воды в быту можно, используя тест-полоски, продающейся в аптеках медтехники.
Для этого анализа можно использовать колориметрическую методику и принцип титрования. Процедура анализа выполняется так: порция воды смешивается с метилоранжем (индикатором), ёмкость устанавливается на светлом фоне. Во вторую тару с водой добавляют соляную кислоту, пока не получится красно-оранжевый цвет воды.
Временную жёсткость жидкости находят в процессе расчёта требуемого количества соляной кислоты по формуле: Нвр = NHCl * VHCL* 1000/ V1, где N-насыщенность раствора, V-его количество, V1-количество пробы.
Этот анализ проводят в лаборатории. Для него используют комплексонометрическую методику. Она базируется на принципе возникновения соединений ионов, подвергающихся анализу, с природными реагентами. Сначала воду в пробирке разводят раствором индикатора на спирту (чёрного этиохрома «Т»). Также для этих целей может использоваться сухая смесь кальциевых и натриевых хлоридов. В итоге полученная смесь окрашивается в насыщенный рубиновый цвет. Затем в пробирку капается вещество, называемое Трилон.
Расчёт общей жёсткости производится по уравнению: Жо=Nx*Vx*1000/V1, где N-насыщенность вещества Трилон, V-его количество, V1-количество пробы.
Как мы уже говорили выше, прибор контроля жёсткости воды называется солемер или TDS-метр. Точность проверки составляет 2%. Основной принцип работы данного агрегата построен на зависимости электропроводности жидкости от общего числа примесей солей магния и калия. То есть чем больше данных солей в воде, тем больше будут показания прибора, а следовательно, тем выше жёсткость воды.
На некоторых предприятиях и заводах наблюдается прямая зависимость между жёсткостью используемой воды и исправностью работы оборудования. Поэтому для обеспечения бесперебойной работы технологического оборудования требуется осуществлять постоянный автоматический контроль жёсткости воды.
Для этих целей используется специальное оборудование, например, анализатор «АКМС-1». Этот прибор непрерывно контролирует содержание солевых частиц кальция и магния в жидкости, поступающей в технологическое оборудование. То есть он подсчитывает общую жёсткость в пределах 0,005-25,0 мг-экв/л.
Как понять, что ваша водопроводная вода жёсткая, мы писали выше. Теперь перечислим ряд мер, позволяющих снизить жёсткость воды в домашних условиях:
- Самый простой способ – кипячение воды.
- Фильтрация воды через системы обратного осмоса (специальные мембраны).
- Использование смягчающих солей.
- Применение фильтрующих картриджей.
- Магнитное фильтрующее устройство.
- Использование ионообменной смолы в комплексе с солевым раствором.
Хотите провести контроль жёсткости воды? Заказать такую услугу вы можете у наших специалистов, для этого вам достаточно связаться с нами по указанным телефонам.
источник